Генотипирование изолятов E.coli с выявлением генов вирулентности
Генотипирование изолятов E.coli с выявлением генов вирулентности
Аннотация
Эшерихиозы являются широко распространенным заболеваниями сельскохозяйственной птицы, включая индеек. Заболевание вызывается грамм-отрицательной условно-патогенной бактерией E.coli. Патогенность микроорганизма определяется наличием совокупности генов вирулентности. Выраженность клинической картины заболевания также определяется состоянием иммунной системы организма хозяина. В качестве мер профилактики инфекционных болезней птицы часто используются карантинные мероприятия, позволяющие изолировать больных особей. Научно обоснованные профилактические мероприятия включают генотипирование патогена, позволяющее оценить эпизоотический потенциал возбудителя, идентифицировать пути передачи бактерии и найти источник инфекции. В ходе проведенной работы выяснилось большее генетическое разнообразие изолятов E.coli, выделенных из материнской линии индеек. Ген птичьего гемолизина (HlyF) присутствовал в геноме всех изолятов данной бактерии, в то время, как ген птичьего фимбриального адгезина отсутствовал.
1. Введение
К числу условно-патогенной микрофлоры птиц относится широко распространенная в природе бактерия E.coli . Обычно эта бактерия является частью микробиоты кишечника и не вызывает развития заболевания у птиц и млекопитающих. Однако, в определенных условиях, когда бактерия приобретает путем горизонтального переноса генетической информации участки ДНК с генами вирулентности, она становится патогенной для хозяина. Ситуацию отягощает скученное содержание птицы, неполноценное кормление, приводящие к снижению иммунитета , . При контактах птицы в условиях индустриального выращивания создаются условия для распространения инфекции. Отследить этот процесс можно с использованием методов генотипирования бактерий , . Широкому распространению генов резистентности к антибиотикам способствует использование последних в кормах . Существует большое число методов генотипирования бактерий , среди которых выделяются методы, основанные на полимеразной цепной реакции, в частности, с использованием праймеров к повторяющемуся генетическому элементу в геноме энтеробактерий ERIC и коротких праймеров к анонимным последовательностям в геноме RAPD . По данным генотипирования E.coli, выделенных из различных источников, бактерии разделяют на несколько кластеров, в зависимости от хозяина, например, птичьи патогены именуются группой APEC , . Цель работы заключалась в определении генетического разнообразия изолятов E.coli, выделенных из разных групп индеек и выявлении носительства генов вирулентности у бактерий. Эти вопросы на примере патогенов индеек, разводимых в условиях промышленных птицефабрик, раскрыты недостаточно, что и предопределило тему работы. Полученные данные могут быть использованы специалистами при планировании ветеринарно-санитарных профилактических мероприятий.
2. Методы и принципы исследования
Объектом исследования служили образцы геномной ДНК, выделенные из чистой культуры E.coli. Бактерии выращивались на бульоне в соответствии с общепринятыми в микробиологии правилами. В анализ были взяты 30 бактериальных изолятов, полученных из смывов клоаки индеек создаваемого среднего кросса (отцовская линия – образцы 1-10, материнская линия – образцы 11-20), а также 10 изолятов из разных органов (почки, легкие, сердце, печень и красный костный мозг) трех заболевших (павших) индеек. В момент взятия биоматериала не было найдено других индеек с клиническими признаками эшерихиоза. У павших особей диагноз «эшерихиоз» был установлен патологоанатомическим исследованием (характерная картина серозно-фибринозного перикардита, дуоденита, воспалительный процесс в тонком кишечнике, и затем подтвержден микробиологическим методом выращивания бактерии на дифференциально-диагностических средах (среда Эндо и XLD-агар).
Для выделения геномной ДНК клетки бульонной культуры E.coli осаждали центрифугированием при 3000g в микроцентрифуге, осадок суспендировали в буфере TES (50 мМ Трис-HCL, 20 мМ ЭДТА, 10 мМ NaCL, pH 8.0). Суспензия инкубировалась в течение 30 минут после внесения лизоцима (конечная концентрация 2 мг/мл) при 37°С. Затем клетки лизировали путем добавления в смесь додецилсульфата натрия до конечной концентрации 1%. Геномную ДНК E.coli выделяли с использованием фенольно-хлороформенного метода. Количество и качество выделяемой ДНК оценивали в спектрофотометре NanoDrop 2000™.
Генотипирование проводили с помощью метода RAPD-PCR с использованием HotStart ДНК полимеразы и двух праймеров – 1254 и OPL-12. Выявление генов резистентности HlyF (птичий гемолизин) и Yqi (птичий фимбриальный адгезин) осуществляли с помощью специфических праймеров, окружающих участок соответствующего гена. Последовательности праймеров и условия амплификации изложены в таблице 1. Устанавливали количество циклов – 42, начальная денатурация ДНК и активация полимеразы 95°С в течение 5 минут, затем на каждом цикле продолжительность денатурации была 15 секунд при этой же температуре. По завершении всех циклов амплификации, проводили инкубацию при температуре 72°С в течение трех минут.
Таблица 1 - Последовательность нуклеотидов и условия проведения ПЦР с RAPD-праймерами 1254, OPL-12 и праймерами для детекции генов вирулентности HlyF и Yqi
Праймеры | Последовательность нуклеотидов | Температура отжига, °С | Температура элонгации, °С |
1254 | CCG CAG CCA A | 37 | 72 |
OPL-12 | GGGCGGTACT | 37 | 72 |
HlyF | GGCCACAGTCGTTTAGGGTGCTTACC GGCGGTTTAGGCATTCCGATACTCAG | 62 | 72 |
Yqi | CTGGTGGCAACATCAAATTG ATGCAATGGCAGTACCCTTC | 62 | 72 |
После проведения амплификации продукты реакции анализировали с помощью электрофореза в 1.5% агарозном геле с бромидом этидия в буфере 1хTAE. Устанавливали напряжение в 120 В, разделение фрагментов ДНК проводили в течение двух часов. По окончании электрофореза гель помещали в систему гель-документации и производили фиксацию результатов. Для оценки длины амплификатов использовали либо рестрикты фага лямбда либо лесенку GeneRuler (Thermo Fisher Sci™).
3. Основные результаты
В процессе проведенной научно-исследовательской работы были выявлены генетические профили изолятов E.coli (Рис.1).
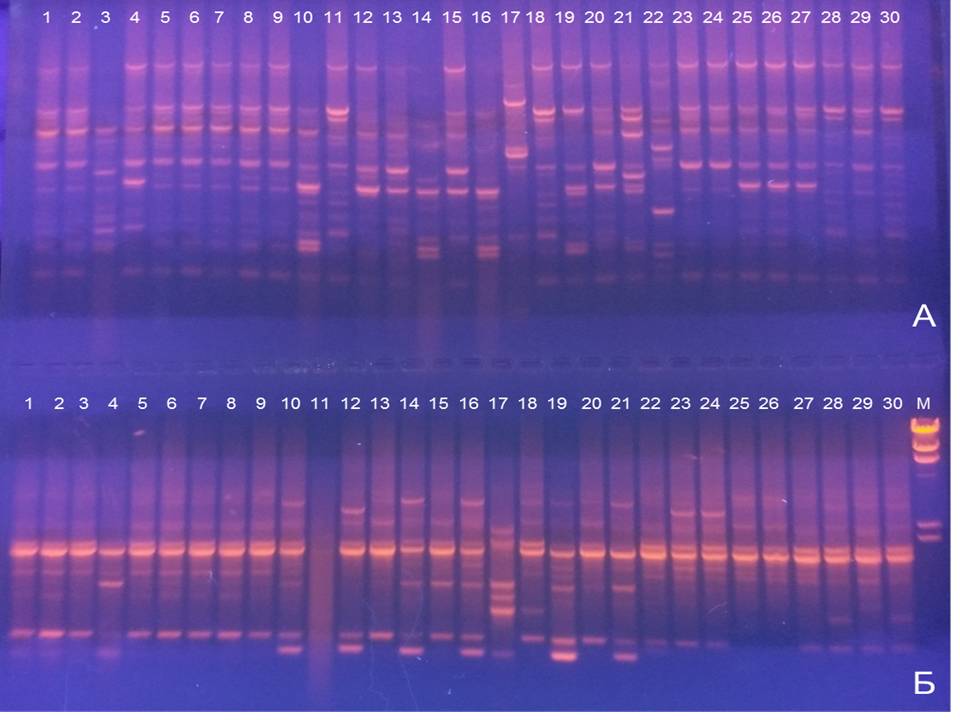
Рисунок 1 - Генетические профили 30 изолятов E.coli:
сверху (а) - праймер 1254; снизу (б) - праймер OPL-12; дорожки 1-10 отцовская линия; дорожки 11-20 материнская линия; дорожки 21-30 патологический материал из индеек
Что касается данных генотипирования изолятов, выделенных от материнской линии, то здесь просматривается большее генетическое разнообразие. Праймер 1254 был более информативным в сравнении с праймером OPL-12 в плане идентификации генетических профилей. Было выявлено восемь различающихся генотипов, что превышает количество выявленных вариантов в отцовской линии (три генотипа).
В группе изолятов, выделенных из биоматериала павших индеек обращает на себя внимание выраженная дифференциация изолятов на отдельные кластеры. Например, один кластер включал изоляты в дорожках №23 и №24, другой – №25, №26 и №27, третий – №28 и №30, выявились также и уникальные штаммы – №21, №22 и №29.
Проведение эксперимента по выявлению двух генов вирулентности HlyF (птичий гемолизин) и Yqi (птичий фимбриальный адгезин) в бактериальных изолятах, выделенных от отцовской и материнской линий, показало, что во всех образцах присутствовал ген птичьего гемолизина, а ген фимбриального адгезина отсутствовал (Рис.2.). Размер амплифицируемого фрагмента ДНК соответствовал ожиданиям (450 пар оснований) и был немного меньше, чем ярко светящийся в электрофоретической дорожке маркерный фрагмент GeneRuler в 500 пар оснований. В дальнейшем планируется проведение аналогичной работы с двумя другими генами вирулентности – Iss (фактор, повышающий выживаемость клетки в сыворотке крови), и OmpT (поверхностный белок с протеазной активностью).
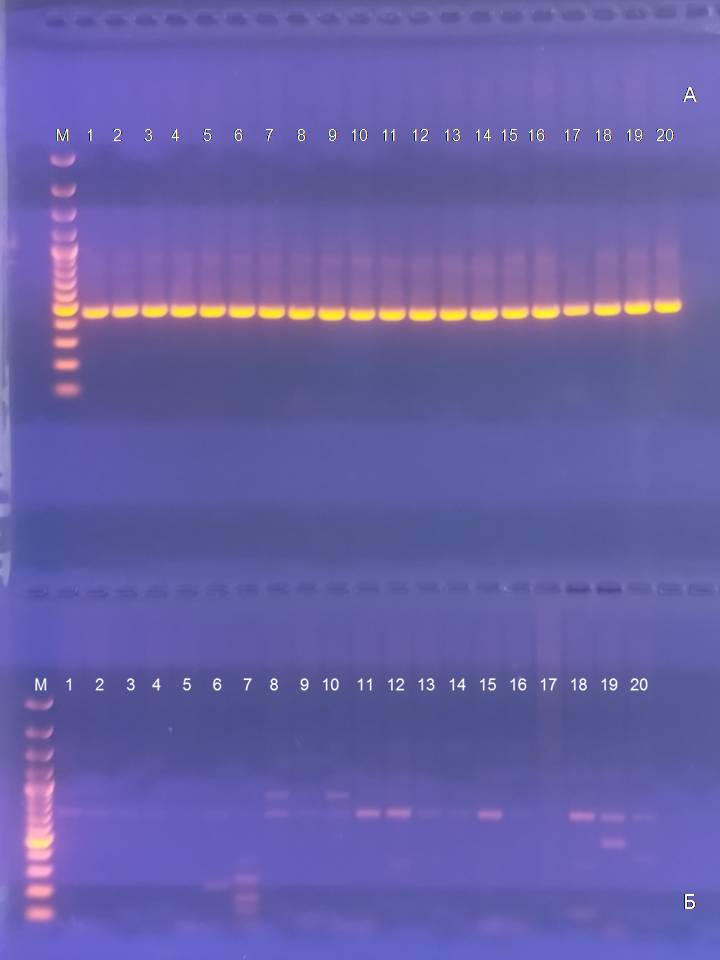
Рисунок 2 - Наличие генов вирулентности у изолятов E.coli:
дорожки 1-10 - смыв из клоаки индеек создаваемого среднего кросса, отцовская линия; дорожки 11-20 - смыв из клоаки индеек создаваемого среднего кросса, материнская линия; а – праймер для выявления гена вирулентности HlyF (птичий гемолизин); б - праймер для выявления гена вирулентности Yqi (птичий фимбриальный адгезин)
4. Заключение
Таким образом, доказано большее генетическое разнообразие изолятов в материнской группе изолятов с формированием восьми различающихся генотипов, в группе изолятов E.coli от клинически больных индеек методом RAPD-PCR удалось идентифицировать 4 генотипа. В группе изолятов от отцовской и материнской линий здоровых индеек выявлено присутствие гена вирулентности птичьего гемолизина (HlyF), в то же время четкой амплификации гена птичьего фимбриального адгезина (Yqi) не наблюдалось.
