ВЛИЯНИЕ ВЫСОКОЧАСТОТНОГО ИЗЛУЧЕНИЯ С ИМПУЛЬСАМИ НАНОСЕКУНДНОЙ ДЛИТЕЛЬНОСТИ НА ИЗОЛИРОВАННЫЕ МИТОХОНДРИИ ПЕЧЕНИ
Жаркова Л.П.1, Романченко И.В.2, Большаков М.А.3, Ростов В.В.4
1Кандидат биологических наук, доцент, Национальный исследовательский Томский государственный университет, Институт сильноточной электроники СО РАН, 2Кандидат физико-математических наук, младший научный сотрудник, Институт сильноточной электроники СО РАН, 3Доктор биологических наук, профессор, Национальный исследовательский Томский государственный университет, 4Доктор физико-математических наук, Институт сильноточной электроники СО РАН
Работа выполнена при поддержке гранта РФФИ № 16-38-60040
ВЛИЯНИЕ ВЫСОКОЧАСТОТНОГО ИЗЛУЧЕНИЯ С ИМПУЛЬСАМИ НАНОСЕКУНДНОЙ ДЛИТЕЛЬНОСТИ НА ИЗОЛИРОВАННЫЕ МИТОХОНДРИИ ПЕЧЕНИ
Аннотация
Исследовано влияние высокочастотных (ВЧ) электромагнитных импульсов на функциональное состояние митохондрий печени мышей. Выявлено снижение скорости потребления кислорода митохондриями, снижение коэффициента дыхательного контроля (КДК), а также снижение омического сопротивления суспензии митохондрий после воздействия. Указанные изменения зависели от амплитуды ВЧ импульсов (амплитуда от 0.1 до 36 кВ/см, частота от 0.6 до 1.0 ГГц, длительность от 4 до 25 нс), их количества (63 - 1000 импульсов) и суммарной поглощенной энергии. Полученные данные указывают на влияние наносекундного ВЧ излучения на функционирование мембранных комплексов митохондрий.
Ключевые слова: дыхание митохондрий, наносекундные импульсы, высокочастотное излучение.Zharkova L.P.1, Romanchenko I.V.2, Bolshakov M.A.3, Rostov V.V.4
1PhD in Biology, Associate Professor, National research Tomsk state university, Institute of high current electronics SB RAS, 2PhD in Physics and Mathematics, Associate scientist, Institute of high current electronics SB RAS, 3PhD in Biology, professor, National research Tomsk state university, 4PhD in Physics and Mathematics, Institute of high current electronics SB RAS
ULTRAWIDEBAND RADIATION WITH NANOSECOND PULSES AFFECTS ON ISOLATED LIVER MITOCHONDRIA
Abstract
The RF electromagnetic pulses effects on the functional state of liver mitochondria of mice were investigated. A reduction in mitochondrial oxygen consumption, decreasing of a respiratory rate and an ohmic resistance after exposure was showed. These changes depended on the amplitude of RF pulses and the number of pulses (amplitude from 0.1 to 36 kV/cm, frequency from 0.6 to 1.0 GHz, duration from 4 to 25 ns). The obtained data indicated the inhibitory effect of RF pulses on the state of irradiated mitochondria.
Keywords: mitochondrial respiration, nanosecond pulses, RF radiation.В настоящее время известно, что импульсное ВЧ излучение эффективно влияет на биологические объекты. В частности, ВЧ импульсы микросекундной длительности используются для противоопухолевой терапии в сочетании с химиотерапией для эффективной таргетной доставки химиопрепарата по механизму электропорации мембраны опухолевой клетки [1]. Кроме того, даже один наносекундный импульс электрического поля (более 20 кВ/см) способен вызывать аномалии в развитии облученных икринок рыб [2]. При этом наносекундные и ультракороткие импульсы ВЧ излучения (до 300 кВ/см) способны повреждать мембраны внутриклеточных органелл и обратимо нарушать целостность плазматической мембраны, резко повышать уровень свободного внутриклеточного кальция, что влияет на уровень клеточного метаболизма [3]. Так же известно, что воздействие микросекундными ВЧ импульсами сопровождается снижением уровня АТФ в облученных клетках [1]. Снижение количества АТФ, в первую очередь связано с уменьшением его продукции в результате разобщения окислительного фосфорилирования и нарушения работы электрон-транспортной цепи (ЭТЦ) на внутренней мембране митохондрий. Как представляется, ВЧ импульсы наносекундной длительности, имеющие более высокую напряженность электрического поля, должны оказывать не менее эффективное действие на вышеупомянутые структуры, и реализовывать свое влияние аналогичным образом. Митохондрии являются важнейшими клеточными органоидами, в которых химическая энергия пищевых субстратов трансформируется в энергию макроэргических связей АТФ для обеспечения энергозависимых процессов клетки. Исходя из этого, представляется логичным и перспективным изучить влияние наносекундных ВЧ импульсов на сопряжение процессов окисления и фосфорилирования изолированных митохондрий. Влияние можно оценить по интенсивности дыхания митохондрий в зависимости от параметров излучения, прежде всего от напряженности электрического поля и количества воздействующих импульсов.
Материалы и методы
Эксперименты выполнены на митохондриях из печени беспородных белых мышей, изолированных методом дифференциального центрифугирования [4]. Суспензии изолированных митохондрий объемом 60 мкл подвергались однократному воздействию ВЧ импульсов с амплитудой от 0.1 до 36 кВ/см, частотой от 0.6 до 1.0 ГГц, длительностью от 4 до 25 нс. Генерация ВЧ импульсов осуществлялась за счет возбуждения гиромагнитной прецессии в нелинейной передающей линии с насыщенным ферритом [5-6]. ВЧ импульс от нелинейной линии преобразовывался из коаксиальной TEM-моды в TE01-моду прямоугольного волновода при помощи коаксиально-волноводного перехода. Пробирка Eppendorf с суспензией помещалась в центр волновода, где амплитуда электрического поля имеет максимальное значение. После воздействия на образец ВЧ импульс поглощался в спиртовой нагрузке.
Скорость потребления кислорода изолированными митохондриями определялась с помощью измерителя кислорода АКПМ-02Л (Россия) амперометрическим сенсором АСрО2-01 в полярографической ячейке при постоянном перемешивании содержимого. Для этого в ячейку объемом 1.3 мл помещалась среда инкубации, содержащая кислород, сахарозу, MgCl2 и KH2PO4 (pH 7.4) [4], в которую добавлялась облученная или ложнооблученная суспензия митохондрий, содержащая 0.7-1 мг белка. Скорость дыхания рассчитывалась в наномолях О2 в минуту на 1 мг белка. Функциональное состояние митохондрий оценивалось по КДК.
Электрическое сопротивление суспензий митохондрий определялось с помощью измерителя иммитанса Е 7-20 (МНИПИ, Беларусь) на частотах электрического тока в диапазоне β-дисперсии. Для этого, суспензии митохондрий объемом 50 мкл (0.7-1 мг белка) заливались в измерительную ячейку со средой инкубации (1 мл), подключаемую к измерителю иммитанса.
В работе использовались облученные (обл.) и ложнооблученные (ЛО) суспензии митохондрий. Последние подвергались аналогичным манипуляциям, что и облученные, но без включения источника излучения. Для всех режимов воздействия показатели были измерены в 6 повторностях. Значимость различия в показателях дыхания облученных и ЛО митохондрий оценивалась с помощью U-критерия Манна–Уитни в программе Statistica 6.0.
Результаты исследования
При анализе функционирования митохондрий наиболее информативным считается дыхательный контроль по Чансу, который представляет изменения контроля скорости окисления субстратов со стороны АДФ [6]. В нормальных условиях, в присутствии субстрата дыхания (например, сукцинат) добавление АДФ в полярографическую ячейку с митохондриями приводит к резкому возрастанию скорости поглощения кислорода митохондриями с последующим возвращением ее к исходному уровню после фосфорилирования всей добавленной АДФ и превращении ее в АТФ (истощение АДФ, рис.1). Для оценки функционального состояния митохондрий рассчитывался КДК, который численно равен отношению скорости окисления субстрата митохондриями в присутствии АДФ (состояние 3 по Чансу со скоростью V3) к скорости поглощения кислорода после исчерпания АДФ (состояние 4 по Чансу с V4) (КДК=V3/V4). Величина КДК ЛО митохондрий в эксперименте составляла не менее 5, что указывает на эффективное сопряжение процессов окисления и фосфорилирования, и следовательно, на качественное выделение митохондрий.
Анализ полярографических кривых, полученных в результате проведенных экспериментов, позволил установить, что наносекундные ВЧ импульсы влияют на скорость дыхания митохондрий.
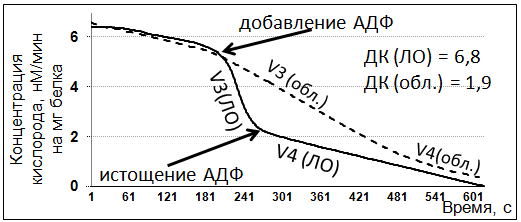
Рис. 1 – Типичные кривые поглощения кислорода ЛО (сплошной линией) и облученными (пунктир) митохондриями в разных дыхательных состояниях по Чансу [7]. V4 — скорость нефосфорилирующего дыхания при наличии в среде инкубации дыхательного субстрата сукцината и отсутствии АДФ; V3 — скорость фосфорилирующего дыхания при наличии сукцината и АДФ
Эффект влияния на митохондрии проявлялся по-разному в разных их метаболических состояниях по Чансу. А именно, после воздействия наносекундных ВЧ импульсов скорость потребления кислорода в метаболическом состоянии 4 не изменялась, тогда как в состоянии 3 (состояние активного дыхания с фосфорилированием АДФ) она существенно снижалась (рис.1). Отсюда следовало, что при снижении показателя КДК существенный вклад вносился именно величиной V3.
При этом после обучения суспензии 1000 наносекундных ВЧ импульсов наблюдалось снижение КДК митохондрий в зависимости от напряженности электрического поля. При увеличении напряженности до величины 0.15 кВ/см и более КДК монотонно уменьшался (рис.2). Это свидетельствовало об ингибирующем действии излучения на митохондрии.
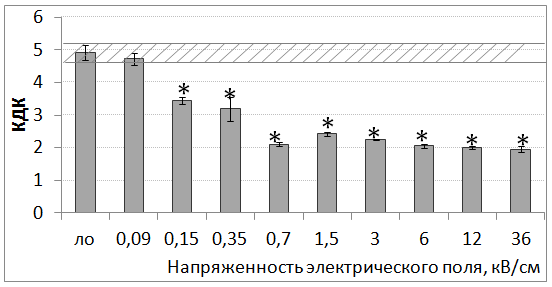
Рис. 2 – Изменение величины КДК после воздействия 1000 наносекундных ВЧ импульсов с частотой повторения 13 имп./с и напряженностью поля в импульсе 0.09 – 36 кВт/см. Заштрихованное пространство – ± ошибка среднего КДК для ЛО митохондрий. * - различия показателей значимы при р≤0.05 по сравнению с ЛО
Полученная зависимость эффекта ингибирования дыхания могла быть обусловлена либо напряжённостью электрического поля, либо суммарной поглощенной энергией. Для определения роли энергетической компоненты были проведены уточняющие эксперименты, в которых эффект измерялся при фиксированной величине суммарной поглощенной энергии, но при разном количестве импульсов и напряженности поля (при условии, что количество импульсов х напряженность электрического поля = const). Оказалось, что воздействие цуга наносекундных ВЧ импульсов с одинаковой суммарной энергией обеспечивает формирование одинакового по величине биологического эффекта. А именно, наблюдалось снижение КДК на 30 % после воздействия ВЧ импульсами c суммарной энергией 2.5 мДж за сеанс (рис. 3А) и на 61 % после воздействия ВЧ импульсами c большей суммарной 10 мДж за сеанс (рис.3Б). Таким образом, увеличение суммарной поглощенной энергии сопровождалось усилением эффекта.
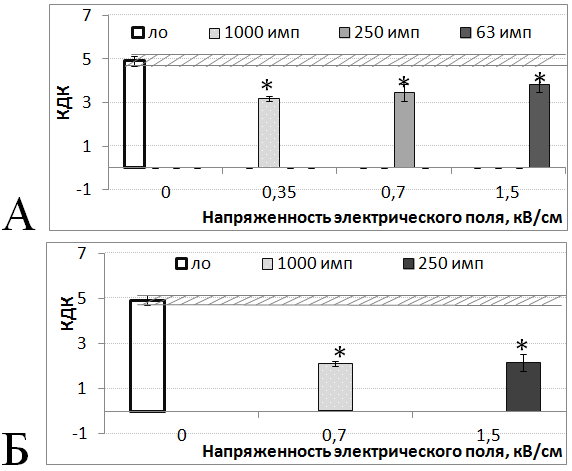
Рис. 3 – Изменение величины КДК после воздействия наносекундных ВЧ импульсов с частотой повторения 13 имп./с и суммарной энергией за сеанс облучения 2.5 мДж (А) и 10 мДж (Б) (напряженности поля в импульсе от 0.35 до 1.5 кВт/см; количество импульсов от 1000 до 63, несущая частота 0.6 ГГЦ, длительность импульса 25 нс). Заштрихованное пространство – ± ошибка среднего КДК для ЛО митохондрий. * - различия показателей значимы при р≤0.05 по сравнению с ЛО
Установленное снижение величины КДК после воздействия указывает на снижение сопряженности процессов окисления и фосфорилирования, а также нарушение интактности мембраны митохондрий. Это должно сопровождаться снижением продукции АТФ в облученных митохондриях. Подтверждением правильности такого предположения являются данные S.K. Frandsen [1], в которых показано снижение уровня АТФ после воздействия микросекундных ВЧ импульсов. Данный эффект авторы работы связывают с электропорацией мембраны клеток и внутриклеточных структур. Для проверки возможности электропорации мембран митохондрий посредством наносекундных ВЧ импульсов были проведены дополнительные эксперименты, в которых измерялось сопротивление суспензии митохондрий переменному току. Целесообразность такого подхода ранее была показана в [8] где установлено, что сопротивление электрическому току может служить индикатором влияния излучений на мембраны митохондрий. Согласно [9], при прохождении переменного тока через биологические ткани наблюдается изменение сопротивления, которое зависит от частоты тока и известно как дисперсия. При этом выделяются α-, β- и γ-дисперсии, причем область β-дисперсии (измеряемая на частотах переменного тока 104-106 Гц) связана с физико-химическим состоянием биомембран. Поэтому изменения сопротивления в данном частотном диапазоне будет отображать изменение состояния мембран.
В результате проведенных экспериментов было обнаружено, что после воздействия наносекундного ВЧ излучения сопротивление митохондрий, измеренное на частоте переменного тока 105 Гц, снижается. В частности, после воздействия 1000 наносекундных ВЧ импульсов с напряженностью 3 кВ/см омическое сопротивление уменьшилось на 23 %. Обнаруженное снижение сопротивления мембран митохондрий указывает на появление дополнительных структур неспецифической проводимости (электропор), индуцированных воздействием ВЧ излучения.
Заключение
В результате проведенных экспериментов установлено снижение уровня дыхания митохондрий в результате нарушения сопряжения процессов окислительного фосфорилирования. Эти изменения могут быть результатом нарушения структуры митохондриальной мембраны.
Снижение сопротивления суспензий митохондрий после воздействия ВЧ импульсов может быть результатом образования электропор в липидном бислое внутренней мембраны митохондрий. Это должно приводить к снижению протонного потенциала на внутренней мембране митохондрий, что, в свою очередь способствует разобщению окисления и фосфорилирования и, в итоге, приводит к снижению КДК. В результате либо возникает дефицит АТФ, либо избыточная генерация АФК (за счет нарушения работы дыхательной цепи и окислительной модификацией липидных компонент мембран митохондрий) [9, 10]. Кроме того, снижение КДК может быть обусловлено потерей митохондриального цитохрома с, изменением соотношения АТФ-синтетазной и АТФ-азной активности комплекса F0F1, снижением протонного потенциала [11, 12]. Все вышеперечисленные процессы согласуются с полученными данными о снижении потребления кислорода митохондриями в состоянии V3, снижении КДК и омического сопротивления суспензий митохондрий.
Кроме того, полученные данные указывают на то, что эффект наносекундного ВЧ излучения зависит как от напряженности электрического поля и количества воздействующих импульсов, так и от суммарной поглощенной энергии за сеанс. Зависимость эффекта от суммарной энергии согласуется с мнением T. Schunc [13], что именно величина энергии определяет эффективность электропорации. В этом случае возможно локальное повышение температуры мембран, и тогда усиление эффекта при поглощении большего количества энергии может объяснятся увеличением подвижности жирнокислотных остатков липидов митохондриальной мембраны, что будет обеспечивать повышение вероятности формирования электропор.
В тех случаях, когда наносекундное ВЧ излучение оказывает влияние на функционирование митохондрий, появляется возможность изменения внутриклеточных процессов. Это делает возможным управление метаболизмом клеток посредством таргетного воздействия наносекундного ВЧ излучения, в том числе с перспективой терапии опухолевых заболеваний. Принципиально важной является обнаруженная зависимость эффекта от количества импульсов, поскольку она позволит минимизировать воздействие на любые клетки в том числе и на опухолевые, для достижения требуемого результата. Кроме того, исследования влияния наносекундных ВЧ импульсов на клеточные мембранные комплексы могут способствовать перспективной разработке методов направленной транспортировки в клетки биологически активных соединений через индуцированные ВЧ воздействием электропоры.
Литература
- Frandsen S.K., Gibot L., Madi M., Gehl G., Rols M.P. Calcium electroporation: evidence for differential effects in normal and malignant cell lines, evaluated in a 3D spheroid model // Plos ONE, 2015, 10 (12): e0144028.
- Dong Koo Kang, S. Hamid R. Hosseini, Eri Shiraishi, Masato Yamanaka, Hidenori Akiyama Single Nanosecond Pulsed Electric Field Effects on Embryonic Development of the Medaka Fish // IEEE Transactions on Plasma Science, 2012, Volume 40, Issue 10, 2379 - 2387
- Ravi P. Joshi, K. H. Schoenbach Bioelectric Effects of Intense Ultrashort Pulses // Critical Review in Biomedical Engineering, 2010, Volume 38, Issue 3 РР. 255-304.
- Князева И.Р., Иванов В.В., Жаркова Л.П., Кутенков О.П., Ростов В.В., Большаков М.А. Влияние импульсно-периодического микроволнового излучения на функциональную активность изолированных митохондрий печени мышей // Вестник Томского государственного университета. Биология. 2011. №4. – С.113-123.
- В.П. Губанов, А.В. Гунин, О.Б. Ковальчук, В.О. Кутенков, И.В. Романченко, В.В. Ростов. Эффективная трансформация энергии высоковольтных импульсов в высокочастотные колебания на основе передающей линии с насыщенным ферритом // Письма в ЖТФ. 2009. Т. 35. В. 13. С. 81–87.
- Ю. А. Андреев, В. И. Кошелев, И. В. Романченко, В. В. Ростов, К. Н. Сухушин, Генерация и излучение мощных сверхширокополосных импульсов с управляемым спектром // Радиотехника и электроника, 2013, Т. 58, №4, С. 337-347.
- Chance B. Electron transfer: Pathways, mechanisms, and controls. 1977 № 46, P. 967-980.
- Жаркова Л.П., Афанасьев К.В., Большаков М.А., Князева И.Р., Ростов В.В. Оценка влияния импульсно-периодического рентгеновского и микроволнового излучений на биологические структуры с помощью измерения импедансных характеристик // Вестник Томского государственного университета. – 2008. – №312. – С.180-183
- Schwan H P and Foster K R RF-Field interactions with biological systems: Electrical properties and biophysical mechanisms // Proc. of the IEEE – 1980. – Vol.68. – P.104–113.
- Zorov D.B., Juhaszova M., Sollott S.J. Mitochondrial reactive oxygen species (ROS) and ROS-induced ROS release. // Physiological reviews. 2014. – 94(3). –P.909-50.
- Губский Ю.И. Смерть клетки: свободные радикалы, некроз, апоптоз: монография / Ю.И.Губский. - Винница: Нова Книга, 2015. – 360 с.
- Deleage G., Penin F., Godinot C., Gautheron D.C. Correlations between ATP hidrolisis, generation and utilization of ΔpH in mitochondrial ATPase- ATPsinthase // Biochimica et Biophysica Acta. 1983. – Vol.725. – P.464-471.
- Schunc T., Bieth F., Pinguet S., Delmote Ph Penetration and propagation into biological matter and biological effects of high-power ultra-wideband pulses: a review // Electomagnetic biology and medicine 2016. Vol.35 (1). P.84-101
References
- Frandsen S.K., Gibot L., Madi M., Gehl G., Rols M.P. Calcium electroporation: evidence for differential effects in normal and malignant cell lines, evaluated in a 3D spheroid model // Plos ONE, 2015, 10 (12): e0144028.
- Dong Koo Kang, S. Hamid R. Hosseini, Eri Shiraishi, Masato Yamanaka, Hidenori Akiyama Single Nanosecond Pulsed Electric Field Effects on Embryonic Development of the Medaka Fish // IEEE Transactions on Plasma Science, 2012, Volume 40, Issue 10, 2379 - 2387
- Ravi P. Joshi, K. H. Schoenbach Bioelectric Effects of Intense Ultrashort Pulses // Critical Review in Biomedical Engineering, 2010, Volume 38, Issue 3 РР. 255-304.
- Knjazeva I.R., Ivanov V.V., Zharkova L.P., Kutenkov O.P., Rostov V.V., Bolshakov M.A. The effect of the repetitive pulsed microwaves on functional activity of isolated mitochondria // Tomsk state university journal of biology. 2011. №4. – P.113-123.
- P. Gubanov, A. V. Gunin, O. B. Kovalchuk, V. O. Kutenkov, I. V. Romanchenko, and V. V. Rostov, Effective transformation of the energy of high-voltage pulses into high-frequency oscillations using a saturated-ferrite-loaded transmission line // Tech. Phys. Lett. 35, 42 (2009).
- A. Andreev, V. I. Koshelev, I. V. Romanchenko, V. V. Rostov, and K. N. Sukhushin, Generation and radiation of high-power ultrawideband pulses with controlled spectrum // J. Commun. Technol. Electron. 58, 297 (2013).
- Chance B. Electron transfer: Pathways, mechanisms, and controls. 1977 № 46, P. 967-980.
- Zharkova L.P., Afanasev K.V., Bolshakov M.A., Knjazeva I.R., Rostov V.V. Ocenka vlijanija impul'sno-periodicheskogo rentgenovskogo i mikrovolnovogo izluchenij na biologicheskie struktury s pomoshh'ju izmerenija impedansnyh harakteristik // Vestnik Tomskogo gosudarstvennogo universiteta. – 2008. – №312. – S.180-183
- Schwan H P and Foster K R RF-Field interactions with biological systems: Electrical properties and biophysical mechanisms // Proc. of the IEEE – 1980. – Vol.68. – P.104–113.
- Zorov D.B., Juhaszova M., Sollott S.J. Mitochondrial reactive oxygen species (ROS) and ROS-induced ROS release. // Physiological reviews. 2014. 94(3). P.909-50.
- Gubskij Ju.I. Smert' kletki: svobodnye radikaly, nekroz, apoptoz: monografija / Ju.I.Gubskij. - Vinnica: Nova Kniga, 2015. - 360 s.
- Deleage G., Penin F., Godinot C., Gautheron D.C. Correlations between ATP hidrolisis, generation and utilization of ΔpH in mitochondrial ATPase- ATPsinthase // Biochimica et Biophysica Acta. 1983. – Vol.725. – P.464-471.
- Schunc T., Bieth F., Pinguet S., Delmote Ph Penetration and propagation into biological matter and biological effects of high-power ultra-wideband pulses: a review // Electomagnetic biology and medicine 2016. Vol.35 (1). P.84-101.
