КЛИНИЧЕСКИЙ СЛУЧАЙ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ПАЦИЕНТА С ИНФИЦИРОВАННОЙ АМПУТАЦИОННОЙ КУЛЬТЕЙ СТОПЫ НА ФОНЕ САХАРНОГО ДИАБЕТА И НЕЙРОПАТИЧЕСКОЙ ФОРМЫ СИНДРОМА ДИАБЕТИЧЕСКОЙ СТОПЫ
КЛИНИЧЕСКИЙ СЛУЧАЙ КОМПЛЕКСНОГО ЛЕЧЕНИЯ ПАЦИЕНТА С ИНФИЦИРОВАННОЙ АМПУТАЦИОННОЙ КУЛЬТЕЙ СТОПЫ НА ФОНЕ САХАРНОГО ДИАБЕТА И НЕЙРОПАТИЧЕСКОЙ ФОРМЫ СИНДРОМА ДИАБЕТИЧЕСКОЙ СТОПЫ
Аннотация
В рукописи представлен и проанализирован клинический случай лечения пациента с нейропатической формой синдрома диабетической стопы и местными инфекционными осложнениями после ампутации пальцев стопы в ближайшем анамнезе. Данный синдром является одним из наиболее распространенных осложнений сахарного диабета (до 20% профильных пациентов) и характеризуется высоким риском потери нижней конечности вследствие развития тяжелых инфекций и необходимости выполнения ампутаций по жизненным показаниям. В комплексном лечении данного пациента были последовательно использованы различные местные хирургические подходы, включая ампутацию и реампутацию пальцев стопы, использование спектра раневых повязок, дермотензию, аутодермопластику. Принципиально важным моментом в комплексе мероприятий стал аспект минимизации анестезиологических рисков и послеоперационных осложнений.
1. Введение
Синдром диабетической стопы (СДС) – одно из наиболее распространенных осложнений сахарного диабета (СД), которое развивается в 20% эпизодов у профильных пациентов, при этом порядка 90% случаев СДС отмечаются при СД 2 типа. Серьезной проблемой СДС является высокая вероятность выполнения инвалидизирующих операций, а именно – ампутаций сегментов нижних конечностей по жизненным показаниям , .
У СДС различают три формы клинического течения: нейропатическую, ишемическую и нейроишемическую . При нейропатической форме СДС поражаются дистальные отделы периферических нервов, что приводит к патологическим изменениям сухожильно-мышечного аппарата, костной ткани и кожных покровов стоп и более проксимальных сегментов конечностей . В результате данных трансформаций опорная нагрузка на стопу перераспределяется, увеличиваясь в определенных участках, прежде всего – в проекции головок плюсневых костей. За счет подобной усиленной нагрузки в указанных участках развивается гиперкератоз, формируются контактно-компрессионные язвенные дефекты. Часто язвы инфицируются, вследствие чего пациенты требуют местного хирургического и системного лечения. При длительном существовании таких язв может развиваться контактно-компрессионный остеомиелит костей стопы , .
Лечение пациентов с СД и СДС должно быть комплексным и воздействовать на все звенья патогенеза указанных патологий. При этом лечебные мероприятия должны характеризоваться высокой степенью персонификации, вследствие зависимости особенностей клинической картины заболевания и, следовательно, эффективности лечения, от индивидуальных особенностей организма , . Поэтому каждый клинический случай может представлять не только медицинский, но и научный интерес для профессионального сообщества. В данной рукописи мы представляем клинический случай эффективного комплексного лечения пациента с СД и нейропатической формой СДС после перенесенной в ближайшем анамнезе ампутации пальцев стопы.
2. Описание случая
Пациент Т., 60 лет, последние 20 лет страдает сахарным диабетом 2 типа. Наблюдается у эндокринолога по месту жительства. Требуемый уровень гликемии поддерживается посредством приема таблетированных сахароснижающих препаратов из класса бигуанидов. В октябре 2023 года, после ношения новой обуви, отметил появление сухого некроза кожных покровов на подошвенной поверхности в области дистальной головки III плюсневой кости правой стопы – около 1,5 см в диаметре. Самостоятельно выполнял перевязки с использованием влажно-высыхающих повязок с водными растворами антисептиков («Местамидин») и мазевых лекарственных препаратов («Левомеколь»). Однако положительной динамики на фоне самостоятельного лечения отмечено не было и через 2 недели в обозначенной области появились боли, а сухой некроз дермы трансформировался во влажный и увеличился в размерах до 2,5 см.
При появлении лихорадки, сопровождавшейся подъемом температуры до 38,2°С, пациент вынужден был обратиться в приемное отделение дежурного хирургического стационара. В экстренном порядке 01.11.2023 г. в отделении хирургической инфекции данного стационара пациенту была выполнена ампутация III пальца правой стопы с резекцией дистальной головки III плюсневой кости. Проводилась системная антибиотикотерапия препаратами цефалоспоринового ряда I поколения, инсулинотерапия (с временной отменой сахароснижающих препаратов на фоне подъема уровня гликемии до 10 ммоль/л), метаболическая терапия (витамины группы В и препараты альфа-липоевой кислоты), а также перевязки с мазью левомеколь. В послеоперационном периоде рана не имела тенденции к заживлению и 17.11.2023 г. была выявлена и вскрыта флегмона подошвенной поверхности правой стопы. В дальнейшем, на фоне проводимого лечения, признаки инфицирования и вторичных некрозов отсутствовали, был достигнут уровень гликемии 7-8 ммоль/л и пациент был выписан с улучшением под наблюдение хирурга поликлиники.
В амбулаторных условиях пациент продолжил прием витаминов группы В и альфа-липоевой кислоты в таблетированной форме, а также вернулся к приему сахароснижающих препаратов с отменой инсулинотерапии на фоне стабилизации гликемии. Однако уже в середине декабря 2023 г. было отмечено повторное появление влажных некрозов в дне операционной раны, сопровождаемое гнилостным запахом.
По месту жительства, в амбулаторном порядке, хирургом была выполнена некрэктомия в пределах здоровых тканей – до появления капиллярной кровоточивости из стенок дефекта. С учетом выраженной нейропатии анестезиологическое пособие не использовалось. В дальнейшем рану на стопе вели открытым путем. Выполняли перевязки с мазью левомеколь. В январе 2024 г. пациент вновь отметил появление влажных некрозов в дне и стенках раны и на окружающих края раны кожных покровах. Негативная локальная симптоматика сопровождалось также выраженным болевым синдромом, нарастанием локального отека и гиперемии на правой стопе. При появлении признаков системной воспалительной реакции в виде лихорадки с повышением температуры тела до 38°С, пациент 09.01.2024 г. был госпитализирован в экстренном порядке в отделение хирургической инфекции Клиник ФГБОУ ВО СамГМУ Минздрава России.
При осмотре на правой стопе отсутствует III палец. В проекции головки III плюсневой кости имеется рана размерами 5,0 х 3,0 см, а также рана на подошвенной поверхности каплевидной формы – 7,0 х 2,0 см. Дно ран выполнено влажным некрозом грязно-серого цвета (рис. 1). Из ран интенсивный гнилостный запах. Отмечается умеренный отек правой нижней конечности от пальцев стопы до средней трети голени. Дистальная часть правой стопы гиперемирована, при пальпации болезненна. Пульсация на a. dorsalis pedis и a. tibialis posterior справа удовлетворительная. Чувствительность в правой стопе снижена (2 ст. по классификации PEDIS). Выполнена рентгенография правой стопы в 2 проекциях. На снимках (рис. 2) определятся деструкция II и IV плюснефаланговых суставов, костей II и IV пальцев стопы, краевой остеомиелит опила III плюсневой кости.
Уровень гликемии при мониторинге составил 8-10 ммоль/л. В общем анализе крови отмечался лейкоцитоз до 12 х 109/л. Биохимический профиль – без выхода референсных значений основных показателей за среднефизиологические границы нормы.
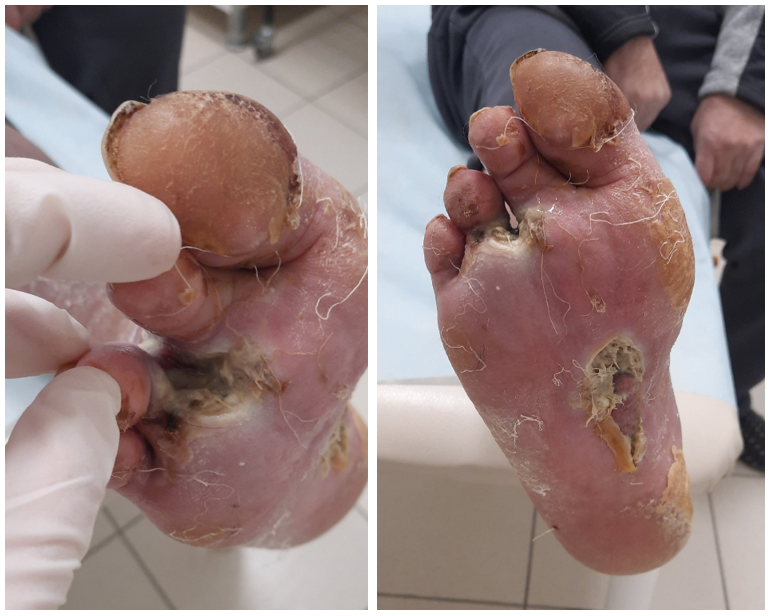
Рисунок 1 - Локальный статус пациента Т., 60 лет, при поступлении в отделение хирургической инфекции Клиник ФГБОУ ВО СамГМУ Минздрава России
Примечание: правая стопа
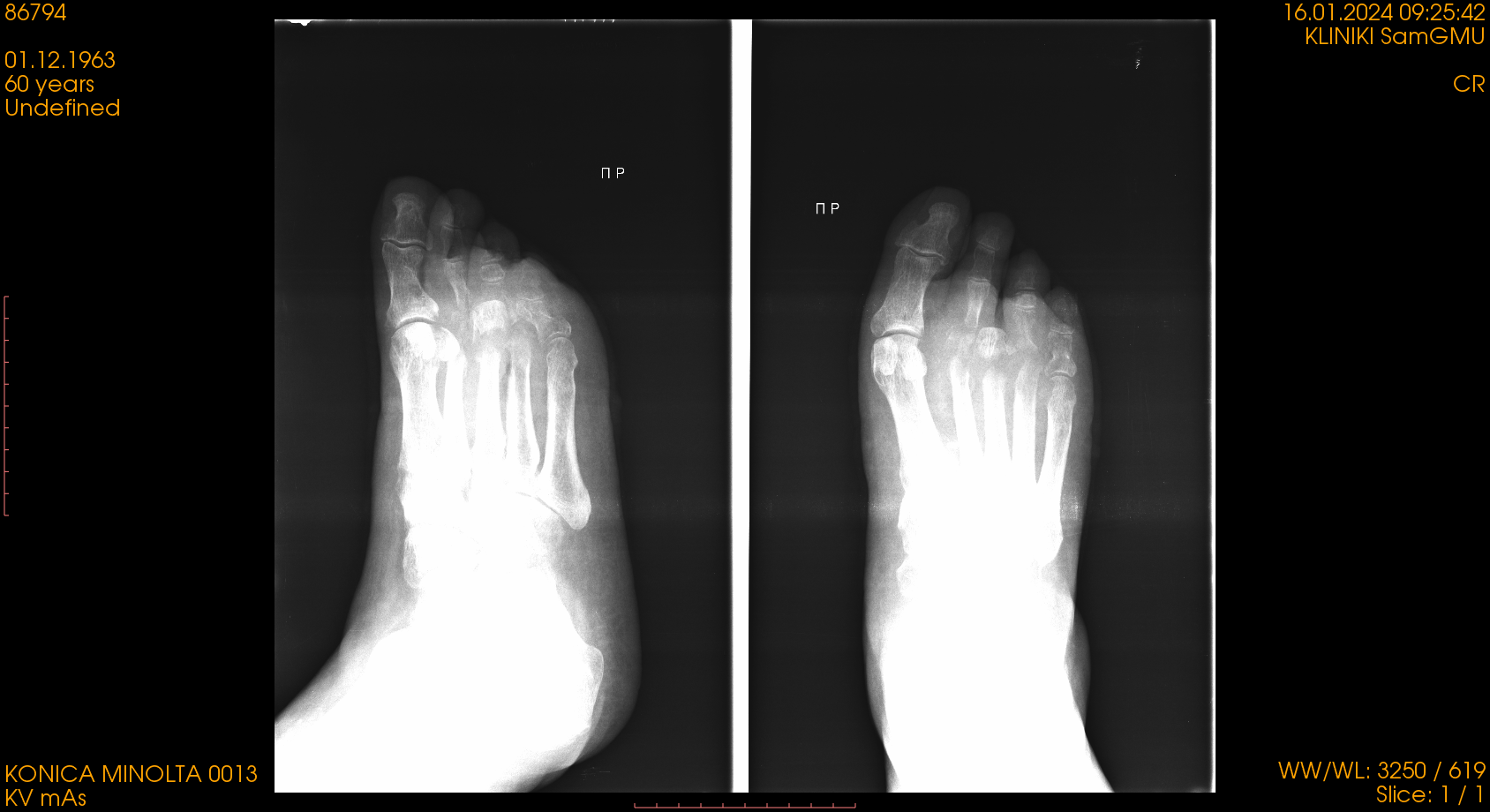
Рисунок 2 - Рентгенография правой стопы пациента Т., 60 лет, при поступлении в отделение хирургической инфекции Клиник ФГБОУ ВО СамГМУ Минздрава России
Иссеченные фрагменты тканей отправлены на гистологическое исследование, по результатам которого получено следующее заключение: кожа и подлежащие ткани ампутированных пальцев с умеренным отеком, расширенными полнокровными сосудами и утолщенными стенками, обширными очагами некрозов, изъязвлений, кровоизлияний, рассеянной и очаговой полиморфноклеточной инфильтрацией, с преобладанием нейтрофильных лейкоцитов; по поверхности фрагментов – наложение клеточно-тканевого детрита с нитями фибрина, распадающимися нейтрофильными лейкоцитами и включениями базофильных колоний микроорганизмов.
Системная терапия включала в себя инсулинотерапию, инфузионную терапию, применение метаболических препаратов (витамины группы В и альфа-липоевой кислоты). Пациенту назначена эмпирическая антибактериальная терапия препаратами цефалоспоринового ряда I поколения. С учетом результатов микробиологического исследования посева раневого содержимого на микрофлору и ее чувствительность к антибиотикам (антибиотикограмма) выполнена смена антимикробного препарата и пациенту назначен ампициллин/сульбактам (табл. 1).
Таблица 1 - Микробиологическое исследование посева раневого содержимого на микрофлору и ее чувствительность к антибиотикам
Биоматериал | Раневое отделяемое | ||||
Диагноз | Флегмона | ||||
№ | Выделенные микроорганизмы | КОЕ/мл | |||
1 | Enteroccocus faecalis | 103 | |||
2 | Corinebactium striatum | 104 | |||
Антибиотикограмма | 1 | 2 | 3 | 4 | |
Β-лактамы (полусинтетические пенициллины, цефалоспорины) | |||||
Ампициллин | S | S |
|
| |
Оксациллин | - | - |
|
| |
Цефазолин | - | - |
|
| |
Цефотаксим | - | - |
|
| |
Цефтазидим | - | - |
|
| |
Цефтриаксон | - | - |
|
| |
Цефепим | - | - |
|
| |
Ингибиторзащищенные Β-лактамы | |||||
Амоксициллин/клавуланат | S | - |
|
| |
Цефоперазон/сульбактам | - | - |
|
| |
Пиперациллин/тазобактам | - | - |
|
| |
Β-лактамы (карбапенемы) | |||||
Имипенем | S | - |
|
| |
Меропенем | - | - |
|
| |
Эртапенем | - | - |
|
| |
Аминогликлозиды | |||||
Гентамицин | - | - |
|
| |
Амикацин | - | - |
|
| |
Фторхинолоны | |||||
Левофлоксацин | - | - |
|
| |
Ципрофлоксацин | S | R |
|
| |
Макролиды | |||||
Эритромицин | - | - |
|
| |
Аитромицин | - | - |
|
| |
Кларитромицин | - | - |
|
| |
Другие группы антибактериальных препаратов | |||||
Ванкомицин | S | S |
|
| |
Тигециклин | - | S |
|
| |
Линезолид | - | S |
|
| |
Даптомицин | - | - |
|
| |
Бисептол | - | - |
|
| |
Примечание: антибиотикограмма
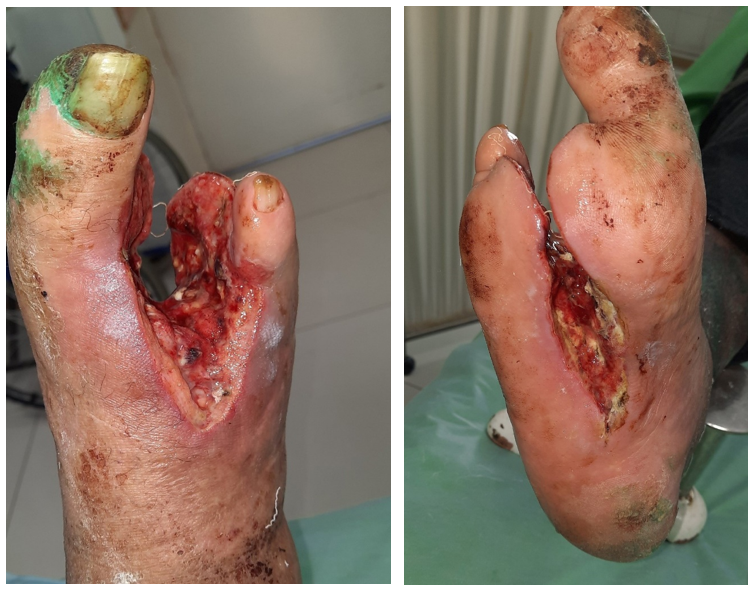
Рисунок 3 - Локальный статус пациента Т., 60 лет, на вторые сутки после оперативного лечения
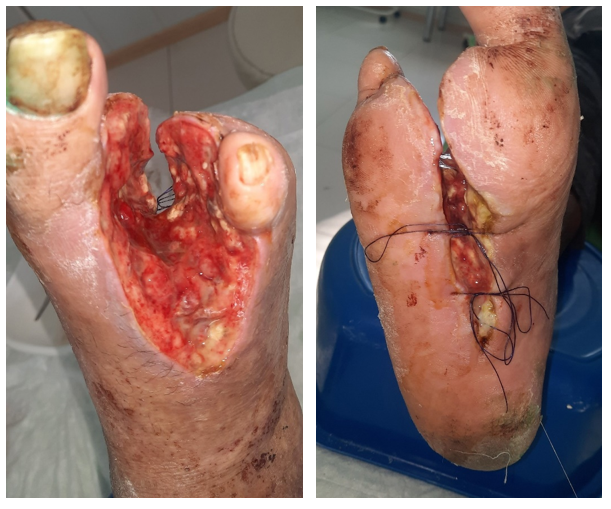
Рисунок 4 - Рана правой стопы с наводящими швами в целях управляемой дермотензии
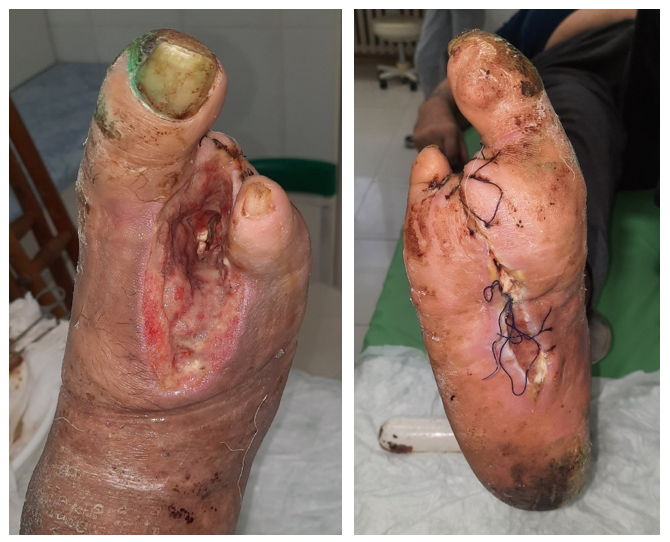
Рисунок 5 - Локальный статус на седьмые сутки после наложения наводящих швов
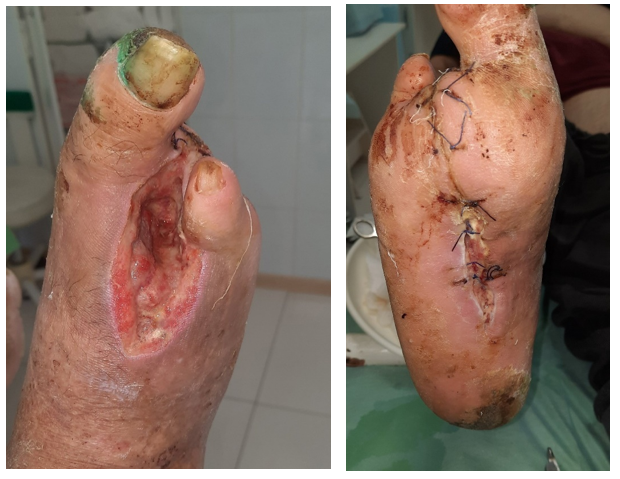
Рисунок 6 - Локальный статус на десятые сутки после наложения наводящих швов
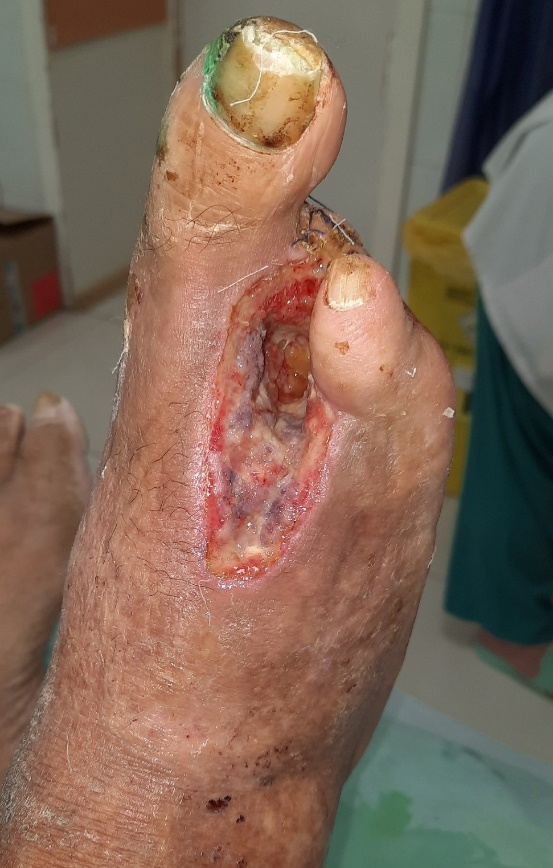
Рисунок 7 - Четвертые сутки после аутодермопластики
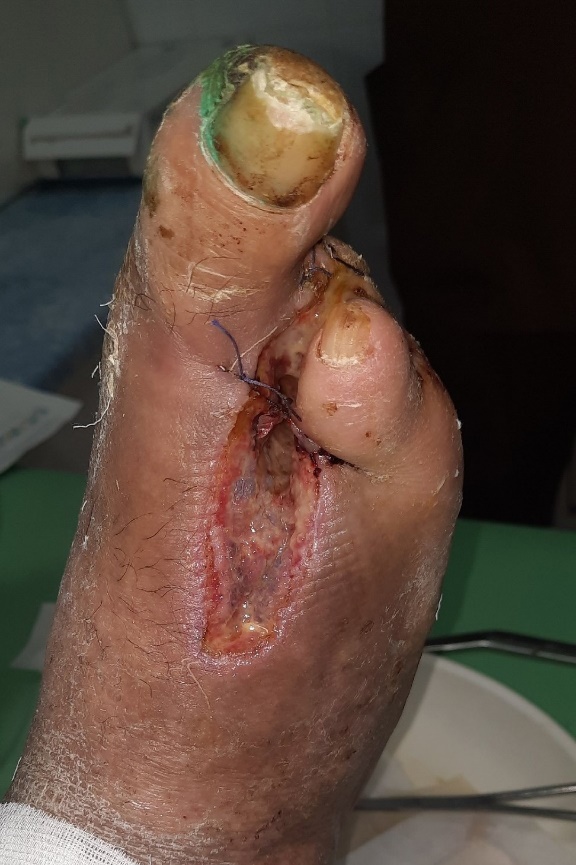
Рисунок 8 - Шестые сутки после аутодермопластики
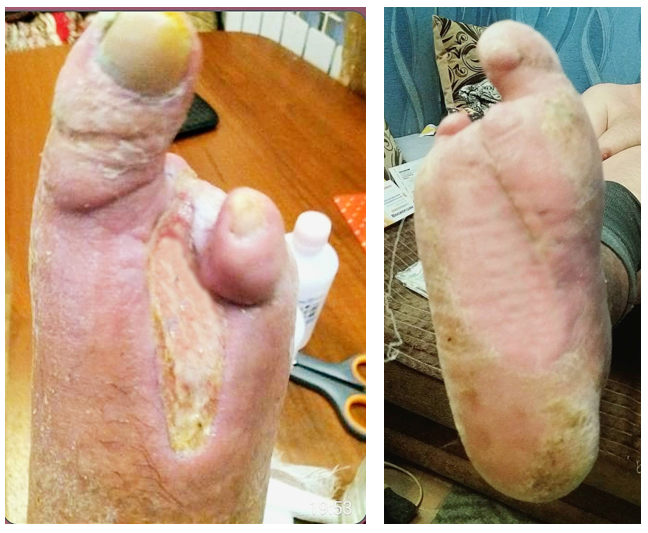
Рисунок 9 - Локальный статус при контрольном осмотре
3. Дискуссия
В рамках обсуждения приведенного в рукописи клинического случая, считаем необходимым обратить внимание на следующие важные моменты. Как отмечено в действующих клинических рекомендациях и профильной медицинской литературе, лечение пациентов с СД и СДС должно быть комплексным и воздействовать на все звенья патогенеза указанных патологий. Эти принципы должны соблюдаться как на стационарном, так и на амбулаторном этапах лечения. Не менее значимым элементом лечебных мероприятий должна являться реабилитация профильных пациентов , .
В то же время можно отметить, что при первичном экстренном обращении пациента в стационар и дальнейшем амбулаторном наблюдении отсутствовал целый ряд необходимых диагностических и лечебных мероприятий. В частности, не проводилась неинвазивная визуализационная диагностика состояния кровообращения в нижних конечностях, например, дуплексное сканирование с цветовым доплеровским картированием. Таким образом, определение уровня возможного нарушения (блока) артериальных сосудов и, соответственно, выбор ампутируемого сегмента, осуществлялись на основе исключительно физикальных данных. Как следствие – потенциально некорректный выбор уровня ампутации и объема некроэктомии. Кроме того, не была проведена корректировка сахароснижающей терапии и пациент продолжал получать таблетированные гипогликемические препараты на фоне активного гнойно-некротического процесса. Указанное обстоятельство может не только затянуть сроки купирования локального воспаления, но и способствовать его распространению проксимально (здесь можно отметить и отсутствие разгрузки стопы после вмешательств), неся в себе риск развития жизнеугрожающих осложнений, таких как сепсис. А при выписке пациенту не были даны рекомендации о наблюдении у специалиста кабинета диабетической стопы. К сожалению, невыполнение перечисленных мер может стоить пациенту потери конечности и даже жизни. В связи с этим считаем, что лечение пациентов с гнойно-хирургическими осложнениями СД должно осуществляться в условиях профильного специализированного отделения. При этом пациент должен ежедневно осматриваться заведующим отделением и находится на контроле службы экспертизы качества медицинской помощи лечебного учреждения.
С хирургической точки зрения представленный клинический случай интересен тем, что управляемая дермотензия в лечении пациентов с СД и СДС продолжает оставаться одним из эффективных методов местного ведения раны. Данный подход обеспечивает минимизацию рисков анестезии и последующего послеоперационного периода по сравнению с вариантом проведения полноценного реконструктивного вмешательства. Тем более на фоне высокого риска развития негативных исходов после реконструкций в дистальных отделах нижних конечностей у профильных больных , . Стоит также отметить, что метод дермотензии психологически воспринимается пациентами более благосклонно по сравнению с повторным оперативным лечением .
Развивая тематику хирургического подхода в лечении пациентов с СД и СДС необходимо отметить, что данное направление активно развивается и дополняется новыми современными методиками. При своевременном и корректном их применении можно избежать ампутации, как калечащей операции, или же попытаться минимизировать ее объем. Речь идет о восстановления магистрального кровотока нижних конечностей с использованием миниинвазивной и атравматичной рентгенэндоваскулярной хирургии. Пациентам с признаками критической ишемии тканей стопы проводят ангиографию с последующей баллонной ангиопластикой и стентированием артерий пораженной конечности .
Одним из новых методов лечения раневых дефектов у профильных пациентов, эффективно дополняющих хирургический подход, является вакуум-терапия (местное применение отрицательного давления). Для стимуляции оттока раневого отделяемого, скорейшего формирования грануляционной ткани, уменьшения инфекционного воспаления и ускорения заживления используют специальные коммерческие аппараты, создающие и поддерживающие отрицательное давление в раневой полости. Подобный аппаратный подход получил название Vacuum-Assisted Closure (VAC). В настоящее время VAC-терапия является широко и активно применяемым методом в комплексной терапии пациентов в СД и СДС .
После проведения ампутаций, даже малых, пациенты с СД и СДС нуждаются в полноценной реабилитации. Передвижение и ходьба даже без пальца стопы или с протезом (имплантатом) требует определенной подготовки пациента. Наряду с классической физиотерапией, которая помогает справиться с локальным болевым синдромом (в том числе фантомными болями) и отеком культи, важнейшее значение приобретает кинезиотерапия, которая помогает восстановить навыки движения и акта ходьбы. Упражнения для ног улучшают эластичность мышц, качество баланса и координации движений, а также увеличивают подвижность суставов. Ходьба же способствует развитию мускулатуры и улучшает моторную функцию конечности. В современных условиях с профильными пациентами до и после ампутаций работает специалист психолог, который работает над формированием адекватного отношения к потере конечности или ее сегмента и восстановлением психического здоровья .
Амбулаторное наблюдение за пациентами с СД и СДС после ампутаций включает в себя периодические приемы у эндокринологов и специалистов кабинетов или центров «Диабетическая стопа». Профилактика развития локальных трофических и некротических поражений заключается в обучении пациентов правилам подбора обуви и ухода за ногами. Проведение лечебных и профилактических мероприятий по приведенному плану достоверно позволяет снизить риск повторных ампутаций конечности у профильных пациентов .
4. Заключение
Представленный клинический случай и его разбор позволяют сформулировать следующие выводы для профильных и смежных специалистов:
- лечение пациентов с СД и СДС является сложной и серьезной задачей, требующей условий специализированного профильного отделения и контроля со стороны клинико-экспертной службы лечебного учреждения;
- лечение пациентов с СД и СДС должно основываться на действующих клинических рекомендациях и воздействовать на все звенья патогенеза заболеваний, а также учитывать индивидуальные особенности пациента;
- включение в комплекс лечебных мероприятий управляемой дермотензии является методом выбора при закрытии ран в послеоперационном периоде у пациентов в нейропатической формой СДС и СД.
