МОРФОЛОГИЧЕСКИЕ ОСОБЕННОСТИ ЛЕГКИХ ПРИ ЭКСПЕРИМЕНТАЛЬНОМ САХАРНОМ ДИАБЕТЕ
МОРФОЛОГИЧЕСКИЕ ОСОБЕННОСТИ ЛЕГКИХ ПРИ ЭКСПЕРИМЕНТАЛЬНОМ САХАРНОМ ДИАБЕТЕ
Аннотация
Исследования дыхательной системы при сахарном диабете (СД), описанные в литературе, касаются развернутой его клинической картины, но известно, что между ранними нарушениями углеводного обмена и постановкой больному диагноза проходят годы и даже десятилетия. Оценить наиболее ранние изменения при СД представляется возможным только в экспериментальных исследованиях. Цель работы – изучить динамику патоморфологических изменений легких крыс при экспериментальном СД. Моделирование СД осуществляли с помощью однократного введения аллоксана моногидрата подкожно в дозе 135 мг/кг. Забор материала осуществляли на 3-й, 7-й, 14-й и 30-й день после введения аллоксана. Полученные результаты свидетельствуют, что дефицит инсулина приводит к появлению в легочной ткани многочисленных очагов ателектазов, сочетающихся с участками эмфиземы и изменений сосудистого русла при сохранении общего строения ткани. Обширные зоны инфильтрации обнаруживаются в перибронхиальной соединительной ткани и стенках альвеол. Таким образом, уже на раннем этапе развития СД появляются существенные морфологические изменения легочной ткани, что усиливает гипоксию при дефиците инсулина.
1. Введение
Сахарный диабет (СД) – заболевание, основным патогенетическим фактором которого является недостаточность инсулина. Дефицит инсулина может быть вызван как непосредственным повреждением поджелудочной железы, так и развитием инсулинорезистентности . В современной классификации сахарного диабета выделяют эти два типа, а также ряд других, например, связанный с генетическими нарушениями, гестационный и пр. Количество больных сахарным диабетом в нашей стране и в мире постоянно увеличивается. На 1 января 2024 года в Российской Федерации зарегистрировано более 5 млн пациентов с СД, а новых случаев за год более 215 тыс. Однако в реальности количество больных намного больше, что связано с поздней диагностикой заболевания . При СД происходит нарушение всех видов обмена веществ и энергии. В результате страдают все органы и системы организма . Наиболее чувствительными являются так называемые «органы-мишени» сахарного диабета – нервная система, сердечно-сосудистая система, почки, сетчатка . Однако часто больные с СД предъявляют жалобы на респираторные симптомы, и риск возникновения заболеваний дыхательной системы у них выше, чем в общей популяции . Исследования дыхательной системы, описанные в литературе, касаются развернутой клинической картины СД, но известно, что между ранними нарушениями углеводного обмена и постановкой больному диагноза «сахарный диабет» проходят годы и даже десятилетия. Также мало учитывается динамика изменений легочной ткани при прогрессировании СД. Оценить наиболее ранние изменения при СД представляется возможным только в экспериментальных исследованиях, когда известно время воздействия инициирующего фактора, повреждающего инсулярный аппарат поджелудочной железы.
Цель исследования – изучить динамику патоморфологических изменений легких крыс при экспериментальном сахарном диабете.
2. Методы и принципы исследования
Исследование проводилось на 50 белых беспородных крысах-самцах, находящихся в стандартных условиях вивария, в соответствии с Европейской конвенцией о защите позвоночных животных. Имеется разрешение локального Этического комитета на его проведение. Экспериментальное моделирование сахарного диабета осуществляли с помощью однократного введения аллоксана моногидрата (производитель – фирма ДиаМ) подкожно в дозе 135 мг/кг . Эта модель является второй по частоте использования после стрептозоциновой модели. Механизм действия аллоксана связан с селективным повреждением бета-клеток островков Лангерганса и развитием инсулинзависимого сахарного диабета. Для оценки динамики изменений в легких забор материала осуществляли на 3-й, 7-й, 14-й и 30-й день после введения аллоксана. На каждом из сроков наблюдения использовали группу по 10 животных, всего 40 с моделью сахарного диабета и 10 контрольных. Эвтаназия осуществлялась под золетиловым наркозом путем декапитации. Легкие забирали целиком и помещали в 10% забуференный формалин для первичной фиксации. После вторичной фиксации осуществляли обезвоживание 99% изопропиловым спиртом. Фрагменты легких заливали в парафин и на санном микротоме «Microtom» изготавливали срезы толщиной 5 – 6 мкм. Срезы окрашивали гематоксилином и эозином. Фотографирование микропрепаратов проводили на микроскопе «Micros» МС-200 с цифровой окулярной камерой DCM 900. При оценке легких исследовалось состояние бронхиального дерева, альвеол, а также сосудистого русла.
Концентрация глюкозы в плазме крови определяли глюкозооксидазным методом, используя набор ООО «Ольвекс диагностикум» (Россия) для количественного определения содержания глюкозы в сыворотке или плазме крови человека энзиматическим колориметрическим методом без депротеинизации. Статистическая обработка результатов измерения глюкозы в крови проводилась в программе Statistica 13, использовали непараметрический критерий Манна-Уитни. Статистически значимыми считали различия при р<0,05.
3. Основные результаты и обсуждение
Введение аллоксана в описанной дозировке приводило к гибели около 30% животных в первую неделю эксперимента. Концентрация глюкозы достоверно (р<0,05) увеличивалась во все сроки исследования и составляла на 3-й день после введения аллоксана 72,0 мМ, на 7-й – 21,7 мМ, на 14-й – 18,8 мМ, на 30-й – 14,8 мМ при 9,4 мМ у крыс контрольной группы.
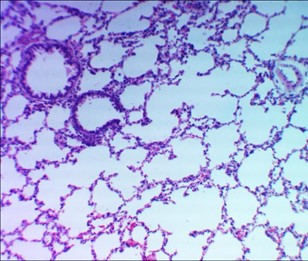
Рисунок 1 - Контрольная группа
Примечание: альвеолы легких расправлены, просвет бронхиол свободен, кровенаполнение капилляров стромы равномерное; окраска гематоксилином и эозином; увеличение х120
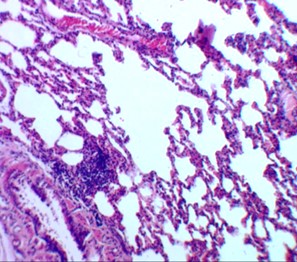
Рисунок 2 - 3-и сутки после введения аллоксана
Примечание: в легких венозное полнокровие, очаговая эмфизема, лейкоцитарная инфильтрация межальвеолярных перегородок; окраска гематоксилином и эозином; увеличение х120
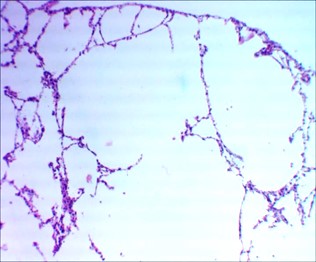
Рисунок 3 - 7-е сутки после введения аллоксана
Примечание: в легких очаговая эмфизема; окраска гематоксилином и эозином; увеличение х 120
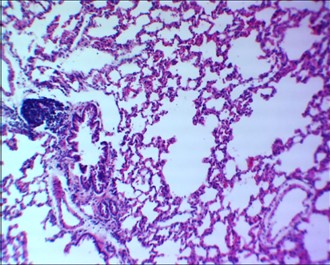
Рисунок 4 - 7-е сутки после введения аллоксана
Примечание: бронхоспазм, лейкоцитарная инфильтрация стромы легкого; увеличение х120
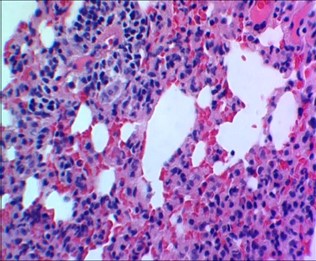
Рисунок 5 - 14-е сутки после введения аллоксана
Примечание: в легких венозное полнокровие, очаговые кровоизлияния, чередование очагов ателектазов и эмфиземы, лейкоцитарная инфильтрация; окраска гематоксилином и эозином; увеличение: х480
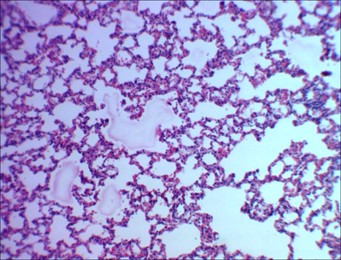
Рисунок 6 - 14-е сутки после введения аллоксана
Примечание: венозное полнокровие, очаговая эмфизема, интраальвеолярный отек стромы легкого; окраска гематоксилином и эозином; увеличение х120
Гипергликемия в течение 1 месяца вызывает еще более выраженные изменения структуры бронхов, альвеолярной ткани и сосудистого русла. Бронхиальное дерево частично в спавшемся состоянии, в просвете отмечается повышенное скопление слизи. Имеются признаки лейкоцитарной инфильтрации стенок бронхов. В респираторном отделе альвеолы частично в спавшемся состоянии, их стенки утолщены, что сочетается с эмфизематозно расширенными альвеолами. Кровообращение существенно изменено. Отмечается выраженная гиперемия, множество очагов кровоизлияний.
4. Заключение
Экспериментально вызванная хроническая гипергликемия приводит к появлению в легочной ткани многочисленных очагов ателектазов, сочетающихся с участками эмфиземы и изменений сосудистого русла при сохранении общего строения ткани. Обширные зоны инфильтрации обнаруживаются в перибронхиальной соединительной ткани и стенках альвеол. Полученные результаты свидетельствуют об еще одной важной мишени влияния хронической гипергликемии – легочной ткани, что усиливает гипоксические нарушения в организме при сахарном диабете.
