ПРИМЕНЕНИЕ ПЦР ДЛЯ ГЕНОТИПИРОВАНИЯ БАКТЕРИИ PASTEURELLA MULTOCIDA, ВЫДЕЛЕННОЙ ОТ КРУПНОГО РОГАТОГО СКОТА
Нефедченко А.В.1, Глотов А.Г.2, Глотова Т.И.3, Тереньева Т.Е.4, Шиков А.Н.5, Семенова О.В.6, Войтова К.В.7, Никонова А.А.8
1Кандидат ветеринарных наук, доцент; 2доктор ветеринарных наук, профессор, 3доктор биологических наук, профессор; 4аспирант, ГНУ Институт экспериментальной ветеринарии Сибири и Дальнего Востока Россельхозакадемии; 5кандидат биологических наук, ФБУН государственный научный центр вирусологии и биотехнологии «Вектор»; 6кандидат биологических наук; 7кандидат ветеринарных наук, ГНУ Институт экспериментальной ветеринарии Сибири и Дальнего Востока Россельхозакадемии; 8студент, Новосибирский государственный аграрный университет
ПРИМЕНЕНИЕ ПЦР ДЛЯ ГЕНОТИПИРОВАНИЯ БАКТЕРИИ PASTEURELLA MULTOCIDA, ВЫДЕЛЕННОЙ ОТ КРУПНОГО РОГАТОГО СКОТА
Аннотация
С помощью разработанной ПЦР изучена частота выявления серогрупп А и D бактерии Pasteurella multocida из легких телят, больных респираторными заболеваниями. Результаты могут быть использованы при планировании противоэпизоотических мероприятий в хозяйствах по производству молока, а также в научных целях при изучении молекулярной эпизоотологии болезней крупного рогатого скота, вызванных бактериями семейства Pasteurellaceae.
Ключевые слова: Pasteurella multocida, крупный рогатый скот, серогруппа, генотипы, ПЦР.
Nefedchenko A.V.1, Glotov A.G.2, Glotovа T.I.3, Terentjeva T.E.4, Shikov A.N.5, Semenova O.V.6, Voitova K.V.7, Nikonovа A.A.8
1PhD in veterinary, associate professor, 2Doktor of veterinary sciences , professor, 3Doktor of Biological Sciences, 4Postgraduate student , Institute of Experimental veterinary of Siberia and the Far East Agricultural Sciences ; 5 PhD in biological, State Research Center of Virology and Biotechnology "Vector"; 6PhD in bialogical, 7PhD in veterinary, Institute of Experimental Veterinary Siberia and the Far East Agricultural Sciences; 8student, Novosibirsk State Agrarian University
APPLICATION PCR FOR GENOTYPING OF BACTERIA PASTEURELLA MULTOCIDA ISOLATED FROM CATTLE
Abstract
With the help of the developed PCR incidence of serogroups A and D Pasteurella multocida bacteria from the lungs of calves suffering from respiratory diseases was studied. The results can be used in the planning of control measures in the dairy farms, as well as for investigation in molecular epizootology of disease caused by bacteria of the Pasteurellaceae family.
Keywords: Pasteurella multocida, cattle, serogroups, genotyping, PCR.
Pasteurella multocida это неподвижная, факультативно анаэробная, граммотрицательная палочкообразная бактерия, являющаяся комменсальным обитателем поверхности слизистых оболочек верхних дыхательных путей, обладающая способностью вызывать вторичные инфекции и болезни у домашних и диких животных и птиц [6].
На основании различий по капсульному антигену все штаммы Pasteurella multocida делятся на 5 серогрупп (А, В, D, E, F), а по соматическому антигену на 16 серотипов.
Штаммы серогрупп А и D наиболее часто выделяются из легких крупного рогатого скота при пневмониях. Во всем мире превалирующей серогруппой бактерии является А, выделение которой от телят в разных странах колеблется от 60 до 92 %. Выделение культур сероварианта D происходит реже, до 25% [2].
Штаммы бактерий серогрупп В и Е вызывают геморрагическую септицемию крупного рогатого скота, характеризующуюся острой септицемией с высокой летальностью. Болезнь распространена в Азии, Африке и на ближнем Востоке. В Азии основным ее этиологическим агентом считается серотип В2, в Африке – Е2. Есть сообщения о выделении культур бактерии серотипа В от диких и домашних жвачных в Европе, Северной и Южной Америке и на территории бывшего СССР [3, 13]. Штаммы серогруппы F изолированы от птиц. Есть несколько сообщений о выделении их случаях инфекционного перитонита телят, пневмониях овец [8, 14, 16].
Традиционно типизация пастерелл осуществляется при помощи серологических реакций на основании различий по капсульному или соматическому антигену [13]. В нашей стране серологическое типирование не разработано, а применяемые методы, основанные на определении выработки гиалуроновой кислоты штаммами серогруппы А или аглютинации в растворе акрифлавина штаммов серогруппы D, не точны и дают значительное количество ошибок [5].
Полимеразная цепная реакция, в настоящее время, является важным диагностическим инструментом в бактериологии, повышает точность видовой идентификации бактерий, сокращает сроки их выявления, дает возможность обнаруживать и типировать возбудителя непосредственно в исследуемом материале без выделения чистой культуры [10].
Цель настоящей работы заключалась в изучении частоты выявления и генотипировании бактерий Pasteurella multocida, выделенных от больных животных, при помощи ПЦР по капсульному гену.
Материалы и методы
Штаммы и изоляты бактерий
Работа выполнена в 2012 – 2013 гг. Использовали референтные штаммы P. multocida «1231» (серогруппа А), «681» (серогруппа В) и штамм «Т80» (серогруппа D), полученые из коллекции культур микроорганизмов ВИЭВ им. Я.Р. Коваленко (Москва), 96 проб биоматериала, отобранного от телят с респираторными заболеваниями в возрасте от 1 до 6 месяцев.
Изоляцию бактерий из проб биоматериала проводили на мясопептонном агаре с добавлением 5 % крови барана. Культуры выращивали течение 24 часов при 370С в атмосфере 5% СО2.
Для определения патогенности и очистки выделенных культур бактерий использовали беспородных белых мышей массой 18-20 грамм. Бактериальную культуру вводили мышам внутрибрюшинно в дозе 0,2 мл. Наблюдение вели в течение 7 дней. Культуры реизолировали из крови и селезенки на кровяном агаре.
В ПЦР исследовали суспензии внутренних органов больных телят, культур бактерий, выделенных на искусственных питательных средах, а также культур, реизолированных из внутренних органов белых мышей.
Для выделения ДНК использовали коммерческий набор «Рибо-преп» (Интерлабсервис, Россия). Для выявления и типирования Р. multocida использовали праймеры, разработанные нами [1]. ПЦР проводили в два этапа. На первом этапе использовали видоспецифичные праймеры с целью определения принадлежности выделенных культур к виду Pasteurella multocida (размер фрагмента 211 п.н.), а также группоспецифичные праймеры для генотипирования серогрупп А (564 п.н.) и D (355 п.н.). На втором этапе проводили генотипирование капсульных серогрупп бактерии В (размер фрагмента 167 п.н.), Е (357п.н.) и F (257 п.н.).
ПЦР проводили в реакционной смеси объемом 30 мкл следующего состава: 5 мкл ДНК; 1хTaq буфер без Mg2+ (ООО «Лаборатория Медиген», Россия), 3,3 mM MgCl2, 0,4 mM dNTP, 0,15 µM каждого праймера, 1,5 е.а. SmartTaq ДНК-полимераза, вода– до 30 мкл. Поверх пробы наносили минеральное масло.
Амплификацию проводили в приборах «Терцик» (ДНК-технология, Россия) при следующем режиме: 1 цикл 95 0С - 5 минут; 45 циклов 95 0С - 20 сек, 57 0С - 30 секунд, 72 0С - 40 секунд; 1 цикл 72 0С - 7 минут.
Амплифицированные ДНК-фрагменты разделяли в 2 % агарозном геле с бромистым этидием. Для визуализации ДНК-фрагментов использовали фотодокументирующую систему Molecular Imager ChemiDoc XRS System 170-8170 (Bio-Rad, США).
Результаты и обсуждения
P. multocida является комменсальным обитателем слизистых оболочек верхних дыхательных путей. Их можно выделить у 10-60 % здоровых животных из носовых секретов и носоглотки [4, 9, 12]. Как правило, культуры бактерии, выделенные со слизистых оболочек животных, являются невирулентными, в то время как из паренхиматозных органов чаще выделяются вирулентные культуры [11]. Поэтому выявление возбудителя в легких, бронхиальных лимфоузлах и селезенке свидетельствует об их патогенности и участии в этиологии заболеваний, что, вероятно, связано с наличием и функционированием гена капсулы.
Нами проведено исследование 96 проб легких, бронхиальных лимфоузлов и селезенки от 32 телят в возрасте от 1 до 6 месяцев с клиническими признаками бронхопневмонии из 14 хозяйств Западной Сибири. Пробы отбирали не позднее 3-5 часов после гибели или вынужденного убоя животных, не подвергавшихся лечению антибиотиками (Рис., таблица 1).
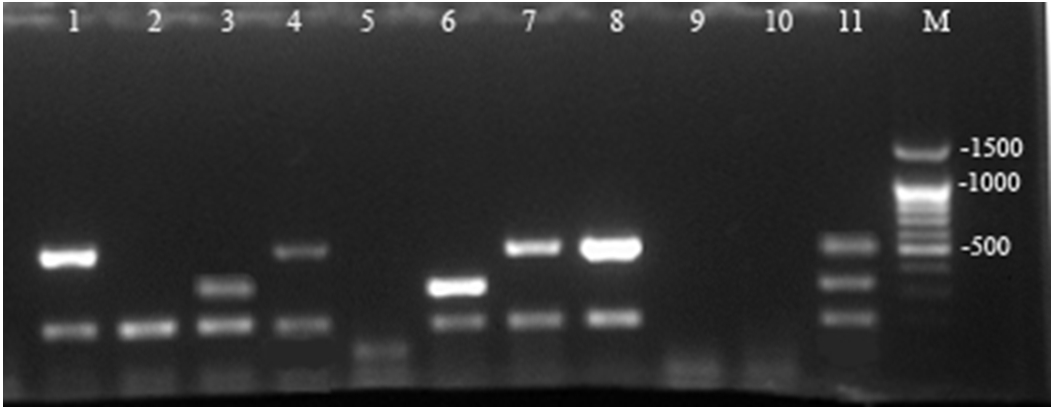
Рис. 1 - Электрофореграмма продуктов амплификации референтных штаммов и суспензии проб внутренних органов телят
Обозначения: 1- P. multocida штамм 1231 (серогруппа А), 2 - P. multocida штамм 681 (серогруппа В), 3 - P. multocida штамм Т80 (серогруппа D), 4 – 10 - пробы внутренних органов телят, 11 – смесь положительных контрольных образцов, М – маркер молекулярного веса 100 вр.
Таблица 1 - Результаты исследования проб внутренних органов от животных методом ПЦР
| № п/п | Пробы | Исследовано | Выявлено положительных в ПЦР / % от исследованных |
| 1 | Легкие | 32 | 15 /46,8 |
| 2 | Бронхиальные лимфоузлы | 32 | 6 /18,7 |
| 3 | Селезенка | 32 | 6 / 18,7 |
| Всего | 96 | 27 / 28,1 |
Результаты исследований показали, что геном P. multocida присутствовал в 28,1% от общего количества исследованных проб органов. Его также выявили в 46,8% проб легких,18,7% проб бронхиальных лимфоузлов и селезенки. На питательных средах из проб легких выделили и типировали в ПЦР 18 изолятов, 14 из которых были реизолированы из внутренних органов белых мышей и повторно типированы в ПЦР.
Наши результаты в общем виде согласуются с данными О. Angen с соавт. (2009), исследовавших бронхоальвеолярные смывы от телят с респираторной патологией. P. multocida чаще удавалось выделить на питательных средах, чем выявить в образце методом ПЦР, что, вероятно, связано с низкой концентрацией бактерий в образце, не полной очисткой ДНК от ингибиторов ПЦР, а возможно и присутствием авирулентных бактерий.
Для проведения капсульного типирования пастерелл серологическими или бактериологическими методами, обязательным этапом является получение чистой культуры. Одним из методов очистки культур бактерии основан на реизоляции ее из органов зараженных белых мышей. При этом происходит избирательное накопление патогенных вариантов всех серогрупп, приводящее к гибели зараженных животных в течение 24 – 48 часов. Этот метод позволяет также очищать P. multocida в смешанных культурах и органах животных-бактерионосителей при низкой концентрации бактерий, когда другие методы не эффективны [13]. Однако по этическим и экономическим вопросам, использование белых мышей для очистки изолятов должно быть сведено к минимуму.
Поэтому в дальнейшем мы определяли эффективность капсульного генотипирования P. multocida методом ПЦР на всех этапах бактериологической диагностики. Результаты, представленные в табл. 2, свидетельствуют о том, что с помощью разработанной нами ПЦР возможно проводить генотипирование бактерии на всех этапах бактериологической диагностики: в суспензии внутренних органов животных, культурах, выделенных на искусственных питательных средах и реизолированных из внутренних органов лабораторных мышей.
Таблица 2 - Генотипирование P. multocida методом ПЦР по наличию капсульного гена
| Пробы | Количество типированных проб | Генотипы, всего/% | ||
| А | D | А + D | ||
| Легкие телят | 15 | 9 /60,0 | 6/40,0 | 0 |
| Культуры P. multocida, выделенные из легких | 18 | 10/55,6 | 7/38,9 | 1/5,6 |
| Культуры бактерии, реизолированные от мышей | 14 | 6 / 42,9 | 7/50,0 | 1/7,1 |
| Всего | 47 | 25/53,2 | 20/42,6 | 2/4,2 |
В большинстве исследованных проб легких и бактериальных культур (60 и 55,6% соответственно) были выявлены и генотипированы бактерии серогруппы А. В одном случае генотипировали культуру, содержащие геномы двух серогрупп. Четыре изолята серогруппы А были непатогенными для белых мышей. В данной работе нам не удалось выявить P. multocida серогрупп В, Е и F.
Таким образом, разработанная нами ПЦР может быть использована для быстрого выявления и генотипирования P. multocida непосредственно в пробах биоматериала от животных, а также на всех этапах бактериологической диагностики. Для диагностики заболевания необходимо одновременно исследовать в ПЦР пробы органов и культуры бактерии, выделенные из этих органов на искусственных питательных средах. При необходимости определения патогенности выделенных культур проводить заражение белых мышей и исследовать реизоляты бактерий от них. Преобладающим генотипом, циркулирующим среди крупного рогатого скота в Сибири, является генотип А. Наличие циркуляции двух генотипов (А и D) среди животных на молочных комплексах необходимо учитывать при разработке противоэпизоотических мероприятий.
Заключение
Определение генотипа возбудителя имеет большое значение при разработке противоэпизоотических мероприятий при пастереллезе крупного рогатого скота и, особенно, при разработке программ вакцинации. Представленные на сегодняшний день на рынке вакцины содержат, в основном, только один вид и один серотип бактерии и не вызывают развитие перекрестного иммунитета с другими серотипами [15]. Лабораторная диагностика, основанная на выделении бактерий, получении чистых культур, изучении их культурально-морфологических и биохимических свойств и постановке биопробы на мышах, без генотипирования, не дает точной информации о генотипе возбудителя, а следовательно, не позволяет выбрать вакцину.
Разработанная нами ПЦР может быть использована в ветеринарных лабораториях как простой, доступный и легко воспроизводимый аналог серологического типирования, позволяющий выявлять и генотипировать P. multocida на всех этапах бактериологической диагностики и, следовательно, сократить время на постановку диагноза и разработку программы вакцинации. Кроме того, разработанную ПЦР можно использовать при исследованиях по молекулярной эпизоотологии болезней, вызванных бактериями сем. Pasteurellaceae, для изучения филогеографического распространения различных генотипов бактерий.
Поддержка
Работа частично выполнена в рамках соглашения № 8792 между Министерством образования и науки РФ, Россельхозакадемией и ГНУ ИЭВСиДВ Россельхозакадемии о предоставлении гранта в форме субсидии.
Список литературы
Глотов А.Г. Типирование культур бактерии Pasteurella multocida, выделенных от крупного рогатого скота при помощи ПЦР / А.Г. Глотов, Т.И. Глотова, А.В. Нефедченко, Т.Е. Терентьева// Сибирский вестник сельскохозяйственной науки. - 2013. - №2. - С. 88-93.
Стрельченя И.И. Изучение определяющей роли серовариантов Pasteurella multocida, выделенных от телят в инфекционной патологии / И.И. Стрельченя // Эпизоотология, иммунология, фармакология и санитария: международный научно – теоретический журнал. - 2006. - №2. - С. 32 – 34.
Шегидевич Э.А. Роль пастерелл в респираторной патологии овец и крупного рогатого скота: дисс…докт. ветеринар. наук. – М., 1993. – 42 с.
Шибаев М.А. Разработка и применение методов молекулярной биологии для выявления возбудителей бактериальных респираторных инфекций крупного рогатого скота: дисс…канд. ветеринар. наук.- Владимир. - 2010.-16 с.
Методические указания по лабораторной диагностике пастереллезов животных и птиц. – М.: Главветуправ. – 1992. - № 22-7/82. – 10 с.
Angen O. Respiratory disease in calves: microbiological investigations on trans-tracheally aspirated bronchoalveolar fluid and acute phase protein response / O. Angen, J. Thomsen, L.E. Larsen et al. // Vet Microbiol. – 2009. – Vol. 137(1-2). – Р.165-171.
Boyce J. Pasteurella / J. Boyce, M. Harper // In: Gyles, C.L., Prescott, J.F., Songer, G. and Thoen, C.O. Pathogenesis of Bacterial Infections in Animals, 4th Edition, (Blackwell Publishing. Ames), 2001. – Р. 325-346.
Carty В. Fatal peritonitis caused by Pasteurella multocida capsular type F in calves / B. Carty, K. Chiers, S. Schwars // J. of Cl. Microbiol. – 2005. – Vol. 43. - P.1480-1483.
Dabo S.M. Pasteurella multocida and bovine respiratory disease / S.M. Dabo, J.D. Taylor, A.W. Confer// Anim. Health. Res. Rev. - 2008. -Vol.8. - Р.129-150.
Dziva F. Diagnostic and typing options for investigating diseases associated with Pasteurella multocida / F. Dziva, A.P. Muhairwa, M. Bisgaard, H. Christensen // Vet. Microbiol. - 2008.- Vol.128. - Р. 1-22.
Griffin D. Bovine pasteurellosis and other bacterial infections of the respiratory tract / D. Griffin // Vet. Clin. Food. Anim. - 2010. - Vol. 26. - P.57-71.
Hunt M.L. The molecular biology of Pasteurella multocida / M.L. Hunt, B. Adler, K.M. Townsend // Vet. Microbiol. - 2000. -Vol.72.- P.3-25.
Kuhnert Р. Pasteurellaceae: Biology, Genomics and Molecular Aspects / P. Kuhnert, H. Christensen // Horizon Scientific Press - 2008. - 267 p.
Kumar P. Identification of Pasteurella multocida isolates of ruminant origin using polymerase chain reaction and their antibiogram study / P. Kumar, V.P. Singh, R.K. Agrawal, S. Singh// Trop. Anim. Health. Prod. - 2009. - Vol. 41. - P. 573-578.
Prado M.E. Maternally and naturally acquired antibodies to Mannheimia haemolytica and Pasteurella multocida in beef calves / M.E. Prado, T.M. Prado, M. Payton// Vet. Im. Immunopathol. - 2006. - Vol.111. - Р.301-307.
Rimler R.B. Serogroup F, a new capsule serogroup of Pasteurella multocida / R. B. Rimler, K.R. Rhoades// J. Clin. microbiol. - 1987. - Vol.25. - P.615-618.
