ИССЛЕДОВАНИЕ ВОЗМОЖНОСТИ ИСПОЛЬЗОВАНИЯ СИРОПА КОРНЯ СОЛОДКИ ПРИ ПОЛУЧЕНИИ ГАЗОМАГНЕЗИТА
Барулина И.В.
Кандидат химических наук, Рудненский индустриальный институт
ИССЛЕДОВАНИЕ ВОЗМОЖНОСТИ ИСПОЛЬЗОВАНИЯ СИРОПА КОРНЯ СОЛОДКИ ПРИ ПОЛУЧЕНИИ ГАЗОМАГНЕЗИТА
Аннотация
В статье исследована возможность использования сиропа корня солодки в качестве стабилизатора при использовании углекислого газа в качестве поризатора при получении газомагнезита.
Ключевые слова: пенообразователь, газомагнезит, кислотность раствора.
Barulina I.V.
Candidate of Chemistry, Rudny Industrial Institute
STUDY OF THE USE OF SYRUP LICORICE ROOT IN OBTAINING GAZOMAGNEZITA
Abstract
The paper studies the use of syrup of licorice root as a stabilizer when using carbon dioxide as the adjustable long when picked gazomagnezita.
Keywords: foamer, gazomagnezit, acidity of the solution.
В современных литературных источниках [1-4] приводится множество различных способов поризации бетонов с целью получения облегченных строительных материалов с улучшенными теплоизляционными и звукоизолирующими свойствами.
По способу создания ячеистой структуры все используемые методы можно классифицировать следующим образом:
- газообразование (газобетоны, газосиликаты),
- пенообразование (пенобетоны, пеносиликаты),
- аэрирование (аэрированный ячеистый бетон, аэрированный ячеистый силикат).
К модификациям способов поризации относятся:
- вспучивание массы газообразованием в вакууме (небольшое разрежение),
- аэрирование массы под давлением (барботирование её сжатым воздухом) с последующим снижением давления до атмосферного (баротермальный способ)
- газопенная технология – сочетание метода аэрирования и газообразования.
Для использования в качестве поризатора при получении газомагнезита углекислого газа можно использовать реакцию взаимодействия сульфата алюминия с карбонатом кальция в присутствии неионогенных пенообразователей, которые нечувствительны к присутствию электролитов или катионных поверхносто-активных веществ (ПАВ), так как выделение углекислого газа будет наблюдаться только в кислой среде.
В растворах, содержащих угольную кислоту, создается сложная равновесная система, которую можно изобразить в общем виде следующим образом:
![]()
Значение pH в такой системе, соответствующей насыщенному раствору диоксида углерода в воде при 25 °C и давлении 760 мм рт. ст., можно рассчитать по формуле:
![]()
где L - растворимость CO2 в воде при указанных условиях, равна 0,034 моль/л;
![]() - кажущаяся константа диссоциации, равная 4,7·10-7.
- кажущаяся константа диссоциации, равная 4,7·10-7.
Таким образом, для выделения диоксида углерода необходимо, чтобы рН раствора был не выше 4, только в этом случае образовавшаяся в результате гидролиза угольная кислота будет разлагаться с образованием диоксида углерода. Для стабилизации в растворе диоксида углерода необходимо использовать неионогенные (синтанол АЛМ-10) или катионные (катионит КУ-2-8) поверхностно-активные вещества.
В работе исследовалась возможность пенообразования в присутствии экстракта корня солодки и сиропа корня солодки, которые эффективно используются для пенообразования, так как содержат органические вещества, обладающие поверхностно-активными свойствами. Экстракт готовился на водяной бане при соотношении 1:15 корня солодки и воды. Экстракт настаивался в течение 20 минут и хранился в холодильнике не более 5 суток.
Сироп более устойчив при хранении, так как в состав входят этиловый спирт и сахар для стабилизации раствора. В состав экстракта корня солодки входят поверхностно-активные вещества различного характера, в том числе и аспарагин, который является ПАВ катионного типа, а, следовательно, эффективен при стабилизации углекислого газа в кислой среде. Первоначально определили критическую концентрацию мицеллообразования экстракта и сиропа солодки. В качестве раствора использовался раствор хлорида магния с плотностью 1,2 г/мл, к которому добавлялся экстракт или сироп корня солодки и определялось поверхностное натяжение сталагмометрическим методом.
Поверхностное натяжение рассчитывалось по формуле:
![]() (1)
(1)
где ρх и ρо – плотность исследуемой и стандартной жидкостей;
nх и n0 – количество капель при истечении из сталагмометра
исследуемой жидкости (nx) и жидкости (nо) с известным поверхностным натяжением (sо).
Результаты зависимости поверхностного натяжения от объемной концентрации экстракта корня солодки представлены на рисунке 1.
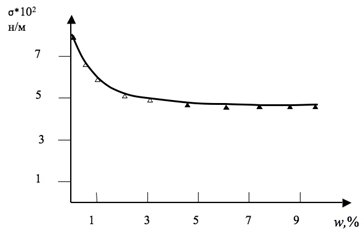
Рис. 1 – Зависимость поверхностного натяжения от объёмной концентрации сиропа солодки
При концентрации экстракта или сиропа более 5 объемных процентов поверхностное натяжение не изменяется, следовательно, критическая концентрация мицеллообразования равна данному значению.
Поскольку важную роль в образовании углекислого газа в растворе играет кислотность, при добавлении реагентов каждый раз измерялся рН раствора. Раствор хлорида магния имеет рН 4.0-4.2, вследствие процесса гидролиза по катиону:
МgCl2 + H2O ↔ Mg(OH)Cl + HCl
Гидролиз процесс обратимый, поэтому при увеличении рН раствора выделяющийся катион водорода (вследствие диссоциации соляной кислоты) будет связываться с гидроксо- группой и гидролиз будет усиливаться. Также увеличению скорости гидролиза будет способствовать повышение температуры. Соли, образованные более слабыми основаниями, например, соли алюминия, гидролизуются сильнее, а, следовательно, скорость взаимодействия с карбонатом кальция будет выше.
Для поризации магнезита использовали дисперсный карбонат кальция и сернокислый алюминий, взаимодействие между которыми идет по реакции с выделением СО2:
Al2(SO4)3 + 3CaCO3 + 8H2О == 2Al(ОН)3 + 3CaSO4·2Н2О + 3СО2.
Если учесть, что объём газа должен составлять 85% от общего объема газомагнезита, то объем выделяющегося газа будет составлять 850 л при получении 1 м3 газобетона. Количество моль выделившегося углекислого газа при температуре 250С будет равен 850:24,04 =35,36 моль. По уравнению реакции рассчитываем количество прореагировавших веществ. Результаты представлены в таблице 1.
Таблица 1 – Расчетные соотношения масс реагирующих веществ
| Вещество | Количество вещества, n моль | Масса, m кг | Соотношение масс |
| CaCO3 Al2(SO4)3 | 35,36 11,79 | 3,536 4,022 | 1 1,14 |
Первоначально изучена смесь, состоящая из раствора хлорида магния с плотностью 1,2 г/мл, к которой добавляли экстракт корня солодки, сульфат алюминия до растворения и карбонат кальция. Изучено влияние количества компонентов сульфата алюминия и карбоната кальция на пенообразование и устойчивость пены, причем соотношение компонентов соответствовало рассчитанному.
При добавлении сульфата алюминия в количестве 0,11 грамм к 10 мл раствора хлорида магния рН раствора практически не изменялся. При добавлении 1 мл экстракта солодки рН раствора увеличивался до 5, что снижает содержание углекислого газа в растворе и приведёт к уменьшению скорости и объёма выделяющего углекислого газа. Для поддержания рН на уровне меньше 4 в раствор добавлялась щавелевая кислота (0,4-0,8% по массе). Затем к полученному раствору добавлялся карбонат кальция, при этом наблюдалось выделение углекислого газа и вспенивание раствора. Значительное вспенивание наблюдалось только в том случае, когда происходило перенасыщение раствора углекислым газом, и он начинал выделяться из раствора. Так как карбонат кальция является плохо растворимым веществом, то скорость выделения газа существенно зависит от степени его дисперсности. Время устойчивости пены составляло не менее 30 минут. Кратность увеличения объёма раствора зависела от масс карбоната кальция и сульфата алюминия, вводимых в раствор. Полученные результаты приведены в таблице 2.
Таблица 2 – Зависимость увеличения объёма раствора от массы компонентов
| Номер образца | Масса Al2(SO4)3, г | Масса CaCO3, г | Кратность увеличения объема, Vп|Vр |
| 1 | 0,11 | 0,1 | 1,1 |
| 2 | 0,23 | 0,2 | 1,5 |
| 3 | 0,34 | 0,3 | 5 |
| 4 | 0,46 | 0,4 | 6 |
С увеличением масс компонентов, используемых для образования газа, существенно увеличивалась скорость выделения диоксида углерода, что приводило к увеличению объёма образующейся пены. Однако при добавлении вяжущего оксида магния происходило резкое уменьшение скорости образования диоксида углерода и уменьшения объёма пены, особенно в образцах 3 и 4, за счет взаимодействия оксида магния с водой и с находящимися в растворе кислотами, образующимися в результате гидролиза, и резкого увеличения рН раствора до 9-10. В щелочном растворе углекислый газ, взаимодействуя с раствором гидроксида магния, образует карбонат магния, и выделение газа прекращается:
МgO + 2HCl → MgCl2 + H2O
МgO+ H2O → Mg(OH)2
CO2 + Mg(OH)2 → MgCO3 + H2O.
Образующая в результате гидролиза кислота полностью взаимодействует при добавлении магнезита, так как мольное соотношение данных веществ в смеси соответствует 1:22. В магнезите остаются только те мелкодисперсные пузырьки газа, которые стабилизированы пенообразователем в растворе (образцы 1 и 2). Поэтому полученный пеномагнезит обладает мелкопористостью. Увеличение объема в процессе твердения практически не происходит и образование «горбушки» не наблюдалось, поскольку в щелочной среде выделения диоксида углерода из раствора невозможно. Причем при увеличении массы карбоната кальция (образцы 3 и 4) скорость выделения газа возрастала, при этом радиус пузырька и величина пор увеличивались, и полученный материал обладал повышенной хрупкостью.
В результате исследования установлен оптимальный состав газомагнезита: 10 мл раствора хлорида магния с плотностью 1,2 г/мл, 0,11 г сульфата алюминия, 1 мл экстракта корня солодки, 0,05 г щавелевой кислоты, 0,1 г карбоната кальция и 7,5 г магнезита. Объём изделия за счет газообразования увеличивается на 30-35%, плотность полученного материала колеблется от 1,0 до 1,1 г/см3.
Снизить плотность и увеличить пористость можно только при сохранении кислотности в смеси на уровне рН= 4, а для этого вместо магнезита необходимо вводить, например, гипс, который является малорастворимым веществом с нейтральной реакцией среды.
Литература
- Мартынов, В. И. Анализ: структурообразования и свойств неавтоклавного пенобетона. Текст. / В.И. Мартынов // Строительные материалы. 2005. - № 1. - С. 48-49.
- Пинскер В. А. Ячеистый бетон как испытанный временем материал для капитального строительства Текст. / В.А. Пинскер, В. П. Выглежанин // Строительные материалы. 2004. - № 3. – с. 44-45.
- Портик, А. А. Всё о пенобетоне Текст. / А. А. Портик. С-Пб. : Стройиздат, 2003.-224 с.
- Прохоров, С.Б. Новые алюминиевые газообразователи Текст. / С. Б. Прохоров, JI. Ф. Вагина // Строительные материалы. – 2006. № 6. - С. 18-19.
