ФАРМАКОКИНЕТИКА АНАЛОГОВ ИНСУЛИНА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ ПРИ САХАРНОМ ДИАБЕТЕ 2 ТИПА
Сорокина Ю.А.1, Копылова М.В.2, Фаткина Д.А.3 , Ловцова Л.В.4
1 ORCID: 0000-0001-8430-237X, Кандидат биологических наук,
2 Ассистент,
3 Студент,
4 ORCID:0000-0003-1480-183X, Доктор медицинских наук, доцент,
1,2,3,4 Приволжский исследовательский медицинский университет Министерства здравоохранения Российской Федерации, Нижний Новгород, Россия
ФАРМАКОКИНЕТИКА АНАЛОГОВ ИНСУЛИНА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ ПРИ САХАРНОМ ДИАБЕТЕ 2 ТИПА
Аннотация
В обзоре литературы приведены фармакокинетические особенности современных аналогов инсулина длительного и сверхдлительного действия, которые отражаются на эффективности и безопасности инсулинотерапии при сахарном диабете 2 типа. Рассмотрены имеющиеся проблемы, связанные с началом инсулинотерапии, а также пути их решения. Все особенности и недостатки имеющихся аналогов подталкивают современную фармацевтическую промышленность к модифицированию уже хорошо исследованных, эффективных и безопасных аналогов, созданию эквивалентных биосимиляров, с поиском путей стабилизации фармакодинамических свойств человеческого инсулина за счет более предсказуемой фармакокинетики.
Ключевые слова: фармакокинетика, инсулин гларгин, детемир, деглудек, аспарт, сахарный диабет 2 типа, инсулинотерапия.
Sorokina Yu.A.1, Kopylova M.V.2, Fatkina D.A.3, Lovtsova L.V.4
1 ORCID: 0000-0001-8430-237X, PhD in Biology,
2 Assistant,
3 Student,
4 ORCID: 0000-0003-1480-183X, MD, Associate professor,
1,2,3,4 Privolzhsky Research Medical University of the Ministry of Health of the Russian Federation, Nizhny Novgorod, Russia
PHARMACOKINETICS OF ANALOGS OF INSULIN OF LONG-TERM ACTION IN INSULIN-DEPENDENT DIABETES
Abstract
According to the review of the literature, the pharmacokinetic features of modern insulin analogs of long-term and super-long-acting effects that affect the efficiency and safety of insulin therapy in insulin-dependent diabetes are presented. The existing problems associated with the onset of insulin therapy, as well as the ways to solve them are considered. All the peculiarities and drawbacks of the existing analogs push the modern pharmaceutical industry to modify already well-researched, effective and safe analogs, to create equivalent biosimilars, and to find ways to stabilize the pharmacodynamic properties of human insulin through more predictable pharmacokinetics.
Keywords: pharmacokinetics, insulin glargine, detemir, degludec, aspart, insulin-dependant diabetes.
В современном представлении сахарный диабет 2 типа (СД 2 типа) перестал именоваться инсулиннезависимым, так как был заново пересмотрен патогенез и течение заболевания. Сегодня инсулинотерапия является важной и полноценной составляющей фармакотерапии пациентов с СД 2 типа [1]. Достижения современных биотехнологий позволили получать аналоги человеческого инсулина, а также биосимиляры [2] (рисунок 1).
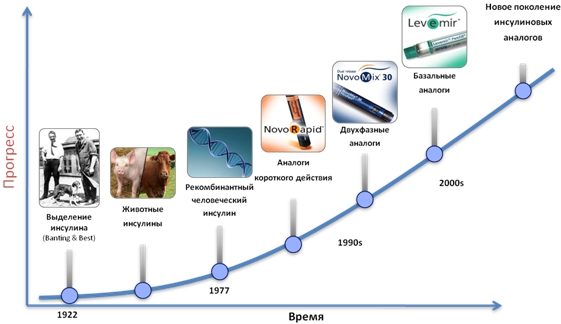
Риc. 1 – Прогресс препаратов инсулина и аналогов
Современные рекомендации, основанные, на исследованиях фармакокинетики препаратов инсулина, включают в схему инсулинотерапии в том числе аналоги инсулина длительного, сверхдлительного действия [1], [3] (представлены в таблице 1). Ниже приведены некоторые ключевые требования к препаратам [3], [4]:
- отсутствие иммуногенности
- отсутствие пиков, стабильный, плоский фармакодинамический профиль
- уровень контроля без увеличения риска гипогликемий с фиксированным дозированием
- доступность
- возможность использования в комбинации с другими препаратами
Таблица 1 – Аналоги инсулинов длительного действия и их комбинации
| Вид | МНН | ТН | Начало, часы | Продолжительность, часы |
| Длительного действия | Инсулин гларгин гла-100 Гла-300 | Лантус Туджео | 1-2 | 29 |
| 36 | ||||
| Инсулин детемир | Левемир | 24 | ||
| Сверхдлительного действия | Инсулин деглюдек | Тресиба | 1-2 | 42 |
| Готовые комбинации аналогов инсулина сверхдлительного действия и аналогов инсулина ультракороткого действия | Инсулин деглудек + инсулин аспарт | Райзодег | Как у аналогов инсулина сверхдлительного действия и аналогов инсулина ультракороткого действия – в комбинации они действуют раздельно | |
Однако при начале инсулинотерапии возникают определенные трудности, для решения которых необходимо участие, как врача, так и пациента:
- При сахарном диабете 2 и 1 типа единицы действия аналогов инсулина не эквивалентны.
- Пациенты неправильно рассчитывают дозы или пытаются сэкономить, что приводит к неэффективности терапии.
- Пациенты боятся гипогликемий. Гипогликемия может привести к снижению уровня гликемического контроля и повышению риска осложнений и отрицательно влияет на приверженность лечению, общее самочувствие, а также ассоциируется с экономической нагрузкой
- При инсулинотерапии часто наблюдается увеличение веса (рисунок 2) [4].
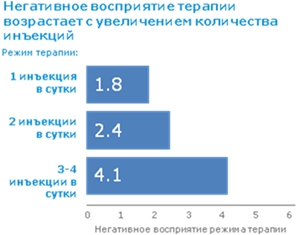
Рис. 2 – Негативное восприятие инсулинотерапии пациентом
Примечание: оценка пациентами восприятия сложности режима по шкале 0-6 баллов; чем выше оценка, тем выше негативное восприятие пациентами (0 - наиболее положительное восприятие, 6 – наиболее негативное восприятие
Пациенты с СД 2 типа, получающие инсулин, как правило, имеют наиболее высокую вариабельность гликемий, что увеличивает риск осложнений [5].
Для решения этой проблемы разрабатываются новые препараты инсулина с оптимизированными фармакокинетическими свойствами - аналоги инсулина пролонгированного действия. Так как фармакодинамика аналогов инсулинов достаточно хорошо изучена, большее внимание уделяется именно фармакокинетике, которая, в свою очередь, определяет эффективность и, что самое главное, безопасность препарата [5], [6].
Особенность инсулина гларгин
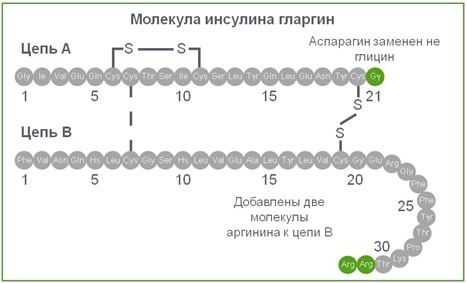
Рис. 3 – строение молекулы инсулина гларгин
Молекула гларгина отличается от молекулы инсулина человека наличием двух дополнительных остатков аргинина и заменой аспарагина на глицин (рисунок 3). Однако существуют несколько модификаций данного аналога человеческого инсулина - гларгин U100 и U300. Структура молекул гларгин U100 и ларгин U300 идентична. Гла-300 (U300) содержит то же количество гларгина в 1/3 части объема в сравнении с Гла-100 (U100). Обе субстанции стабильны и растворимы в условиях кислой pH, но формируют преципитат при физиологической pH в подкожной клетчатке, что обеспечивает медленное растворение (в отличие от других инсулинов с пролонгированным профилем). Фармакокинетика гларгина характеризуется битрансформацией в метаболиты M1 и М2, что делает В-цепь молекулы гларгина идентичной В-цепи инсулина человека. Концентрации активных метаболитов М1 и М2 в плазме не имеют выраженного пика, что обусловливает низкую вариабельность гликемии и риск гипогликемии. По метаболической активности метаболиты М1 и М2 подобны инсулину гларгин, в то время как их митогенный эффект не превышает таковой у инсулина человека. Митогенный эффект связан с активацией процессов в органах кроветворения, нервной системе, опухолях, и является нежелательным [10].
Вследствие более компактного распределения в подкожном депо гларгин 300 U обладает более стабильными и продолжительными фармакокинетическим и фармакодинамическим профилями по сравнению с гларгином 100U: после введения в одинаковых дозах демонстрирует более ровное и пролонгированное распределение концентрации в течение суток, период полувыведения в среднем на 5,5 часа больше [10]. Однако при всех положительных характеристиках у инсулина гларгин есть и недостатки. Например, нейтральное значение изоэлектрической точки гларгина лишает возможности смешивать препарат с короткодействующими формами инсулина, например, инсулином аспарт растворим при низкой pH и образует преципитаты при pH 7,4. Аналоги инсулина ультракороткого действия не совместимы с инсулином гларгин при низкой pH, так как растворимы при pH 7,4.
Особенность инсулина детемир
Инсулин детемир растворим в нейтральной среде. Его молекулярная структура отличается от структуры человеческого инсулина отсутствием треонина в положении ВЗО и присоединением к лизину в положении В29 миристиновой кислоты — жирнокислотного остатка из 14 атомов углерода.
Присоединение к молекуле инсулина жирных кислот, которые связываются с альбумином в крови, позволило получить инсулиновый аналог, который остается в растворенном состоянии после инъекции. Таким образом, был устранен один из основных источников вариабельности действия препарата. После инъекции инсулин детемир образует жидкостное депо в подкожной жировой клетчатке. Молекулы инсулина в растворе соединены в гексамеры. Как только введенный инсулин детемир попадает в интерстициальную жидкость, разведение раствора приводит к обратимой агрегации некоторых гексамеров, которые формируют дигексамеры. Такая агрегация происходит в результате контакта между цепями жирных кислот молекул инсулина. Дальнейшее разведение приводит к распаду гексамеров на димеры и мономеры. Гексамеры и димеры проходят через капиллярную стенку очень медленно, а свободные мономеры инсулина детемир быстро проникают в циркуляцию. Большинство мономеров быстро связывается с молекулами альбумина сыворотки крови. Свободные мономеры инсулина детемир выходят из циркуляции и достигают тканей-мишеней.
Вместе с тем ацилирование приводит к снижению сродства к инсулиновым рецепторам, что обусловливает необходимость в увеличении концентрации аналога инсулина для достижения эквивалентной биоактивности с препаратами инсулина человека, а для достижения такого же метаболического эффекта, как эффект неацилированных инсулинов. Так одна «единица» детемира оказывается биоэквивалентной 1 международной единице инсулина человека при СД 1 типа, но менее биоэквивалентной — при СД 2 типа и, как показывают клинические исследования, примерно на 30% менее активной, чем 1 единица гларгина при СД 1 и 2 типа.
Детемир обладает более низким сродством к рецепторам инсулина, оказывает меньшее влияние на рост клеток и митогенность, чем человеческий инсулин. А пролиферативный и онкогенный потенциал гларгина не отличается от потенциала инсулина человека. Детемир растворим при нейтральных значениях pH и поэтому не вызывает боли при инъекции [11], [12], [13].
Инсулин детемирпри смешивании с аналогами инсулина ультракороткого действия в стандартных условиях, образуются смешанные гексамеры с неконтролируемыми фармакокинетическими и фармакодинамическими характеристиками (рисунок 4) [14].
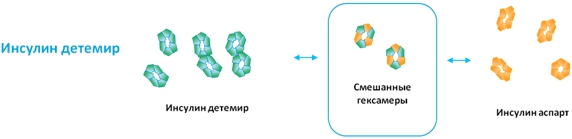
Рис. 4 – Смешанные гексамеры инсулина детемир и инсулина аспарт
Особенность инсулина деглудек
В создании молекулы инсулина деглудек использована технология присоединения жирнокислотного остатка через линкер в виде глутаминовой кислоты с удалением аминокислоты из 30 положения цепи В. В подкожной клетчатке сразу после инъекции и диффузии фенола дигексамеры становятся открытыми с обоих концов, что способствует их связыванию друг с другом с образованием длинных цепочек мультигексамеров в присутствии цинка. диффузия цинка из подкожного депо происходит медленно, гексамеры постепенно отщепляются от обоих концов участков мультигексамера, мономеры медленно и постепенно попадают в кровь. Полученные фармакокинетические свойства привели к увеличенному периоду полувыведения из депо до 25 часов, а действие препарата в 2 раза дольше инсулина гларгин [15]. Медленное стабильное всасывание определяет фармакокинетические и фармакодинамические свойства инсулина деглудек. Плоский профиль действия, низкая вариабельность и достижение стабильной концентрации на 3-4 сутки введения. Важно, что фармакокинетика инсулина деглудек не меняется с возрастом, а также при нарушении функции печени и почек [16], [17].
Важен тот факт, что физико – химические свойства инсулина деглудек позволяют совмещать инсулина деглудек (70%) и инсулина аспарт (30%) в одной лекарственной форме с сохранением фармакодинамических и фармакокинетических свойств индивидуальных компонентов.
Фармакодинамические эффекты компонентов комплексного препарата отчетливо различаются. При введении лекарственной формы дважды в сутки обеспечивается потребность в базальном инсулине и прандиальный контроль двух основных приемов пищи.
Заключение
Важнейшим достижением диабетологии стало появление пролонгированных аналогов инсулина, в частности гларгина, детемира, деглудека. Тем не менее, в настоящее время заместительная инсулиновая терапия сахарного диабета 2 типа еще не совершенна. Большое значение в этом имеет экономические аспекты, такие как большая стоимость базальных инсулинов. Также большинство больных изначально демонстрируют готовность к инсулинотерапии, понимают её важность и значимость, в реальности же это не означает надлежащего самоконтроля и соблюдения предписанного режима лечения в будущем. Врач может недооценивать значимость инсулинотерапии для конкретного больного, сомневаться в том, что пациент будет досконально выполнять рекомендации, что может привести к гипогликемии, медработник не обладает достаточным временем для обучения пациента правильному дозированию или не может принять решение об интенсификации режима. Принимая во внимание все требования и недостатки имеющихся аналогов, современная фармацевтическая промышленность модернизует уже хорошо исследованные, эффективные и безопасные субстанции аналогов или идет по пути поиска стабилизации фармакодинамических свойств человеческого инсулина за счет более предсказуемой фармакокинетики.
Список литературы / References
- Алгоритмы специализированной медицинской помощи больным сахарным диабетом / Под редакцией И.И.Дедова, М.В. Шестаковой, А.Ю. Майорова. – 8-й выпуск. – М.: УП ПРИНТ; 2017. – 112 с.
- Климонтов В.В. Биосимиляры аналогов инсулина: что мы должны о них знать / В.В. Климонтов, Н.Е. Мякина // Эффективная фармакотерапия. – 2015. – №7. – С. 28-34.
- Tibaldi J.M. Evolution of insulin development: focus on key parameters / J.M. Tibaldi // Adv. Ther. – 2012. – Vol. 29. – P. 590-619.
- Peyrot M. Insulin adherence behaviours and barriers in the multinational Global Attitudes of Patients and Physicians in Insulin Therapy Study / M. Peyrot, A.H. Barnett, L.F. Meneghini and others // Diabetic Medicine. 2012:29:682-689.
- Климонтов В.В. Вариабельность гликемии при сахарном диабете / В.В. Климонтов, Н.Е. Мякина. – Новосибирск: ИПЦ НГУ, 2016. – 252с.
- Bербовая Н.И. Аналоги инсулина пролонгированного действия: сравнительная характеристика строения, фармакологических свойств, возможностей клинического применения / Н.И Bербовая // Проблемы эндокринологии. – – №2. – С. 64-71.
- Dailey G. A review of the safety and efficacy data for insulin glargine 300 units/mL, a new formulation of insulin glargine / Dailey, F. Lavernia // Diabetes Obes Metab. – 2015. – №17(12). – Р. 1107-1114.
- Steinstraesser A. Investigational new insulin glargine 300 U/ml has the same metabolism as insulin glargine 100 U/ml / Steinstraesser, R. Schmidt, K. Bergmann and others // Diabetes Obes Metab. – 2014. -№16(9). – Р. 873–876. doi: 10.1111/dom.12283
- Steinstraesser A. New insulin glargine 300 Units mL-1 provides a more even activity profile and prolonged glycemic control at steady state compared with insulin glargine 100 Units mL-1. / A. Steinstraesser, R. Schmidt, K.Bergmann and others // Diabetes Care. – 2015. – №38(4). – Р.637-6 doi: 10.2337/dc14-0006.
- Tennagels N. The metabolic and mitogenic properties of basal insulin analogues / N. Tennagels, U. Werner // Archives of Physiology and Biochemistry. – 2013. - №119(1). – Р.1–14. doi: 10.3109/13813455.2012.754474
- Климонтов В.В. Инсулин гларгин: фармакокинетические и фармакодинамические основы клинического эффекта / В.В. Климонтов, Н.Е. Мякина // Сахарный диабет. – 2014. – №4. – С. 99-107.
- Дедов И.И. Современные базальные инсулины: продолжение истории или начало новой эры / И.И. Дедов // Сахарный диабет. – 2015. – №18 (4). – С. 5-11.
- Аметов А.С. Преимущества терапии сахарного диабета инсулиновым аналогом/ А.С. Аметов, Т.Н. Солуянова // Медицинский cовет. – 2011. – №7-8. – С. 21-24
- Jonassen I. Design of the novel protraction mechanism of insulin degludec, an ultra-long-acting basal insulin / I. Jonassen, S. Havelund, T. Hoeg-Jensen and others // Pharm Res. – 2012 – №29(8). – Р. 2104-2114. doi: 10.1007/s11095-012-0739-z.
- Шестакова М.В. Инсулин деглудек: новый базальный аналог инсулина сверхдлительного действия. Безопасность и эффективность у российских пациентов с сахарным диабетом / М.В. Шестакова, М.Б. Анциферов, А.Ю. Майоров и др. // Сахарный диабет. – 2015. – №18(4). – C. 130-141. DOI: 10.14341/DM7694
- Европейская Медицинская ассоциация. - [Electronic resorce] URL: https://goo.gl/cwvoZE (accessed: 28.03.2018)
- Kupčová V. Insulin degludec: pharmacokinetic properties in subjects with hepatic impairment / V. Kupčová, G. Arold, C. Roepstorff and others // Clin Drug Investig. – 2014. -№34(2). – Р. 127-133.. doi: 10.1007/s40261-013-0154-1.
- Steensgaard D.B. Ligand-controlled assembly of hexamers, dihexamers, and linear multihexamer structures by the engineered acylated insulin degludec / D.B. Steensgaard, G. Schluckebier, H.M. Strauss and others // Biochemistry. – 2013. – №52(2). – Р. 295-309. doi: 10.1021/bi3008609
- Fulcher G. Comparison of insulin degludec/insulin aspart and biphasic insulin aspart 30 in uncontrolled, insulin-treated type 2 diabetes: a phase 3a, randomized, treat-to-target trial / G. Fulcher, J.S. Christiansen, G. Bantwal and others // Diabetes Care. – 2014. – №37(8). – Р. 2084–2090.
- Heise T. Distinct prandial and basal glucose-lowering effects of insulin degludec/insulin aspart (IDegAsp) at steady state in subjects with type 1 diabetes mellitus / T. L .Heise, Nosek, C. Roepstorff and others // Diabetes Therapy. – – №5(1). – Р. 255–265.
- Дедов И.И. Инсулин деглудек/инсулин аспарт – первый комбинированный препарат базального и прандиального аналогов инсулина / И.И. Дедов, М.В. Шестакова // Сахарный диабет. – 2014. – №4. – C. 108-119
Список литературы на английском языке / References in English
- Algoritmy specializirovannoj medicinskoj pomoshchi bol'nym saharnym diabetom [Algorithms of specialized medical care for patients with diabetes mellitus] / edited by I.I. Dedova, M.V. SHestakovoj, A.YU. Majorova. – 8th – M.: UP PRINT; 2017. – 112 p. [in Russian]
- Klimontov V.V. Biosimilyary analogov insulina: chto my dolzhny o nih znat' [Biosimilars of insulin analogues: what we need to know about them] / V.V. Klimontov, N.E. Myakina // Effektivnaya farmakoterapiya. [Effective pharmacotherapy] – 2015. – №7. – P. 28-34. [in Russian]
- Tibaldi J.M. Evolution of insulin development: focus on key parameters / J.M. Tibaldi // Adv. Ther. – 2012. – Vol. 29. – P. 590-619.
- Peyrot M. Insulin adherence behaviours and barriers in the multinational Global Attitudes of Patients and Physicians in Insulin Therapy Study / M. Peyrot, A.H. Barnett, L.F. Meneghini and others // Diabetic Medicine. – 2012 – 29 – P. 682-689.
- Klimontov V.V. Variabel'nost' glikemii pri saharnom diabete [Variability of glycemia in diabetes mellitus] / V.V. Klimontov, N.E. Myakina. – Novosibirsk: IPC NGU, 2016. – 252p. [in Russian]
- Berbovaya N.I. Analogi insulina prolongirovannogo dejstviya: sravnitel'naya harakteristika stroeniya, farmakologicheskih svojstv, vozmozhnostej klinicheskogo primeneniya [Analogues of insulin prolonged action: a comparative characteristic of the structure, pharmacological properties, the possibilities of clinical application] / N.I Berbovaya // Problemy ehndokrinologii [Problems of endocrinology]. – 2010. – №2. – P.64-71. [in Russian]
- Dailey G. A review of the safety and efficacy data for insulin glargine 300 units/mL, a new formulation of insulin glargine / Dailey, F. Lavernia // Diabetes Obes Metab. – 2015. – №17(12). – Р. 1107-1114.
- Steinstraesser A. Investigational new insulin glargine 300 U/ml has the same metabolism as insulin glargine 100 U/ml / Steinstraesser, R. Schmidt, K. Bergmann and others // Diabetes Obes Metab. – 2014. – №16(9). – Р. 873–876. doi: 10.1111/dom.12283
- Steinstraesser A. New insulin glargine 300 Units · mL-1 provides a more even activity profile and prolonged glycemic control at steady state compared with insulin glargine 100 Units · mL-1. / A. Steinstraesser, R. Schmidt, K. Bergmann and others // Diabetes Care. – 2015. – №38(4). – Р.637-6 doi: 10.2337/dc14-0006.
- Tennagels N. The metabolic and mitogenic properties of basal insulin analogues / N. Tennagels, U. Werner // Archives of Physiology and Biochemistry. – 2013. – №119(1). – Р.1–14. doi: 10.3109/13813455.2012.754474
- Klimontov V.V. Insulin glargin: farmakokineticheskie i farmakodinamicheskie osnovy klinicheskogo ehffekta [Insulin glargine: pharmacokinetic and pharmacodynamic bases of the clinical effect] / V.V. Klimontov, N.E. Myakina // Saharnyj diabet [Diabetes mellitus]. – 2014. – №4. – P. 99-107. [in Russian]
- Dedov I.I. Sovremennye bazal'nye insuliny: prodolzhenie istorii ili nachalo novoj ehry [Modern basal insulins: continuation of history or the beginning of a new era] / I.I. Dedov // Saharnyj diabet [Diabetes mellitus]. – 2015. – №18 (4). – P. 5-11. [in Russian]
- Ametov A.S. Preimushchestva terapii saharnogo diabeta insulinovym analogom [Advantages of diabetes therapy with insulin analogue] / A.S. Ametov, T.N. Soluyanova // Medicinskij covet [The medical council]. – 2011. – №7-8. – P. 21-24 [in Russian]
- Jonassen I. Design of the novel protraction mechanism of insulin degludec, an ultra-long-acting basal insulin / I. Jonassen, S. Havelund, T. Hoeg-Jensen and others // Pharm Res. – 2012 – №29(8). – Р. 2104-2114. doi: 10.1007/s11095-012-0739-z.
- Shestakova M.V. Insulin degludek: novyj bazal'nyj analog insulina sverhdlitel'nogo dejstviya. Bezopasnost' i ehffektivnost' u rossijskih pacientov s saharnym diabetom [nsulin degludec: a new basal analogue of insulin of super-long action. Safety and efficacy in Russian patients with diabetes mellitus] / M.V. SHestakova, M.B. Anciferov, A.Yu. Majorov and others // Saharnyj diabet [Diabetes mellitus]. – 2015. – №18(4). – P. 130-141. DOI: 10.14341/DM7694 [in Russian]
- European medical association. [Electronic resource] URL: https://goo.gl/cwvoZE (accessed: 28.03.2018)
- Kupčová V. Insulin degludec: pharmacokinetic properties in subjects with hepatic impairment / V. Kupčová, G. Arold, C. Roepstorff and others // Clin Drug Investig. – 2014. -№34(2). – Р. 127-133. doi: 10.1007/s40261-013-0154-1.
- Steensgaard D.B. Ligand-controlled assembly of hexamers, dihexamers, and linear multihexamer structures by the engineered acylated insulin degludec / D.B. Steensgaard, G. Schluckebier, H.M. Strauss and others // Biochemistry. – 2013. – №52(2). – Р. 295-309. doi: 10.1021/bi3008609
- Fulcher, G. Comparison of insulin degludec/insulin aspart and biphasic insulin aspart 30 in uncontrolled, insulin-treated type 2 diabetes: a phase 3a, randomized, treat-to-target trial / G. Fulcher, J.S. Christiansen, G. Bantwal and others // Diabetes Care. – 2014. – №37(8). – Р. 2084–2090.
- Heise T. Distinct prandial and basal glucose-lowering effects of insulin degludec/insulin aspart (IDegAsp) at steady state in subjects with type 1 diabetes mellitus / T. L .Heise, Nosek, C. Roepstorff and others // Diabetes Therapy. – - №5(1). – Р. 255–265.
- Dedov I.I. Insulin degludek/insulin aspart – pervyj kombinirovannyj preparat bazal'nogo i prandial'nogo analogov insulin [Insulin degludec / insulin aspart - the first combined preparation of basal and prandial insulin analogues] / I.I. Dedov, M.V. SHestakova // Saharnyj diabet [Diabetes mellitus] – 2014. – №4. – P. 108-119 [in Russian]
