СТАНДАРТИЗАЦИЯ ГЕЛЯ «ИБУПРОЗОЛЬ» С ПРИМЕНЕНИЕМ АЛКАЛИМЕТРИЧЕСКОГО МЕТОДА
Бачева Н.Н.1, Илиев К.И.2, Кобелева Т.А.3, Сичко А.И.4
1Аспирант, 2ассистент, 3доктор фармацевтических наук, профессор, 4доктор фармацевтических наук, профессор, Тюменский государственный медицинский университет
СТАНДАРТИЗАЦИЯ ГЕЛЯ «ИБУПРОЗОЛЬ» С ПРИМЕНЕНИЕМ АЛКАЛИМЕТРИЧЕСКОГО МЕТОДА
Аннотация
Предложена новая мягкая лекарственная форма «Ибупрозоль», изготовленная на основе геля «Тизоль» и содержащая 3,0 % ибупрофена. Установлена константа ионизации лекарственного препарата в водно-этанольной среде, рассчитана и построена кривая алкалиметрического титрования, осуществлен выбор индикаторов. Разработан простой и воспроизводимый способ количественного анализа ибупрофена в мази, позволяющий определять содержание фармакологически активного вещества с погрешностью в пределах допустимых норм и отклонений, предусмотренных нормативно-технической документацией.
Ключевые слова: ибупрофен, тизоль, алкалиметрическое титрование, количественный анализ препарата в мази.
Bacheva N.N.1, Iliev K.I.2, Kobeleva T.A.3, Sichko A.I.4
1Postgraduate Student, 2Postgraduate Student, 3PhD in Pharmaceutics, Professor, 4PhD in Pharmaceutics, Professor, Tyumen State Medical University
STANDARDIZATION OF “IBUPROSOL” GEL WITH APPLICATION OF ALKALIMETRIC METHOD
Abstract
The article offers a new soft preparation form of “Ibuprozol” based on the “Tizol” gel and containing 3.0% of ibuprofen. The ionization constant of the preparation in the water-ethanol medium was established, the curve of alkalimetric titration was calculated and drawn, and indicators were selected. A simple and reproducible method for the quantitative analysis of ibuprofen in ointments was developed. It enables us to determine the content of a pharmacologically active substance with an error within the limits of permissible norms and deviations provided for by normative and technical documentation.
Keywords: ibuprofen, tizol, alkalimetric titration, quantitative analysis of the preparation in ointments.
В настоящее время наибольшую угрозу качества жизни человечества представляет болевой синдром различного генеза. В связи с этим нами предложена мазь, содержащая 3,0 % ибупрофена. При разработке мягких лекарственных форм, одним из факторов, влияющих на эффективность действия и их стабильность, является основа. Для этой цели нами выбрано органическое металлокомплексное соединение отечественного производства – тизоль, которое уже нашло применение в медицинской практике [1], [3]. Данный гель хорошо сочетается со многими фармакологическими субстанциями, позволяет создавать лекарственные формы, вводимые трансдермально, применять их в педиатрии и геронтологии, при нарушении функций желудочно-кишечного тракта [4]. Предлагаемая лекарственная форма, состоящая из 0,3 г ибупрофена и 9,7 г тизоля, названная нами «Ибупрозоль», может найти применение в неврологии, хирургии и гинекологии, как противовоспалительное, анальгетическое и умеренно жаропонижающее антисептическое средство. Ее рационально применять при ревматоидном артрите, деформирующем остеоартрозе, а также различных формах суставных и внесуставных ревматоидных заболеваниях. Лекарственная форма так же может быть востребована в стоматологии, физиотерапии и педиатрии.
Создание новых лекарственных форм должно сопровождаться разработкой способов установления их доброкачественности. Одним из основных факторов, определяющих качество лекарственных средств, является правильная постановка контроля. Поэтому мы поставили перед собой цель разработать способ стандартизации мази «Ибупрозоль». В аптечных организациях применяют различные виды контроля качества лекарств. Среди них наиболее простым и доступным является химический [2], [5], [6].
Наличие в молекуле ибупрофена карбоксильной группы, дает основание отнести данное вещество к слабым кислотам, поэтому его можно титровать растворами щелочей. Для обоснования данного утверждения и определения оптимальных условий анализа необходимо установить константу ионизации лекарственного препарата, рассчитать, построить кривую титрования и выбрать индикатор.
Для определения константы ионизации ибупрофена готовили исходные 0,01 моль/л растворы лекарственного препарата и 0,1 моль/л раствор гидроксида натрия. Титрование раствора кислоты проводили по следующей методике: в стакан помещали 50,0 мл водно-этанольного раствора (1:1) лекарственного препарата и титровали раствором щелочи, прибавляя его по 0,5 мл. Измеряли значение рН среды после прибавления каждой порции титранта с помощью рН-150МИ. Титрование проводили с использованием стеклянного и хлорсеребряного электродов, термодатчика.
По результатам титрований установили, что константа ионизации ибупрофена равна 0,15∙10-5, рK = 5,82. Нами осуществлено титрование 0,01моль/л спиртового раствора ибупрофена 0,1моль/л раствором гидроксида натрия и установлено, что константа ионизации лекарственного препарата в этаноле равна 0,44∙10-7, рK = 7,35. Это свидетельствует об уменьшении ионизации изучаемого соединения и невозможности осуществлять алкалиметрическое титрование в спиртовой среде. Поэтому, для дальнейших исследований нами выбрана водно-этанольная среда.
Для построения кривой титрования использовали 50,0 мл 0,05 моль/л раствора лекарственного препарата, который титровали 0,05 моль/л раствором гидроксида натрия. Расчет рН среды проводили без учета разбавления и ионной силы с погрешностью объемного анализа ± 0,1 %. Вычисление значений водородного показателя осуществляли до начала, в процессе титрования, в точке и за точкой эквивалентности. На основании полученных данных установили, что ибупрофен является слабой кислотой и при титровании его раствором гидроксида натрия скачок находится в пределах значений водородного показателя 7,11 – 9,70, в точке эквивалентности рН = 9,26. Поэтому для нахождения точки конца титрования рационально использовать такие фармакопейные индикаторы, как нейтральный красный, феноловый красный (рН = 6,8 – 8,4, окраска: красная - желтая), тимоловый синий (рН = 8,0 – 9,6, окраска: желтая - синяя), бромтимоловый синий (рН = 6,0 – 7,6, окраска: желтая - синяя) или крезоловый красный (рН = 7,0 – 8,8, окраска: желтая - пурпурная).
Для прямого титрования ибупрофена в качестве титранта рационально применять 0,02-0,05 моль/л раствор щелочи, так как в прописи содержание лекарственного препарата не превышает 5,0 %. С целью разработки способа количественного определения ибупрофена в мази готовили искусственную смесь, заменяя гель «Тизоль» этанолом. Анализ проводили следующим образом: в колбу для титрования вносили 1,0 мл этанольного раствора ибупрофена, прибавляли 3,0 мл этанола, 4,0 мл воды очищенной, 2 капли нейтрального красного, 1 каплю метиленового синего (смешанный индикатор) и титровали смесь 0,05 моль/л раствором гидроксида натрия до перехода окраски раствора из фиолетового цвета до зеленого. Содержание лекарственного препарата рассчитывали по формулам объемного анализа. Для достоверности опытов провели семь параллельных титрований, и полученные данные статистически обработали (табл. 1).
Таблица 1 – Результаты расчета массовой доли ибупрофена алкалиметрическим методом (смешанный индикатор)
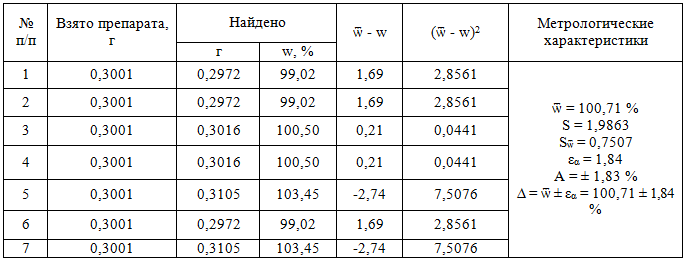
Относительная погрешность анализа ибупрофена равна ± 1,83 %, что дает основание применить данную методику для количественного определения лекарственного препарата в мази. Параллельно провели титрование искусственной смеси в присутствии бромтимолового синего и бромфенолового красного (табл. 2).
Таблица 2 – Результаты алкалиметрического определения ибупрофена
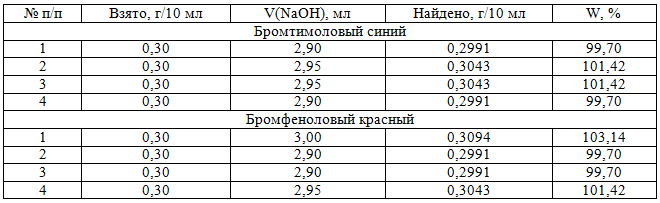
Массовая доля ибупрофена в искусственной смеси с бромтимоловым синим находится в пределах 99,70 – 101,42 %, бромфеноловым красным – 99,70 – 103,14 %. Следовательно, для количественного определения соединения в лекарственной форме можно использовать оба индикатора. Лучший переход окраски раствора наблюдается с применением бромтимолового синего.
На основании проведенных исследований нами предложен способ количественного определении ибупрофена в мягкой лекарственной форме «Ибупрозоль». Методика: точную массу (около 2,0 г) мази помещают в стаканчик, прибавляют 25,0 мл этанола, растворяют лекарственный препарат при перемешивании смеси и фильтруют через складчатый фильтр. К 4,0 мл фильтрата прибавляют 4,0 мл воды очищенной, 2 – 3 капли бромтимолового синего и титруют смесь 0,05 моль/л раствором гидроксида натрия до перехода окраски раствора из желтого до зелено-синего цвета. Ввиду того, что гель «Тизоль» частично растворяется в этаноле, проводят анализ его с аналогичной массой и в одинаковых условиях (контрольный опыт). Содержание ибупрофена в лекарственной форме рассчитывают по формуле объемного анализа.
Таблица 3 – Результаты анализа ибупрофена в мази «Ибупрозоль»
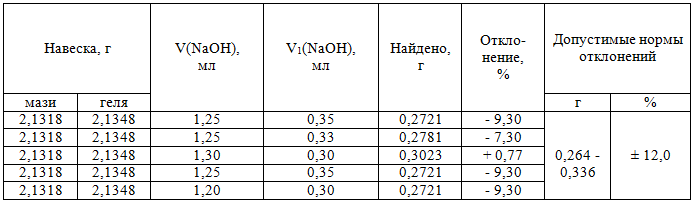
По результатам опытов (табл. 3) установлено, что масса ибупрофена в лекарственной форме находится в пределе 0,2721 - 0,3023 г, а отклонение в процентах составляет от - 9,30 % до + 0,77 %. Это не противоречит допустимым нормам и отклонениям по нормативной документации при анализе ингредиентов в мазях.
Таким образом, исследования по определению константы ионизации ибупрофена, построению кривой титрования, выбору индикаторов, позволили предложить для провизоров-аналитиков простой и точный способ алкалиметрического определения лекарственного препарата в мази «Ибупрозоль».
Список литературы / References
- Бачева Н.Н. Изучение физико-химических свойств новых мягких лекарственных форм, изготовленных на основе геля Тизоль / Н.Н. Бачева, К.И. Илиев, Т.А. Кобелева и др. // Здоровье и образование в XXI веке. - 2016. - Т. 18. - №. 2. - С.721-725.
- Илиев К.И. Применение классических методов анализа для количественного определения лидокаина гидрохлорида в мази «Лидозоль» / К.И. Илиев, Т.А. Кобелева, А.И. Сичко // Научный альманах. - 2015. - № 9. - С. 957-961.
- Илиев К.И. Актуальность исследования и применения в медицинской практике трансдермальной лекарственной формы «Дидиклозоль» / К.И. Илиев, Т.А. Кобелева, А.И. Сичко // Академический журнал Западной Сибири. - № 1 (56). – Т. 11. – 2015. – С. 74 – 75.
- Илиев К.И. Биофармацевтические и фармакологические исследования мази «Лидодиклозоль» / К.И. Илиев, Н.Н. Бачева, Л.П. Ларионов // Медицинская наука и образование Урала. - 2016. - № 2. - С. 127-131.
- Илиев К.И. Химический анализ новой лекарственной формы «Анедиклозоль» / К.И. Илиев, Т.А. Кобелева, А.И. Сичко // Фундаментальные исследования. - 2015. - № 2. - С. 323 - 329.
- Терентьева Н.Е. Количественное определение натрия пара-аминосалицилата в лекарственной форме с тизолем [Электронный ресурс] / Н.Е. Терентьева, К.И. Илиев, Т.А. Кобелева и др. // Современные проблемы науки и образования. – 2014. – № 6. - URL:www.science-education.ru/120-15511 (дата обращения: 26.05.2017).
Список литературы на английском языке / References in English
- Bacheva N.N. Izuchenie fiziko-himicheskih svoystv novyih myagkih lekarstvennyih form, izgotovlennyih na osnove gelya Tizol [The study of physico-chemical properties of new soft medicinal forms, made on basis of gel Tizol] / N.N. Bacheva, K.I. Iliev, T.A. Kobeleva, etc. / / Zdorove i obrazovanie v XXI veke [Health and education in XXI century]. - 2016. - V. 18. - № 2. - P. 721-725. [in Russian]
- Iliev K.I. Primenenie klassicheskih metodov analiza dlya kolichestvennogo opredeleniya lidokaina gidrohlorida v mazi «Lidozol» [Application of classical methods of analysis for quantitative determination of lidocaine hydrochloride in ointments «Lidozol»] / K.I. Iliev, T.A. Kobeleva, A.I. Sichko // Nauchnyiy almanah [Scientific almanac]. - 2015. - № 9. - P. 957-961. [in Russian]
- Iliev K.I. Aktualnost issledovaniya i primeneniya v meditsinskoy praktike transdermalnoy lekarstvennoy formyi «Didiklozol» [Relevance of research and application in medical practice of transdermal dosage forms «Didiklozol»] / K.I. Iliev, T.A. Kobeleva, A.I. Sichko // Akademicheskiy zhurnal Zapadnoy Sibiri [Academic journal of Western Siberia]. - № 1 (56). – V. 11. – 2015. – P. 74 – 75. [in Russian]
- Iliev I.K. Biofarmatsevticheskie i farmakologicheskie issledovaniya mazi «Lidodiklozol» [Biopharmaceutical and pharmacological research of ointment «Lidodiklozol»] / K.I. Iliev, N.N. Bacheva, L.P. Larionov // Meditsinskaya nauka i obrazovanie Urala [Medical science and education of the Urals]. - 2016. - № 2. - P. 127-131. [in Russian]
- Iliev I.K. Himicheskiy analiz novoy lekarstvennoy formyi «Anediklozol» [Chemical analysis of new dosage form «Anediklozol»] / K.I. Iliev, T.A. Kobeleva, A.I. Sichko // Fundamentalnyie issledovaniya [Fundamental research]. - 2015. - № 2. - P. 323 - 329. [in Russian]
- Terentieva N.E. Kolichestvennoe opredelenie natriya para-aminosalitsilata v lekarstvennoy forme s tizolem [Quantitative determination of paraaminosalicylic acid in medicinal form with Tizol] [Electronic resource] / N.E. Terent'eva, I.K. Iliev, T.A. Kobeleva, and others // Sovremennyie problemyi nauki i obrazovaniya [Modern problems of science and education]. – 2014. – № 6. - URL: www.science-education.ru/120-15511 (accessed: 26.05.2017). [in Russian]
