РАСПРЕДЕЛЕНИЕ АЛЬФА-[3-[[2-(3,4-ДИМЕТОКСИФЕНИЛ)-ЭТИЛ]-МЕТИЛАМИНО]ПРОПИЛ]-3,4-ДИМЕТОКСИ-АЛЬФА-(1-МЕТИЛ-ЭТИЛ) БЕНЗОЛАЦЕТОНИТРИЛА В ОРГАНИЗМЕ ТЕПЛОКРОВНЫХ ЖИВОТНЫХ
Квачахия Л.Л.1, Шорманов В.К.2, Андросов И.А.3, Денисов А.А.4
1Кандидат фармацевтических наук, старший преподаватель, Курский государственный медицинский университет, 2Доктор фармацевтических наук, профессор, Курский государственный медицинский университет, 3,4Студент, Курский государственный медицинский университет
РАСПРЕДЕЛЕНИЕ АЛЬФА-[3-[[2-(3,4-ДИМЕТОКСИФЕНИЛ)-ЭТИЛ]-МЕТИЛАМИНО]ПРОПИЛ]-3,4-ДИМЕТОКСИ-АЛЬФА-(1-МЕТИЛ-ЭТИЛ) БЕНЗОЛАЦЕТОНИТРИЛА В ОРГАНИЗМЕ ТЕПЛОКРОВНЫХ ЖИВОТНЫХ
Аннотация
Изучены особенности распределения альфа-[3-[[2-(3,4- диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-ме-тилэтил) бензолацетонитрила в организме всеядных теплокровных животных (крысы) после внутрижелудочного введения половинной летальной дозы отравляющего вещества. Изолирование альфа-[3-[[2-(3,4-диметоксифенил)этил]-метил-амино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацето-нитрила из органов, их содержимого и биожидкостей животных проводили ацетоном. Очистку извлечённого соединения осуществляли хроматографией в колонке «Силасорб С-18» 30 мкм (элюент – ацетонитрил –вода (9:1)). Для идентификации и количественного определения исследуемого соединения использовали методы ТСХ, ГХ-МС и УФ-спектрофотометрии. Присутствие наибольших количеств исследуемого вещества зафикировано в желудке, его содержимом, печени и почках. Полученные результаты позволяют рекомендовать данные органы в качестве основных объектов судебно-химических экспертиз при отравлении верапамилом.
Ключевые слова: альфа-[3-[[2-(3,4-диметоксифенил)этил]метиламино]-пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрил (верапамил), распределение, судебно-химический анализ.
Kvachakhiya L.L.1, Shormanov V.K.2, Androsov I.A.3, Denisov A.A.4
1PhD in Pharmaceutics, Senior Lecturer, Kursk State Medical University, 2PhD in Pharmaceutics, Professor, Kursk State Medical University, 3,4Student, Kursk State Medical University
DISTRIBUTION OF ALPHA-[3-[[2-(3.4-DIMETHOXYPHENYL)-ETHYL]-METHYLAMINO] PROPYL]-3.4-DIMETOXY-ALPHA-(1-METHYL-ETHYL) BENZOL ETHAN NITRILE IN THE ORGANISM OF WARM-BLOODED ANIMALS
Abstract
The article studies the distribution of alpha-[3-[[2-(3.4-dimethoxyphenyl)ethyl]-methylamino] propyl] -3.4-dimethoxy-alpha-(1-methylethyl) benzol ethan nitrile in the organism of omnivorous warm-blooded animals (rats) after intragastric infiltration of a half lethal dose of the poison agent. Isolation of alpha-[3-[[2-(3.4-dimethoxyphenyl)ethyl]-methyl-amino] propyl]-3.4-dimethoxy-alpha-(1-methylethyl) benzol ethan nitrile from organs, their contents and bio-fluids of the animals was conducted with the help of acetone. Purification of the extracted compound was carried out by chromatography on a column of “Silasorb S-18” 30 micrometers (eluent-ethan nitrile-water (9:1)). To identify and quantify the test compound, TLC, GC-MS, and UV spectro-photometry were used. The presence of the largest quantities of the tested substance is fixed in the stomach, its contents, liver and kidneys. The results obtained enable us to recommend these organs as the main objects of forensic and chemical analysis for finoptin poisoning.
Keywords: alpha-[3-[[2-(3.4-dimethoxyphenyl)ethyl]methylamino]-propyl]-3.4-dimethoxy-alpha- (1-methylethyl) benzol ethan nitrile (finoptin), distribution, forensic and chemical analysis.
Альфа-[3-[[2-(3,4-диметоксифенил)этил]метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрила гидрохлорид) (верапамил) (синонимы: верапамила хлоргидрат, ипровератрила гидрохлорид, 5-((3,4-диметоксифенетил)метиламино)-2-(3,4-диметокси-фенил)-2-изопропилвалеронитрила моногидрохлорид); торговые названия: изоптин, фаликард, финоптин, манидон, калан, кордилокс) – лекарственное вещество, проявляющее свойства антагониста ионов кальция. Он способен оказывать сосудорасширяющее, а также отрицательное инотропное действие, снижает потребность сердечной мышцы в кислороде, обладает недостаточно выраженным противоаритмическим эффектом [1, C. 411], [2, C. 1].
Гидрохлорид альфа-[3-[[2-(3,4-диметоксифенил)этил]метиламино]-пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрила имеет форму бесцветных кристаллов, плавящихся при 146оС и способных растворяться (мг/мл) в воде (83), а также ряде гидрофильных (метанол (более 100), этанол (более 100), пропанол-2 (4,6), пропиленгликоль (93), диметилформамид (более 100) и гидрофобных (дихлорметан (более 100), этилацетат (1,0), гексан (0,001)) органических растворителях [3, C. 568]. Растворимость верапамила-основания в воде – 4,47 мг/л [4, C. 1].
Рассматриваемое соединение относится к группе веществ достаточно токсичных для теплокровных животных и человека. ЛД50 альфа-[3-[[2-(3,4- диметоксифенил)этил]метиламино]пропил]-3,4-диметокси-альфа-(1-метил-этил) бензолацетонитрила гидрохлорида (в мг/кг) при пероральном введении лабораторным крысам составляет по разным данным 108, 150 или 341, мышам – 163, морским свинкам – 140, собакам – более 400, при введении в вену крысам – 16, мышам – 5,8 [2, C. 1], [5, C. 1].
LD50 альфа-[3-[[2-(3,4- диметоксифенил)этил]метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрила – основания для мышей при введении в вену – 8 мг/мл [4, C. 1].
В научных литературных источниках приводятся различные примеры отравления людей данным лекарственным средством, произошедших из-за его ошибочного приёма, превышения допустимых доз в ходе лечебных мероприятий или с суицидальными целями [6, C. 401], [10, C. 253].
Достаточно высокая токсичность альфа-[3-[[2-(3,4- диметоксифенил)этил]метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрила, его многоцелевое применение в медицинской практике, отмеченные случаи отравления с летальным исходом позволяют рассматривать данное лекарственное вещество в качестве важного объекта судебно- химического исследования [11, C. 50], [12, C. 167], [13, C. 21 ], [14, C. 32].
Для определения органов и биожидкостей - наиболее целесообразных объектов исследования при экспертизе случаев отравления - необходимо предварительное изучение на лабораторных животных особенностей распределения отравляющего вещества в организме теплокровных [15, C. 24], [16, C. 50].
Целью настоящей работы явилось изучение характера распределения альфа-[3-[[2-(3,4-диметоксифенил)этил]метиламино]-пропил]-3,4-ди-метокси-альфа-(1-метилэтил) бензолацетонитрила в организме всеядных теплокровных (крысы) при летальном отравлении.
Экспериментальная часть. Как объект исследования был рассмотрен альфа-[3-[[2-(3,4-диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрила гидрохлорид, отвечающий критериям НД 42-5047-01 и содержащий ≥ 99 % основного вещества.
В ходе экспериментов использовались крысы породы Wistar (возраст пять месяцев, масса – 230-245 г), из которых были сформированы 5 опытных групп и 1 контрольная, в каждую из которых входило по 5 особей. Животным опытных групп через пластмассовый зонд вводили рассматриваемое вещество в желудок в виде водной суспензии в количестве 341 мг на 1 кг массы крысы. После того, как животные погибали, их трупы подвергались вскрытию, одинаковые биологические объекты (органы или биожидкости), взятые от погибших особей внутри каждой из групп, объединяли и исследовали на наличие в них альфа-[3-[[2-(3,4- диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрила. Параллельно подобным образом исследовали органы и биожидкости животных контрольной группы.
Схема изолирования аналита из биоматриц. В каждом случае определённое количество измельченного (средние размеры частиц 0,2-0,4 см) паренхиматозного или полого органа, содержимого полого органа или биожидкости заливали количеством ацетона, в два раза (по массе) превышавшем количество биологического объекта. Смесь биоматериала с изолирующим агентом выдерживали в течение получаса, периодически перемешивая. По истечении указанного времени жидкую часть смеси (ацетоновое извлечение) отделяли от твёрдого остатка, а процесс настаивания повторяли в описанном выше режиме. Первое и второе ацетоновые извлечения сливали в одну выпарительную чашку, растворитель и остатки воды испаряли в токе воздуха (температурный интервал 18-22оС) до получения сухого остатка [17, C. 9], [18, C. 14].
Порядок очистка извлечённого аналита. Сухой остаток подвергали обработке 2-3 мл системы растворителей ацетонитрил-вода (9:1), получаемый раствор вносили в макроколонку сорбента «Силасорб С-18» 30 мкм (диаметр 10 мм, высота 150 мм). Аналит элюировали из колонки двухкомпонентным полярным элюентом ацетонитрил-вода (9:1). Фракции элюата, истекающего из макроколонки (по 2 мл каждая) собирали в градуированные пробирки. Серию фракций с 14 по 17 сливали в выпарительную чашку, а растворители удаляли из чашки, помещая её в поток воздуха комнатной температуры. После удаления растворителей остаток обрабатывали 5-7 мл этанола, количественно переносили в мерную колбу вместимостью 10 мл и доводили этанолом до метки (исходный раствор). В две фарфоровые выпарительные чашки (№ 1 и № 2) вносили по 1,0-4,5 мл исходного раствора и удаляли из него растворитель в потоке воздуха комнатной температуры.
Идентификация в тонком слое сорбента. Остаток, находящийся в чашке № 1, обрабатывали несколькими небольшим порциями этанола по 0,2-0,3 мл и количественно перенося раствор в виде полосы на линию старта хроматографической пластины «Сорбфил» ПТСХ-АФ-А-УФ. Рядом на линию старта наносили 5-10 мкл 0,04% раствора (в этаноле) вещества-свидетеля. Хроматографировали, используя элюент гексан-ацетон (2:8). Получаемые тонкослойные хроматограммы проявляли, облучая их УФ-светом с длиной волны 254 нм. Альфа-[3-[[2-(3,4- диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацето-нитрил, идентифицировали по величине Rf.
Идентификация и количественное определение с использованием УФ- спектрофотометрии. Часть хроматограммы с находящимся на ней пятном исследуемого вещества вырезали, вносили в градуированную пробирку вместимостью 10 мл и элюировали вещество из сорбента в течение 15 минут 5 или 10 мл этанола в режиме периодического перемешивания. Полученный этанольный элюат отделяли в кварцевую кювету с длиной оптического пути 10 мм и проводили исследование его светопоглощения в диапазоне длин волн от 200 до 400 нм на спектрофотометре модели СФ-2000. Если оптическая плотность элюата превыщала 1,4, его разбавляли этанолом.
Принимая во внимание оптическую плотность этанольного элюата, измерения которой проводили в области 282 нм, определяли количественное содержание альфа-[3-[[2-(3,4- диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил)бензолацето-нитрила спектрофотометрическим методом.
Идентификация методом ГХ-МС. Сухой остаток, находящийся в выпарительной чашке № 2 обрабатывали 2 мл трихлорметана. 4 мкл, взятые из полученного раствора, вводили в хроматограф фирмы Agilent Technologies (США) модели 6890N с масс-селективным квадрупольным детектором модели 5973N (Agilent Technologies). Процесс хроматографирования осуществляли в колонке DB-1MS (J&WScientific, США) с неподвижной жидкой фазой диметилполисилоксан (длина колонки 30 м, внутренний диаметр 0,25 мм, толщина пленки фазы 0,25 мкм).
Начальная температура термостата колонки составляла 80°С (задержка на 2 минуту). Температура программировалась от 80°С до 250°С со скоростью 40°С в минуту с выдержкой при конечной температуре 6 минут. Температура инжектора составляла 280°С, температура интерфейса – 300°С. В качестве газа-носителя использовался гелий. Подача газа-носителя производилась со скоростью 39 см/с. Проба вводилась в режиме без деления потока, задержка 3 мин. Фрагментация молекул аналита в ионизационной камере осуществлялась с использованием электронного удара (70 эВ). Обнаружение вещества проводилось в режиме регистрации по полному ионному току (диапазон сканирования 40-550 m/z). Анализируемое соединение идентифицировали как по значению времени удерживания, так и по совпадению его масс-спектра с масс-спектром стандарта на 86% и более.
Результаты и их обсуждение. При идентификации в тонком слое сорбента альфа-[3-[[2-(3,4- диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрил проявлялся на хроматограммах в УФ-свете в виде темных розово-фиолетовых пятен на более светлом общем фоне пластины. Анализируемое вещество идентифицировали на основе совпадения значения его абсолютной хроматограической подвижности (Rf) в тонком слое силикагеля со значением Rf вещества-стандарта (038±0,03).
По результатам идентификации альфа-[3-[[2-(3,4- диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил)бензолацетонитрила методом УФ-спектрофотометрии отмечается совпадение формы спектральных кривых аналита, извлечённого из биоматриц, а также положения в них максимумов (при 205 и 232 и 282 нм) с этими же характеристиками вещества-стандарта.
Градуировочный график линейной зависимости оптической плотности этанольных растворов альфа-[3-[[2-(3,4-диметоксифенил)этил]-метиламино]про-пил]-3,4-диметокси-альфа-(1-метилэтил)бензолацето-нитрила от концентрации в них аналита (5,00-120,00 мкг/мл) для спектрофотометрического определения может быть описан уравнением прямой:. А = 0,010202∙С-0,001794, в котором переменные А и С – орсоответственно значения оптической плотности и концентрации анализируемого вещества в фотометрируемом растворе (мкг/мл). Коэффициент корреляции > 0,99.
Относительная ошибка среднего результата при определении альфа-[3-[[2-(3,4-диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрила данной методикой в субстанции не превышает 1,0 % (при шести параллельных опытах и доверительной вероятности 0,95).
При исследовании извлечений из биоматриц, взятых от крыс, не получавших альфа-[3-[[2-(3,4-диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил)бензолацетонитрил, установлено отсутствие данного вещества в паренхиматозных и полых органах, их содержимом, а также в крови животных контрольной серии. Измеренное при длине волн 282 нм фоновое поглощение элюатов из участков хроматограмм, по площади и положению относительно линии старта соответствующих анализируемому веществу, не превышало 0,024 единиц оптической плотности для различных биологических объектов в пересчёте на 5 г биоматериала.
На рис. 1 представлен внешний вид газо-жидкостных хроматограмм исследуемого аналита, выделенного из некоторых биоматриц (желудок (А) и печень(Б)), а также вид хроматограммы вещества-стандарта (В).
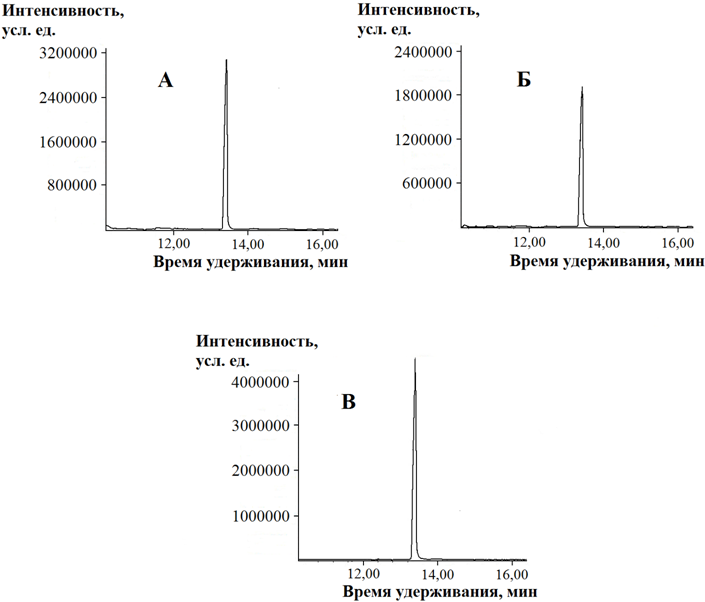
Рис. 1 – Газо-жидкостные хроматограммы исследуемого аналита: выделенного из желудка (А), выделенного из печени (Б), вещества-стандарта (В)
Данные, приводимые на рисунке, позволяют заключить, что в предложенных условиях проведения идентификации сочетанием ГЖХ и масс-селективного детектирования значение времени удерживания альфа-[3-[[2-(3,4-диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацетонитрила, извлечённого из биоматериала, совпадало с таковым вещества-стандарта и соответствовало интервалу 13,4±0,14 минуты.
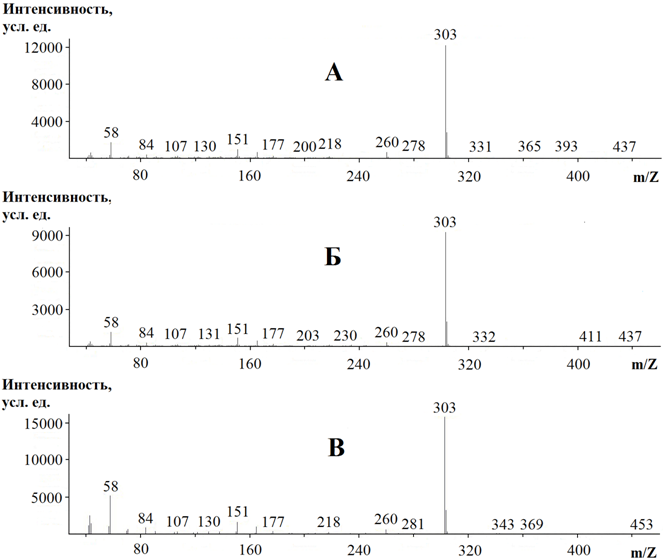
Рис. 2 – Масс-спектры исследуемого аналита: извлечённого из желудка (А), извлечённого из печени (Б), вещества-стандарта (В)
При сравнении хроматограмм исследуемого соединения с хроматограммой вещества-стандарта (метод ГХ-МС) не наблюдалось присутствие дополнительных пиков и заметного смещения базовой линии в зоне, соответствующей промежутку значений времени удерживания 12,5-14,5 мин.
В масс-спектрах исследуемого вещества, извлечённого из биологических объектов (желудок и печень), взятых от отравленных животных, присутствовали сигналы характерных осколков (заряженных частиц) для молекулы альфа-[3-[[2-(3,4- диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацето-нитрила с массами (m/Z): 58, 84, 107, 130, 151, 177, 260, 303. Основным (масса которого принимается за 100%) является осколок с массой 303 (см. рис. 2).
Результаты определения рассматриваемого соединения в 10 биологических объектах (паренхиматозных органах, полых органах и их содержимом, биожидкостях), взятых от трупов отравленных животных, представлены в таблице.
Таблица 1 – Результаты изучения распределения альфа-[3-[[2-(3,4- диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-ме-тилэтил) бензолацетонитрила в организме теплокровных (крысы)
| Орган или биожидкость | Масса органов (суммарная для 5 особей), взятая для ис-следования, г | Найдено верапамила | Метрологи-ческие характеристики | |
| мг в исследуе-мой массе биологического объекта | мг в 100 г биологичес-кого объекта | |||
| Почки | 6,28 6,67 6,55 6,92 6,49 | 11,299 10,947 13,112 13,286 10,361 | 179,914 164,127 200,181 191,994 159,643 | x= 179,172 S = 17,422 Sx = 7,791 ∆x= 21,660 ε= 12,09 |
| Печень | 8,33 8,33 8,33 8,33 8,33 | 22,042 18,024 20,033 21,026 19,565 | 264,615 216,374 240,493 252,411 234,871 | x= 241,753 S = 18,230 Sx = 8,153 ∆x= 22,664 ε= 9,37 |
| Сердце | 3,54 3,71 3,33 3,05 3,26 | 0,141 0,151 0,123 0,107 0,124 | 3,991 4,076 3,694 3,513 3,795 | x= 3,814 S = 0,227 Sx = 0,101 ∆x= 0,282 ε= 7,39 |
| Лёгкие | 8,33 8,33 8,33 8,33 8,33 | 3,782 3,407 3,603 3,912 3,294 | 45,398 40,896 43,254 46,963 39,541 | x= 43,210 S = 3,070 Sx = 1,373 ∆x= 3,816 ε= 8,83 |
| Кровь | 8,33 8,33 8,33 8,33 8,33 | 0,954 0,994 0,854 0,906 0,924 | 11,449 11,933 10,251 10,873 11,095 | x= 11,120 S = 0,630 Sx = 0,282 ∆x= 0,783 ε= 7,04 |
| Тонкий кишечник с содержимым | 8,33 8,33 8,33 8,33 8,33 | 10,116 11,100 10,672 9,621 9,132 | 121,438 133,248 128,117 115,493 109,628 | x= 121,585 S = 9,471 Sx = 4,236 ∆x= 11,775 ε= 9,68 |
| Желудок | 8,33 8,33 8,33 8,33 8,33 | 43,743 41,510 42,712 44,947 40,478 | 525,121 498,324 512,751 539,582 485,928 | x= 512,341 S = 21,211 Sx = 9,486 ∆x= 26,371 ε= 5,15 |
| Содержимое желудка | 8,33 8,33 8,33 8,33 8,33 | 76,235 89,290 79,336 66,711 78,000 | 915,181 1071,909 952,413 800,849 936,379 | x= 935,346 S= 96,744 Sx= 43,265 ∆x= 120,278 ε= 12,86 |
| Мышцы | 8,33 8,33 8,33 8,33 8,33 | 4,582 4,997 4,679 4,360 4,818 | 55,002 59,987 56,167 52,335 57,836 | x= 56,265 S = 2,888 Sx = 1,292 ∆x= 3,591 ε= 6,38 |
| Селезёнка | 3,01 2,64 3,38 3,14 3,50 | 3,857 3,701 5,010 3,933 4,786 | 128,139 140,184 148,239 125,253 136,745 | x= 135,712 S = 9,283 Sx = 4,152 ∆x= 11,542 ε= 8,50 |
Как видно из таблицы, альфа-[3-[[2-(3,4- диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолаце-тонитрил присутствует в неизменном виде как в органах, так и в крови погибших организмов. Наибольшие количества отравляющего вещества (мг в 100 г органа или биожидкости) обнаруживаются в желудке (512,341±26,371) и его содержимом (935,346±120,278), печени (241,753±22,664) почках (179,172±21,660) и селезёнке (135,712±11,542) несколько меньшие – в тонком кишечнике с содержимым (121,585±11,775), в мышцах (56,265±3,591) и лёгких (43,210±3,816) отравленных животных.
Выводы. Изучено распределение альфа-[3-[[2-(3,4-диметоксифенил)-этил]метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил) бензолацето-нитрила в организме теплокровных животных (крысы) при введении LD50 данного отравляющего вещества в желудок.
Показано, что отравляющий агент обнаруживается в значительных количествах в трупах погибших от отравления крыс в неизменном виде.
Наибольшие количества альфа-[3-[[2-(3,4-диметоксифенил)этил]-метиламино]пропил]-3,4-диметокси-альфа-(1-метилэтил)бензолацето-нитрила присутствуют в желудке (512,341±26,371), его содержимом (935,346±120,278), печени (241,753±22,664) и почках (179,172±21,660).
Список литературы / References
- Машковский М.Д. Лекарственные средства. В 2 т. Т. 1. / М.Д. Машковский. – 16-е изд. – М.: Новая волна, 2014. – 540 с.
- Verapamil Hydrochloride Injection. – URL: https://system.netsuite.com/core/media/media.nl?id=12072&c=723462&h=1ca152815ad524204649&_xt=.pdf (аccessed: 13.06.2017).
- O'Neil M.J. (ed.). The Merck Index - An Encyclopedia of Chemicals, Drugs, and Biologicals. 13th Edition, Whitehouse Station. – N.J.: Merck and Co., Inc., 2001. – 1772 р.
- Verapamil: DrugBank. – URL: https://www.drugbank.ca/drugs/DB00661 (аccessed: 13.06.2017).
- Verapamil Hydrochloride MSDS. – URL: www.sciencelab.com/msds.php?msdsId=9925411 (аccessed: 13.06.2017).
- Clarke's analysis of drugs and poisonsin Pharmaceuticals, body fluids and postmortem material. 3rd ed.- London: Pharmaceutical Press, 2004.- Vol. 2.- 550 p.
- MacDonald D. Case report: fatal overdose with sustained-release verapamil / D. MacDonald, P.C. Alguire // Am. J. Med. Sci. – 1992– Vol. 303, N 2– Р. 115-117.
- Calcium channel blocker sustained release: Only three tablets can be life threatening / M. Mihalcea, A. Geiger, J. Kopferschmitt and others // Journal of Emergencies, Trauma, and Shock. – 2012. – Vol. 5, N 2– Р. 208-209.
- Gelbke H.P. Fatal poisoning with verapamil / H.P. Gelbke, H.J. Schlicht, Gg. Schmidt // Archives of Toxicology. – 1977. – Vol. 37, N 2. – Р. 89–94.
- Critical care management of verapamil and diltiazem overdose with a focus on vasopressors: a 25-year experience at a single center / M. Levine, S.C. Curry, A. Padilla-Jones and others // Ann Emerg Med. – 2013. – Vol. 62, N 3.– Р. 252-258.
- Карташов В.А. Сравнительная характеристика способов изолирования верапамила из биологического материала / В.А. Карташов, Л.Е. Кудрикова // Фармация. – 1988. – № 3. – С. 49-52.
- Кормишин В.А. Денситометрический анализ эфедрина и верапамила в судебно-химической экспертизе / В.А. Кормишин, А.В. Воронин, И.Ф. Шаталаев // Вестник СамГУ – Естественнонаучная серия. – 2013. – № 6. – С. 167-174.
- Муравьева Г.М. Судебно-химическое определение курантила и верапамила / Г.М. Муравьева, М.И. Дмитриченко // Судебно-медицинская экспертиза. – 1995. – Т. 38, № 1. – С. 21-23.
- Кормишин В.А. Денситометрический анализ верапамила в судебно- химической экспертизе / В.А. Кормишин, А.В. Воронин, И.Ф.Шаталаев // Технические науки - от теории к практике: сборник статей по материалам VI международной научно-практической конференции. – Новосибирск: СибАК, 2012.-С. 31-35.
- Шорманов В.К. Распределение карбосульфана в организме теплокровных животных / В.К. Шорманов, С.Г. Галушкин, А.П. Терских // Судебно-медицинская экспертиза. – 2015. – Т. 58, № 5. – С. 23-29.
- Шорманов В.К. Распределение амлодипина в организме теплокровных животных / В.К. Шорманов, Л.Л. Квачахия // Судебно-медицинская экспертиза. – 2017. – Т. 60, № 1. – С. 48-53.
- Квачахия Л.Л. Выявление верапамила в биологических жидкостях / Л.Л. Квачахия, В.К. Шорманов // Фармация. – 2015. – Т. 64, № 2. – С. 8-13.
- Квачахия Л.Л. Определение нимодипина в биологическом материале / Л.Л. Квачахия, В.К. Шорманов, Г.С. Мещерякова // Фармация.-2016. – Т. 65, № 6. – С. 12-15.
Список литературы на английском языке / References in English
- Mashkovskii M.D. Lekarstvennyie sredstva [Drugs]. In 2 t. V. 1 / M.D. Mashkovskii. – 16nd ed. – M.: Novaya volna [New wave]. 2014. – 540 p. [in Russian]
- Verapamil Hydrochloride Injection. – URL: https://system.netsuite.com/core/media/media.nl?id=12072&c=723462&h=1ca152815ad524204649&_xt=.pdf (аccessed: 13.06.2017).
- O'Neil M.J. (ed.). The Merck Index - An Encyclopedia of Chemicals, Drugs, and Biologicals. 13th Edition, Whitehouse Station. – N.J.: Merck and Co., Inc., 2001. – 1772 р.
- Verapamil: DrugBank. – URL: https://www.drugbank.ca/drugs/DB00661 (аccessed: 13.06.2017).
- Verapamil Hydrochloride MSDS. – URL: www.sciencelab.com/msds.php?msdsId=9925411 (аccessed: 13.06.2017).
- Clarke's analysis of drugs and poisonsin Pharmaceuticals, body fluids and postmortem material. 3rd ed. – London: Pharmaceutical Press, 2004. – Vol. 2. – 550 p.
- MacDonald D. Case report: fatal overdose with sustained-release verapamil / D. MacDonald, P.C. Alguire // Am. J. Med. Sci. – 1992. – Vol. 303, N 2. – Р. 115-117.
- Calcium channel blocker sustained release: Only three tablets can be life threatening / M. Mihalcea, A. Geiger, J. Kopferschmitt and others // Journal of Emergencies, Trauma, and Shock. – 2012. – Vol. 5, N 2. – Р. 208-209.
- Gelbke H.P. Fatal poisoning with verapamil / H.P. Gelbke, H.J. Schlicht, Gg. Schmidt // Archives of Toxicology. – 1977. – Vol. 37, N 2. – Р. 89–94.
- Critical care management of verapamil and diltiazem overdose with a focus on vasopressors: a 25-year experience at a single center / M. Levine, S.C. Curry, A. Padilla-Jones and others // Ann Emerg Med. – 2013. – Vol. 62, N 3. – Р. 252-258.
- Kartashov V.A. Sravnitel'naya kharakteristika sposobov izolirovaniya verapamila iz biologicheskogo materiala [Comparative characteristics of methods for isolating verapamil from biological material] / V.A. Kartashov, L.Ye. Kudrikova // Farmatsiya [Рharmacy]. – 1988. – № 3. – S. 49-52. [in Russian]
- Kormishin V.A. Densitometricheskiy analiz efedrina i verapamila v sudebno-khimicheskoy ekspertize [Densitometric analysis of ephedrine and verapamil in forensic chemical examination] / V.A. Kormishin, A.V. Voronin, I.F. Shatalayev // Vestnik SamGU – Yestestvennonauchnaya seriya [Bulletin of the Samara state University – natural Science series]. – 2013. – № 6. – P. 167-174. [in Russian]
- Muraveva G.M. Sudebno-khimicheskoye opredeleniye kurantila i verapamila [Forensic and chemical definition of curantyl and verapamil] / G.M. Muraveva, M.I. Dmitrichenko // Sudebno-meditsinskaya ekspertiza [A forensic examination]. – 1995. – V. 38, № 1. – P. 21-23. [in Russian]
- Kormishin V.A. Densitometricheskiy analiz verapamila v sudebno- khimicheskoy ekspertize [Densitometric analysis of verapamil in forensic chemical examination] / V.A. Kormishin, A.V. Voronin, I.F. Shatalaev // Tekhnicheskiye nauki - ot teorii k praktike: sb. st. po mater. VI mezhdunar. nauch.-prakt. konf. [Technical science - from theory to practice: proceedings of the VI international scientific-practical conference]. – Novosibirsk: SibAK, 2012. – P. 31-35. [in Russian]
- Shormanov V.K. Raspredeleniye karbosul'fana v organizme teplokrovnykh zhivotnykh [Distribution of carbosulfan in the body of warm-blooded animals] / V.K. Shormanov, S.G. Galushkin, A.P. Terskih // Sudebno-meditsinskaya ekspertiza [A forensic examination]. – 2015. – V. 58, № 5. – P. 23-29. [in Russian]
- Shormanov V.K. Raspredeleniye amlodipina v organizme teplokrovnykh zhivotnykh [Distribution of amlodipine in the body of warm-blooded animals] / V.K. Shormanov, L.L. Kvachakhiya // Sudebno-meditsinskaya ekspertiza [A forensic examination]. – 2017. – V. 60, № 1. – P. 48-53. [in Russian]
- Kvachakhiya L.L. Vyyavleniye verapamila v biologicheskikh zhidkostyakh [Detection of verapamil in biological fluids] / L.L. Kvachakhiya, V.K. Shormanov // Farmatsiya [Рharmacy]. – 2015. – V. 64, № 2. – P. 8-13. [in Russian]
- Kvachakhiya L.L. Opredeleniye nimodipina v biologicheskom materiale [Determination of nimodipine in biological material] / L.L. Kvachakhiya, V.K. Shormanov, G.S. Meshcheryakova // Farmatsiya [Рharmacy].-2016. – V. 65, № 6. – P. 12-15. [in Russian]
