АНТИОКСИДАНТНЫЙ И АНТИАМИЛОИДНЫЙ ПОТЕНЦИАЛ ПРОИЗВОДНЫХ ЯНТАРНОЙ КИСЛОТЫ
АНТИОКСИДАНТНЫЙ И АНТИАМИЛОИДНЫЙ ПОТЕНЦИАЛ ПРОИЗВОДНЫХ ЯНТАРНОЙ КИСЛОТЫ
Научная статья
Поздняков Д.И.1, *, Мамлеев А.В.2, Ладыка А.А.3, Рыбалко И.Е.4, Ларский М.В.5
1 ORCID:0000-0003-0889-7855;
1, 2, 3, 4, 5 Пятигорский медико-фармацевтический институт, Пятигорск, Россия
* Корреспондирующий автор (pozdniackow.dmitry[at]yandex.ru)
АннотацияДанное исследование посвящено изучению влияния янтарной, ацетиламиноянтарной кислот и этилметилгидроксипиридина сукцината на процесс генерации супероксид-радикала и образование конгломератов амилоида β в in vitro тестах. Влияние изучаемых соединений на образование супероксид-радикала оценивали в реакции фотообращения рибофлавина. Агрегацию амилоидных частиц регистрировали в реакции с конго красным. В результате было установлено, что в ряду изучаемых веществ наиболее высокие супероксид-радикал «скэвенджерные» свойства отмечены у ацетиламиноянтарной кислоты (IC50 109,3±12,947 мкг/мл), кроме того, данное соединение существенно ингибировало процесс агрегации амилоида β.
Ключевые слова: сукцинаты, болезнь Альцгеймера, окислительный стресс, амилоид β.
ANTIOXIDANT AND ANTIAMYLOID POTENTIAL OF SUCCINIC ACID DERIVATIVES
Research article
Pozdnyakov D.I.1, *, Mamleev A.V.2, Ladyka A.A.3, Rybalko I.E.4, Larsky M.V.5
1 ORCID ID:0000-0003-0889-7855;
1, 2, 3, 4, 5 Pyatigorsk Medical and Pharmaceutical Institute, Pyatigorsk, Russia
* Corresponding author (pozdniackow.dmitry[at]yandex.ru)
AbstractThis study aims to examine the effect of succinic acid, acetylaminosuccinic acid, and Ethylmethylhydroxypyridine succinate on the generation of superoxide radicals and the formation of amyloid β conglomerates during in vitro tests. The effect of the examined compounds on the formation of a superoxide radical was evaluated in the riboflavin photochemical reaction. Amyloid deposits were detected in the reaction with Congo red. As a result, it was found that among the studied substances, the highest superoxide-radical "scavenger" properties were observed in acetylaminosuccinic acid (IC50 109.3±12.947 µg/ml), in addition, this compound significantly inhibited the aggregation process of amyloid β.
Keywords: succinates, Alzheimer's disease, oxidative stress, amyloid β.
ВведениеСреди заболеваний, вызванных техническим прогрессом, одно из первых мест занимает деменция и сопряженные с ней нейродегенеративные заболевания. Особо значимое распространение когнитивных нарушений наблюдается среди населения Азиатско-Тихоокеанского региона. Это объясняется сочетанием ряда социально-экономических причин и высокого профиля сосудистого риска [1]. Симптомокомплекс деменции представляет собой нарушение интеллектуальной деятельности, снижение доступного уровня суждений, нивелирование индивидуальных особенностей личности, изменение поведения вследствие нейродегенеративных нарушений, в частности болезни Альцгеймера [2]. Согласно статистике, количество пациентов с болезнью Альцгеймера за 26-ти летний период (с 1990 по 2016 год) увеличилось с 20,2 млн до 43,8 млн человек. За данный временной промежуток число смертей в результате деменции возросло на 148%. В этой связи деменция считается пятой по распространённости причиной смертности в мире, а среди людей старше 70 лет — второй после ишемической болезни сердца [3].
Последние исследования показывают, что одной из причин развития деменции и болезни Альцгеймера является нарушение функциональной активности митохондрий – митохондриальная дисфункция, сопровождающаяся генерацией активных форм кислорода, представленных, как правило, супероксид-радикалом. В свою очередь супероксид-радикал запускает каскад реакций, приводящий к активации секретазного комплекса с расщеплением белка-предшественника амилоида и образованием фрагментов амилоида β различной длины [4]. В настоящее время было установлено, что амилоид β и связанный с ним гиперфосфорилированный тау-протеин обладают выраженной нейротоксичностью и являются основными компонентами сенильных бляшек. Таким образом, можно предположить, что подавление оксидативного стресса и амилоидогенеза являются перспективными направлениями терапии деменции и болезни Альцгеймера [5].
Широко распространенными веществами, оказывающими антиоксидантное действие, являются производные янтарной кислоты. Также для сукцинатов описано «шунтирующее» действие в отношении митохондриального комплекса I – основного источника активных форм кислорода в клетке, что делает данные соединения перспективными объектами для оценки антиамилоидного действия [6].
Методы и принципы исследования
В данном исследовании в качестве изучаемых объектов выступали ацетиламиноянтарная кислота («Когитум», Санофи), этилметилгидроксипиридина сукцинат («Мексидол», Фармасофт) и янтарная кислота («Татхимфармпрепараты»). Работа была выполнена с применением in vitro подхода с изучением влияния исследуемых объектов на процесс агрегации частиц бета-амилоида и генерацию супероксид-радикала в модельной смеси.
Влияние ацетиламиноянтарной кислоты, этилметилгидроксипиридина сукцината и янтарной кислоты на процесс агрегации Aβ оценивали спектрофотометрически в реакции с конго красным. Изучаемые соединения растворяли в диметилсульфоксиде до конечной концентрации 20 мг/мл. 25 мкл полученного раствора смешивали с 225 мкл 20 мМ раствора конго красного. После чего полученную смесь инкубировали в течении девяти дней при комнатной температуре. Оптическую плотность модельной смеси оценивали на третий, шестой и девятый день при 405 нм и 540 нм. Количество образовавшихся агрегатов Aβ рассчитывали по формуле:
где:
ACR405 - оптическая плотность раствора конго красного при длине волны 405 нм;
A540 и A405 оптическая плотность раствора, содержащего исследуемые вещества при длине волны 540 нм и 405 нм, соответственно. Фрагмент Aβ1-40 был получен от Sigma-Aldrich (Германия) [7].
Оценку супероксид-антирадикальной активности проводили по методу Winterbourn. Супероксид-радикал генерировали в реакции фотообращения рибофлавина. Среда инкубации состояла из 0,1 мл раствора изучаемого соединения (в конечной концентрации 1000 мкг/мл; 500 мкг/мл; 250 мкг/мл; 125 мкг/мл и 62,5 мкг/мл) с добавлением 0,1 мл 1,5мМ раствора нитро-синего тетразолия; 0,2 мл 0,1М раствора ЭДТА; 0,05 мл 0,12 мМ раствора рибофлавина и 2,55 мл PBS (pH 7,4). Полученную смесь инкубировали 5 мин при 250С. Оптическую плотность проб измеряли при 560 нм против воздуха. Положительным контролем выступала среда инкубации без добавления исследуемых веществ. Все тесты выполнялись в триплетном варианте. Процент ингибиции рассчитывали по формуле [8]:
где:
Ах – оптическая плотность пробы образца
А0 - оптическая плотность пробы положительного контроля
Статистическую обработку полученных результатов проводили с применением программного пакет STATISTICA 6.0 (StatSoft, США). Данные выражали в виде M (среднее значение) ± SEM (стандартная ошибка среднего). Статистические отличия между группами оценивали методом однофакторного дисперсионного анализа с пост тестом Ньюмена-Кейсла при p<0,05. Показатель IC50 рассчитывали методом пробит анализа.
Основные результаты
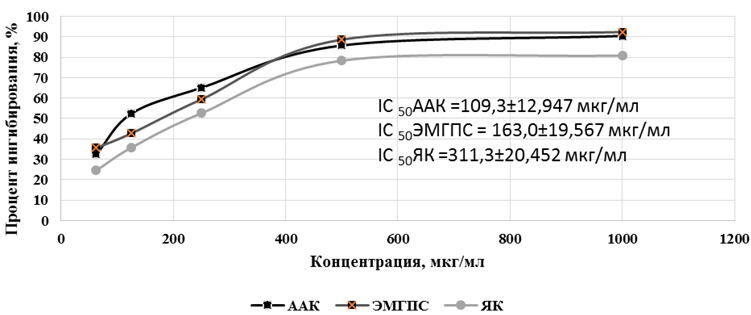
В ходе проведения данного исследования было установлено, что наиболее выраженными супероксид-антирадикальными свойствами обладает ацетиламиноянтарная кислота, которая в концентрации 1000 мкг/мл ингибировала образование супероксид-радикала в модельной смеси на 90,5% при показателе IC50 109,3±12,947 мкг/мл (см. рисунок 1). Этилметилгидроксипиридина сукцинат также значимо подавлял генерацию супероксида (на 92,4% в максимальной тестируемой концентрации), однако величина IC50 этилметилгидроксипиридина сукцината была выше таковой у ацетиламиноянтарной кислоты и составляла 163,0±19,567 мкг/мл. Внесение в модельную среду янтарной кислоты в концентрации 1000 мкг/мл способствовало снижению степени образования супероксид-радикала на 80,6%, при этом показатель IC50 составил 311,3±20,452 мкг/мл (см. рисунок 1).
Рис. 1 – Результаты оценки супероксид-антирадикальной активности исследуемых соединений
Примечание: ААК – ацетиламиноянтарная кислота; ЭМГПС – этилметилгидроксипиридина сукцинат; ЯК – янтарная кислота; IC50 – коэффициент полуингибиции
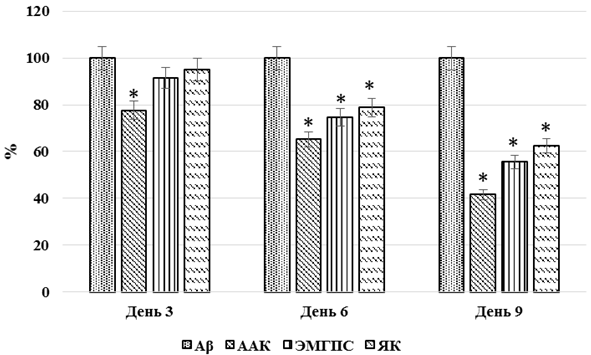
В ходе оценки влияния изучаемых веществ на процесс агрегации амилоидных частиц было установлено, что наиболее значимо данный процесс ингибировало добавление в анализируемую среду ацетиламиноянтарной кислоты. При этом процент ингибирования составил на 3-й, 6-й и 9-й день эксперимента 22,4% (p<0,05); 34,8 % (p<0,05) и 58,4% (p<0,05) соответственно. Следует отметить, что этилметилгидроксипиридина сукцинат и янтарная кислота значимого влияния на агрегацию Aβ через 3 дня инкубации не оказали. На 6-й день исследования добавление в модельную смесь этилметилгидроксипиридина сукцината и янтарной кислоты способствовало уменьшению агрегации амилоидных частиц на 25,4% (p<0,05) и 44,4% (p<0,05) соответственно, в то время как на 9-й день эксперимента степень ингибирования составила 25,1% (p<0,05) и 37,6% (p<0,05) соответственно (см. рисунок 2).
Рис. 2 – Влияние исследуемых соединений на агрегацию амилоидных частиц in vitro в реакции с конго красным
Примечание: Aβ – модельная среда без добавления исследуемых соединений; ААК – ацетиламиноянтарная кислота; ЭМГПС – этилметилгидроксипиридина сукцинат; ЯК – янтарная кислота; * - статистически значимо относительно Aβ (p<0,05, критерий Ньюмена-Кейсла)
Обсуждение
Процесс образование сенильных включений Aβ является одной из значимых составляющих патогенеза нейродегенеративных заболеваний, включая болезнь Альцгеймера. В свою очередь, активация секретаз и последующее расщепление белка предшественника амилоида с образованием патологичных форм Aβ непосредственно связано с генерацией активных форм кислорода, в частности, супероксид-радикала [9]. Таким образом, можно предположить, что средства антиоксидантного действия, к которым относятся этилметилгидроксипиридина сукцинат, ацетиламиноянтарная и янтарная кислоты, способны предотвратить агрегацию амилоидных частиц посредством эффективного «скэвенджинга» активных форм кислорода. Данное исследование показало, что ацетиламиноянтарная кислота в большей степени, этилметилгидроксипиридина сукцинат и янтарная кислота в меньшей степени способны подавлять генерацию супероксид-радикала в реакции фотообращения рибофлавина. В то же время ацетиламиноянтарная кислота более значимо (по сравнению с остальными изучаемыми соединениями) ингибировала агрегацию Aβ с развитием эффекта уже на третий день эксперимента и последующим его увеличением к девятому дню исследования. Этилметилгидроксипиридина сукцинат и янтарная кислота также угнетали агрегацию амилоидных частиц, но только начиная с шестого дня инкубации.
Заключение
Проведенное исследование показало, что этилметилгидроксипиридина сукцинат, ацетиламиноянтарная и янтарная кислоты способны in vitro подавлять образование амилоидных бляшек и ингибировать образование супероксид-радикала, что делает данные соединения перспективными для дальнейшего изучения на предмет возможности использования в качестве средств патогенетической терапии нейродегенеративных заболеваний.
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Alzheimer's Association. Alzheimer's disease facts and figures // Alzheimers Dement. 2016. – Vol.12(4). - P. 459-509. 2016 doi: 10.1016/j.jalz.2016.03.001.
- Lyketsos C.G. Neuropsychiatric symptoms in Alzheimer's disease / C.G. Lyketsos, M.C. Carrillo, J.M.Ryan, A.S. Khachaturian, P. Trzepacz, J. Amatniek, J. Cedarbaum, R. Brashear, D.S. Miller // Alzheimers Dement. – 2011.- Vol. - 7(5).- P.532-9. doi: 10.1016/j.jalz.2011.05.2410.
- Sancesario G. M. Alzheimer's disease in the omics era / G.M. Sancesario, S. Bernardini // Clin Biochem. – 2018. – Vol.59.- P.9-16. doi: 10.1016/j.clinbiochem.2018.06.011
- Cubinkova V. Alternative hypotheses related to Alzheimer's disease / V. Cubinkova, B. Valachova, I. Uhrinova, V. Brezovakova, T. Smolek, S. Jadhav, N. Zilka // Bratisl Lek Listy. – 2018.- Vol.119(4).- P.210-216. doi: 10.4149/BLL_2018_039.
- Polito C. A. Association of Tea Consumption with Risk of Alzheimer's Disease and Anti-Beta-Amyloid Effects of Tea / C.A. Polito, Z.Y. Cai, Y.L. Shi, X.M. Li, R. Yang, M. Shi, Q.S. Li, S.C. Ma, L.P. Xiang, K.R. Wang, J.H. Ye, J.L. Lu, X.Q. Zheng, Y.R. Liang // Nutrients. – 2018. –Vol. 10(5).- P.655. doi: 10.3390/nu10050655.
- Nowak G. Succinate ameliorates energy deficits and prevents dysfunction of complex I in injured renal proximal tubular cells / G. Nowak, G.L. Clifton, D. Bakajsova // J Pharmacol Exp Ther. – 2008.- Vol.324(3).- P.1155–1162. doi:10.1124/jpet.107.130872.
- Wang W.Inhibition of amyloid peptide fibril formation by gold-sulfur complexes / W. Wang, C. Zhao, D. Zhu, G. Gong, W. Du // J Inorg Biochem. – 2017.- Vol.171.- P.1-9.doi:10.1016/j.jinorgbio.2017.02.021
- Winterbourn C. C. The estimation of red cell superoxide dismutase activity / C.C. Winterbourn, R.E. Hawkins, M. Brian, R.W. Carrell // J Lab Clin Med.- 1975.- Vol.85.- P.337–41.
- Han F. Beta-amyloid accumulation in neurovascular units following brain embolism / F. Han, K. Fukunaga // J Pharmacol Sci. – 2009.- Vol.111(2).- P.101-9. doi: 10.1254/jphs.09r02cp.