АКТУАЛЬНОСТЬ ОПРЕДЕЛЕНИЯ ПРОИЗВОДНЫХ БАРБИТУРОВОЙ КИСЛОТЫ ПРИ ХИМИКО-ТОКСИКОЛОГИЧЕСКОМ АНАЛИЗЕ НА ПРИМЕРЕ ЦИКЛОБАРБИТАЛА
АКТУАЛЬНОСТЬ ОПРЕДЕЛЕНИЯ ПРОИЗВОДНЫХ БАРБИТУРОВОЙ КИСЛОТЫ ПРИ ХИМИКО-ТОКСИКОЛОГИЧЕСКОМ АНАЛИЗЕ НА ПРИМЕРЕ ЦИКЛОБАРБИТАЛА
Научная статья
Петрова О.С.1, *, Матвеева Л.В.2, Сухова Н.А.3
1 ORCID: 0000-0002-4458-7953,
1 Новгородский государственный университет имени Ярослава Мудрого, Великий Новгород, Россия;
2, 3 Новгородское бюро судебно-медицинской экспертизы, Великий Новгород, Россия
* Корреспондирующий автор (yalome[at]mail.ru)
АннотацияСохраняется актуальность химико-токсикологического анализа на производные барбитуровой кислоты, так как отравления ими встречаются нередко, и в смеси с другими токсикологически важными препаратами [4], [5], [6]. Основу экспертной оценки отравления производными барбитуровой кислоты составляет качественное определение препарата в организме человека с учетом обстоятельств дела и клинической картины отравления, однако имеется возможность количественной оценки обнаруженных препаратов и их метаболитов. С целью улучшения диагностики отравления производными барбитуровой кислоты составлена и оптимизирована четкая схема химико-токсикологического анализа при судебно-химических экспертных исследованиях биообъектов.
Ключевые слова: производные барбитуровой кислоты, химико-токсикологический анализ.
RELEVANCE OF DETERMINATION OF BARBITURIC ACID DERIVATIVES BY CHEMICAL AND TOXICOLOGICAL ANALYSIS ON EXAMPLE OF CYCLOBARBITAL
Research article
Petrova O.S.1, *, Matveeva L.V.2, Sukhova N.A.3
1 ORCID: 0000-0002-4458-7953,
1 Yaroslav-the-Wise Novgorod State University, Velikiy Novgorod, Russia;
2, 3 Novgorod Forensic Bureau, Velikiy Novgorod, Russia
* Corresponding author (yalome[at]mail.ru)
AbstractThe relevance of the chemical and toxicological analysis for derivatives of barbituric acid are due to common poisoning with these substances and in a mixture with other toxicologically important drugs [4], [5], [6]. The basis of the expert assessment of poisoning with derivatives of barbituric acid is a qualitative determination of the drug in the human body, considering the circumstances of the case and the clinical picture of poisoning; however, it is possible to quantify the detected drugs and their metabolites. A transparent scheme of chemical-toxicological analysis was compiled and optimized in forensic chemical expert studies of biological objects to improve the diagnosis of poisoning with derivatives of barbituric acid.
Keywords: derivatives of barbituric acid, chemical, and toxicological analysis.
ВведениеС каждым годом расширяется ассортимент веществ, используемых молодыми людьми с целью воздействия на центральную нервную систему. Среди наркотических веществ, употребляемых наркоманами, наиболее часто используются синтетические аналоги опиатов и курительные смеси на основе синтетических каннабиноидов, часто в комбинации с этанолом. Первый способ лечения наркомании, который приходит в голову самому наркоману – облегчение абстиненции с помощью различных лекарственных средств [3]. Самым подходящими с их точки зрения являются снотворные средства, которые они готовы употреблять в количествах, превышающих высшую суточную дозу. Примером комбинированного снотворного препарата является реладорм – таблетки, содержащие циклобарбитал и диазепам – способен сформировать настоящую зависимость [4]. Кроме того, он при массивном использовании, а именно так его применяют наркоманы, вызывает поражение головного мозга – энцефалопатию.
В настоящее время остается актуальным определение производных барбитуровой кислоты в смеси с наркотическими веществами при химико-токсикологическом анализе. Указанное обстоятельство требует подобрать оптимальную схему исследования, позволяющую, не ухудшая качество, значительно снизить сроки проведения химико-токсикологического анализа.
В практике ГОБУЗ «Новгородское Бюро судебно-медицинской экспертизы» встретился случай злоупотребления таблетками «Реладорм», содержащими диазепам и циклобарбитал. Из реанимационного отделения больницы был доставлен больной, со слов родственников стало известно, что он принял таблетки анальгина и димедрола, после чего отметил ухудшение самочувствия и был госпитализирован. Для проведения химико-токсикологического анализа были направлены кровь, моча и промывные воды желудка, а также таблетки (14 штук), обнаруженные в кармане больного, которые исследовались в первую очередь, так как предварительная реакция мочи и промывных вод на производные пиразолона (с раствором хлорида окисного железа) была отрицательной.
В ходе эксперимента было решено разработать схему химико-токсикологического анализа: изолирование, очистку, скрининг, качественный и количественный анализ для исследуемых биожидкостей и неизвестных таблеток. Для анализа было предоставлено: 100 мл мочи, 10 мл крови, 100 мл промывных вод из желудка, неизвестные таблетки 14 штук (таблетки белого цвета, плоской округлой формы, диаметром 7 мм, весом 110 мг, толщиной 1,5 мм).
Для иммунохроматографического определения использовали тест-полоски на фенциклидин серия №100804, трициклические антидепрессанты серия №240801, морфин серия №50810, бензодиазепины серия №60810, амфетамин серия №30810, метамфетамин серия №80804, марихуану серия №20810, метадон серия №70810, кокаин серия №40810, барбитураты №90810.
В чистую емкость вносили анализируемый образец мочи (1,5 мл). Погружали тест-полоски строго вертикально концом со стрелками в мочу на 30 секунд. Извлекали и через 5минут наблюдали одну розовую полосу на тест-полосках для барбитуратов и бензодиазепинов. На других тест-полосках наблюдали по две розовые полосы. Делали вывод, что в анализируемом образце предположительно присутствуют производные барбитуровой кислоты, 1,4-бензодиазепина.
Далее проводили пробоподготовку: 10 мл крови помещали в колбу, прибавляли 20 мл 96% этилового спирта, подкисленного насыщенным раствором щавелевой кислоты, до рН=2 и нагревали на кипящей водяной бане с обратным холодильником 50 минут. После охлаждения содержимое колбы фильтровали в фарфоровую чашку и выпаривали досуха на водяной бане. Сухой остаток обрабатывали 20 мл теплой воды и проводили экстракцию органическими растворителями: при рН=2 и рН=9 – хлороформом, при рН=13 – эфиром. При аналогичных значениях рН проводили прямую экстракцию для мочи и промывных вод. Щелочные извлечения для каждого объекта объединяли соответственно. Растворители испаряли при комнатной температуре. Сухие кислые остатки растворяли в 3 мл хлороформа каждый. Параллельно исследовали неизвестные таблетки, предварительно растворив их в 5 мл хлороформа и профильтровав.
Полученные хлороформные вытяжки экстрагировали 0,1 н раствором едкого натра и центрифугировали – водные фазы отбирали пипеткой, промывали хлороформный слой водой очищенной дважды по 5 мл. Промывные воды также отбирали пипеткой, присоединяя их к основной водной фазе, подкисляли щавелевой кислотой до рН=2 и дважды по 5 мин экстрагировали хлороформом порциями по 20 мл. Хлороформные вытяжки объединяли и доводили до объема 50 мл (V1).
0,3 мл хлороформных извлечений и раствора неизвестной таблетки наносили с помощью капилляра в виде точки на стартовую линию трех хроматографических пластинок Sorbfil. На линию старта наносили в качестве свидетелей в одну точку последовательно по 0,2 мл (1мг в 1мл этанола) барбитал, фенобарбитал, этаминал-натрий, барбамил, и 0,2 мл (1мг в 1мл хлороформа) бензонал, циклобарбитал, диазепам. Полученные пятна диаметром не более 0,5 см подсушивали.
Хроматографирование проводили в следующих системах растворителей: хлороформ – н-бутанол – 25 % раствор аммиака (70:40:5), хлороформ – ацетон (9:1), изопропанол – хлороформ – 25% раствор аммиака (90:90:20). Камеры предварительно насыщали системой растворителей в течение 60 мин. Длина пробега фронта растворителя – 10 см. Время хроматографирования – 45 мин. После подсушивания при комнатной температуре до полного удаления растворителей пластинки равномерно опрыскивали 0,02% раствором дифенилкарбазона в хлороформе, а затем 2,5% раствором сульфата ртути [2].
На первой пластине в зоне нанесения свидетелей наблюдали пятна сиреневато-фиолетового цвета с Rf: барбитал – 0,22, фенобарбитал – 0,21, бензонал – 0,39, барбамил – 0,29, этаминал-натрия – 0,35, циклобарбитал – 0,31. В зоне нанесения исследуемых извлечений и неизвестной таблетки наблюдали пятна сиреневато-фиолетового цвета с Rf – 0,31.
На второй пластине в зоне нанесения свидетелей наблюдали пятна сиреневато-фиолетового цвета с Rf: барбитал – 0,70, фенобарбитал – 0,49, бензонал (2 пятна) – 0,49 и 0,61, барбамил – 0,85, этаминал-натрия – 0,94, циклобарбитал – 0,56. В зоне нанесения исследуемых извлечений и неизвестной таблетки наблюдали пятна сиреневато-фиолетового цвета с Rf –0,56.
На третьей пластине в зоне нанесения свидетелей наблюдали пятна сиреневато-фиолетового цвета с Rf: барбитал – 0,65, фенобарбитал – 0,44, бензонал – 0,54, барбамил – 0,80, этаминал-натрия – 0,89, циклобарбитал –0,59. В зоне нанесения исследуемых извлечений и неизвестной таблетки наблюдали пятна сиреневато-фиолетового цвета с Rf – 0,59.
Затем эти пластины обесцвечивали в токе теплого воздуха и проявляли реактивом Драгендорфа. В зоне нанесения свидетелей наблюдали пятна оранжевого цвета с Rf: на первой пластине – 0,45; на второй пластине – 0,65; на третьей – 0,70 для диазепама. В зоне нанесения исследуемых извлечений и неизвестной таблетки наблюдали пятна оранжевого цвета с Rf: на первой пластине – 0,45; на второй пластине – 0,65; на третьей – 0,70.
По результатам экспериментальной части можно сделать вывод, что системы хлороформ-н-бутанол-25 % раствор аммиака (70:40:5), хлороформ-ацетон (9:1), используемые в тонкослойной хроматографии, являются оптимальными для определения производных барбитуровой кислоты, так как пятна для веществ-свидетелей проявляются более четко и разгоняются на разные уровни.
Для исследуемых биожидкостей проводили качественное и количественное определение неизвестного токсиканта методом – спектрофотометрия в УФ-области: по 1 мл (V2) исследуемых кислых хлороформных извлечений помещали в фарфоровые чашки, растворитель испаряли, а сухие остатки растворяли в 4 мл (V3) боратного буфера (pH=9). Снимали спектры поглощения в области длин волн 220-300 нм на спектрофотометре СФ-46 с толщиной слоя кюветы 10 мм, раствор сравнения – боратный буфер (pH=9) [1], [7]. Затем в кюветы добавляли по 2 капли насыщенного раствора едкого натра (рН=13) и после тщательного перемешивания вновь снимали спектр поглощения в том же интервале длин волн. Далее в кюветы вносили по одной капле концентрированной соляной кислоты для достижения значения рН=2, и вновь снимали спектр в области длин волн 220-300нм (см. таблицу 1).
Таблица 1 – Результаты спектрофотометрического определения биообъектов
| Длина волны | Кровь | Моча | Промывные воды | ||||||
| рН=9 | рН=13 | рН=2 | рН=9 | рН=13 | рН=2 | рН=9 | рН=13 | рН=2 | |
| 220 224 228 232 236 240 244 248 252 256 260 264 268 272 276 280 300 | 1,730 1,600 1,630 1,720 1,800 1,840 1,710 1,450 1,110 0,800 0,590 0,480 0,400 0,350 0,325 0,300 0,215 | 1,610 1,530 1,410 1,320 1,240 1,180 1,170 1,240 1,300 1,360 1,310 1,250 1,170 1,080 1,015 0,950 0,900 | 2,030 1,740 1,450 1,240 1,100 0,990 0,900 0,820 0,760 0,730 0,710 0,680 0,650 0,620 0,590 0,570 0,460 | 0,870 0,740 0,860 1,040 1,165 1,225 1,155 1,015 0,900 0,805 0,720 0,645 0,580 0,515 0,450 0,390 0,250 | 0,780 0,710 0,640 0,560 0,480 0,410 0,370 0,395 0,470 0,535 0,470 0,415 0,355 0,300 0,245 0,200 0,100 | 0,990 0,860 0,760 0,680 0,600 0,520 0,450 0,370 0,295 0,200 0,175 0,150 0,120 0,100 0,085 0,065 0,045 | 1,650 1,500 1,360 1,200 1,450 1,710 1,310 0,970 0,760 0,590 0,480 0,420 0,390 0,360 0,330 0,300 0,155 | 1,350 1,280 1,235 1,180 1,140 1,080 1,015 1,035 1,090 1,170 1,130 1,055 0,980 0,920 0,850 0,800 0,750 | 1,800 1,540 1,310 1,085 0,900 0,750 0,650 0,580 0,540 0,520 0,520 0,520 0,500 0,490 0,460 0,440 0,270 |
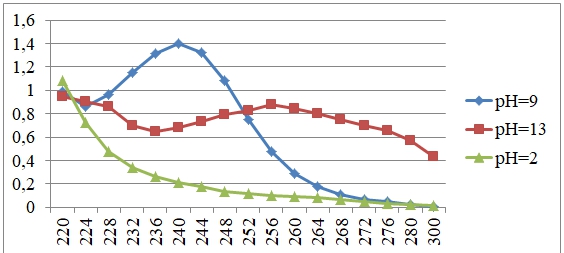
Рис. 1 – УФ-спектр поглощения циклобарбитала при разных значениях рН
Наблюдались максимумы поглощения для циклобарбитала и исследуемых извлечений: при рН=9 – 240 нм, рН=13 – 256 нм. При рН=2 каких-либо максимумов не наблюдали.
Для количественного определения измеряли оптическую плотность на спектрофотометре СФ-46 с толщиной слоя кюветы 10 мм при длине волны 260 нм, раствор сравнения – боратный буфер. Были получены результаты:
рН=9 – Dкровь=0,263, Dмоча=0,530, Dпромывные воды=0,230;
рН=13 – Dкровь=0,265, Dмоча=0,540, Dпромывные воды=0,255.
Для расчета пользовались значениями удельного показателя поглощения (Е1%1см), который вычисляли по формуле (см. таблицу 2):
![]() (1)
(1)
Из однородных результатов, используя статистическую обработку, определяли среднее арифметическое значение удельного показателя поглощения, которое составило Е1%1см = 410.
Расчет концентрации циклобарбитала (Х) в исследуемых объектах производили по формуле:
Таблица 2 – Результаты количественного определения
| Концентрация циклобарбитала, мг% | D при рН=9 | D при рН=13 | Е1%1см |
| 0,4 0,6 0,8 0,10 0,15 0,20 | 0,192 0,286 0,396 0,490 0,712 0,947 | 0,030 0,040 0,066 0,075 0,100 0,127 | 405 410 412 415 408 410 |
Концентрация циклобарбитала по формуле (2) равна: в крови 0,9 мг%; в моче 0,4 мг%, в промывных водах 1,2 мг%.
По 1 мл кислых извлечений и 0,1 мл хлороформного раствора таблетки переносили в чистые флаконы и испаряли растворитель досуха. К сухим остаткам добавляли 100 мкл этилацетата и по 1 мкл этилацетатных растворов исследовали на хромато-масс-спектрометре Agilent7890/5975N EI/PCI с капиллярной колонкой НР-5 MS длиной 30 м и диаметром 0,25 мм. Начальная температура колонки 100°С, скорость подъема температуры 25°С в минуту до 300°С. Время эксперимента – 26 минут.
По результатам исследования были идентифицированы пики, соответствующие по времени удерживания и масс-спектрам циклобарбиталу и диазепаму в крови, моче, промывных водах желудка, неизвестной таблетке.
Стоит отметить, что газовая хроматография с масс-селективным детектированием (ГХ/МС) получила широкое распространение в судебно-химическом и химико-токсикологическом анализе как высокоспецифичный, чувствительный и достаточно экспрессный метод.
Заключение
С целью сокращения времени химико-токсикологического анализа биожидкостей при отравлении производными барбитуровой кислоты и смешанных отравлениях, в том числе производными барбитуровой кислоты, предложено использовать комбинацию принципиально разных методов, и получение по каждому из них положительных результатов. При этом выполняется основное правило – проведение химико-токсикологического анализа как минимум двумя методами, причем один из этих методов используется для предварительного исследования, а другой – для подтверждающего исследования. Также оптические и хроматографические, в совокупности с масс-селективным детектированием, методы позволяют открывать не только производные барбитуровой кислоты, но и другие токсикологически важные соединения одновременно.
| Конфликт интересов Не указан. | Conflict of Interest None declared. |
Список литературы / References
- Вергейчик Т.Х. Токсикологическая химия: учебник / Т. Х. Вергейчик. – М.: МЕДпресс-информ, 2009. – С. 142-157
- Внуков В.И. Тонкослойная хроматография при исследовании наркотических средств [Электронный ресурс] / В.И, Внуков, Д.В. Кайргалиев, Д.В. Васильев и др. // Современные проблемы науки и образования. – 2015. – №1-2; URL: http://science-education.ru/ru/article/view?id=19878 (дата обращения: 14.02.2020).
- Ермаков М.Г. Психоактивные свойства сильнодействующих и ядовитых веществ: уголовно-правовой аспект / М.Г. Ермаков // Психопедагогика в правоохранительных органах. – 2012. – №4 (51). – С. 10-13
- Захарченко М.Ю. Барбитураты, бензодиазепины, анаболические стероиды: история создания, действие, анализ: учебно-справочное пособие / М.Ю. Захарченко, И.Н. Мельников, Д.В. Кайргалиев; под ред. С. Я. Пичхидзе // Саратов: КУБиК, 2015. – 189 с.
- Илларионова Е.А. Химико-токсикологический анализ снотворных лекарственных средств: учебное пособие / Е.А. Илларионова, И.П. Сыроватский; ФГБОУ ВО ИГМУ Минздрава России, кафедра фармацевтической и токсикологической химии. – Иркутск: ИГМУ, 2016 – 32 с.
- Кайргалиев Д.В. Современные возможности экспертного исследования барбитуратов в сложных смесях / Д.В. Кайргалиев, И.Н. Мельников, Д.В. Васильев // Технико-криминалистическое обеспечение раскрытия и расследования преступлений: сборник тезисов и статей Международной научно-практической конференции, 19 октября 2018 г. / [составитель: Васильев Д. В.]. – Волгоград: Перископ-Волга, 2018. – С. 119-122
- Калетина Т.И. Токсикологическая химия. Аналитическая токсикология: учебник / Т.И. Калетина; под ред. Р.У. Хабриева, Н.И. Калетиной. – М.: ГЭОТАР-Медиа, 2010. – С. 472-484
- Киричек А.В. Исследование производных барбитуровой кислоты в застарелых пятнах крови на тканях / А.В. Киричек, А.Э. Шабалина, Л.А. Рассинская // Судебно-медицинская экспертиза. – М., 2017 – №2. – С. 27-29.
- Петрова О.С. Токсикологическая химия: учебно-методическое пособие / О.С. Петрова, Г.А. Антропова // НовГУ им. Ярослава Мудрого. – Великий Новгород, 2012. – С. 49-54
- Clarke`s analysis of drugs and poisons / Ed.Moffat A.C., Osselton M.D., Widdop B.– London, Pharmaceutical Press, 2011. – Fourth Edition. – Р. 1177
Список литературы на английском языке / References in English
- Vergejchik T.H. Toksikologicheskaya himiya: uchebnik [Toxicological chemistry: textbook] / T. H. Vergejchik. – M.: MEDpress-inform, 2009. – Р. 142-157 [in Russian]
- Vnukov V.I. Tonkoslojnaya hromatografiya pri issledovanii narkoticheskih sredstv [Thin-layer chromatography in the study of narcotic drugs] [Electronic resource] / V.I, Vnukov, D.V. Kajrgaliev, D.V. Vasil'ev et al // Sovremennye problemy nauki i obrazovaniya. – 2015. – №1-2; URL: http://science-education.ru/ru/article/view?id=19878 (accessed: 14.02.2020).
- Ermakov M.G. Psihoaktivnye svojstva sil'nodejstvuyushchih i yadovityh veshchestv: ugolovno-pravovoj aspekt [Psychoactive properties of potent and toxic substances: criminal law aspect] / M.G. Ermakov // Psihopedagogika v pravoohranitel'nyh organah. – 2012. – №4 (51). – P. 10-13
- Zaharchenko M.Yu. Barbituraty, benzodiazepiny, anabolicheskie steroidy: istoriya sozdaniya, dejstvie, analiz: uchebno-spravochnoe posobie [Barbiturates, benzodiazepines, anabolic steroids: history of creation, action, analysis: educational reference guide] / M.Yu. Zaharchenko, I.N. Mel'nikov, D.V. Kajrgaliev; pod red. S. Ya. Pichkhidze // Saratov: KUBiK, 2015. – 189 р. [in Russian]
- Illarionova E.A. Himiko-toksikologicheskij analiz snotvornyh lekarstvennyh sredstv: uchebnoe posobie [Chemical and Toxicological analysis of sleeping pills: textbook] / E.A. Illarionova, I.P. Syrovatskij; FGBOU VO IGMU Minzdrava Rossii, kafedra farmacevticheskoj i toksikologicheskoj himii. – Irkutsk: IGMU, 2016 – 32 р. [in Russian]
- Kajrgaliev D.V. Sovremennye vozmozhnosti ekspertnogo issledovaniya barbituratov v slozhnyh smesyah [Modern possibilities of expert research of barbiturates in complex mixtures] / D.V. Kajrgaliev, I.N. Mel'nikov, D.V. Vasil'ev // Tekhniko-kriminalisticheskoe obespechenie raskrytiya i rassledovaniya prestuplenij: sbornik tezisov i statej Mezhdunarodnoj nauchno-prakticheskoj konferencii, 19 oktyabrya 2018 g. / [sostavitel': Vasil'ev D. V.]. – Volgograd: Periskop-Volga, 2018. – Р. 119-122 [in Russian]
- Kaletina T.I. Toksikologicheskaya himiya. Analiticheskaya toksikologiya: uchebnik [Toxicological chemistry. Analytical toxicology: textbook] / T.I. Kaletina; pod red. R.U. Habrieva, N.I. Kaletinoj. – M.: GEOTAR-Media, 2010. – Р. 472-484 [in Russian]
- Kirichek A.V. Issledovanie proizvodnyh barbiturovoj kisloty v zastarelyh pyatnah krovi na tkanyah [Study of barbituric acid derivatives in old blood spots on tissues] / A.V. Kirichek, A.E. Shabalina, L.A. Rassinskaya // Sudebno-medicinskaya ekspertiza. – M., 2017 – №2. – Р. 27-29 [in Russian]
- Petrova O.S. Toksikologicheskaya himiya: uchebno-metodicheskoe posobie [Toxicological chemistry: educational and methodical manual] / O.S. Petrova, G.A. Antropova // NovGU im. Yaroslava Mudrogo. – Velikij Novgorod, 2012. – Р. 49-54 [in Russian]
- Clarke`s analysis of drugs and poisons / Ed.Moffat A.C., Osselton M.D., Widdop B.– London, Pharmaceutical Press, 2011. – Fourth Edition. – Р. 1177
