Experience with thrombolytic therapy and thrombectomy in patients with acute ischaemic stroke (clinical cases)
Experience with thrombolytic therapy and thrombectomy in patients with acute ischaemic stroke (clinical cases)
Abstract
Acute ischaemic stroke occupies one of the leading places in the structure of disability and mortality of the adult population worldwide, which also determines a significant social and economic burden of this pathology. Recent advances in the diagnosis and treatment of acute ischaemic stroke have significantly reduced mortality and improved functional outcomes in patients. However, there are still categories of patients with unsatisfactory results of reperfusion therapy, as well as its complications. In some categories of such patients, mortality may exceed the overall rate. To date, there are still controversial aspects in determining the indications and choosing the preferred method of cerebral reperfusion. In the presented clinical observations, the results of thrombolytic therapy and thrombectomy in patients of different age groups in acute ischaemic stroke are reviewed. The importance of various methods of neuroimaging (multispiral computed tomography, computed angiography, ultrasound duplex scanning of extracranial and intracranial arteries) for timely diagnosis and determination of optimal revascularization tactics is noted.
1. Введение
Острые нарушения мозгового кровообращения остаются одной из ведущих причин смертности и инвалидизации пациентов как в Российской Федерации, так и во всем мире. Доля острого ишемического инсульта (ОИИ) составляет более 60% среди всех известных подтипов. Последние достижения в диагностике и лечении ОИИ позволили существенно (в 2 раза) снизить летальность и улучшить функциональные исходы у пациентов. Однако сохраняются категории пациентов с неудовлетворительными результатами реперфузионной терапии, а также ее осложнениями. В некоторых категориях таких пациентов летальность может превышать общий показатель (до 44%) .
Оказание эффективной помощи пациентам с ОИИ основывается на своевременном применении реперфузионной терапии. Для этого очевидна необходимость раннего распознавания симптомов, корректной сортировки в ближайший сосудистый центр, а также эффективной диагностики. Целью лечения является достижение реканализации и реперфузии ишемизированной области с помощью внутривенного тромболизиса и/или эндоваскулярной тромбэкстракции (ТЭ) у соответствующим образом отобранных пациентов. Непосредственное значение для эффективности любого метода реваскуляризации имеет длительность так называемого терапевтического окна. Для тщательного мониторинга раннего неврологического ухудшения и предотвращения вторичных осложнений необходимо применение современных наиболее точных методов нейровизуализации.
В настоящее время достигнуты значительные успехи в области реперфузионной терапии. Системная тромболитическая терапия (ТЛТ) с использованием рекомбинантного тканевого активатора плазминогена (recombinant tissue plasminogen activator – rt-PA) альтеплазы стала возможной более 30 лет назад благодаря внедрению в клиническую практику мультиспиральной компьютерной томографии (МСКТ), позволяющей диагностировать характер инсульта.
В ходе многоцентрового рандомизированного плацебо контролируемого исследования NINDS была впервые доказана безопасность и эффективность системной ТЛТ с использованием rt-PA в первые три часа от начала развития заболевания . Ряд последующих исследований продемонстрировали противоречивые результаты введения разных доз rt-PA на более поздних сроках: в исследованиях ECASS I, ECASS II, ATLANTIS (А и В), IST III эффективность ТЛТ не была подтверждена по сравнению с группой плацебо , , , , тогда как данные авторов ECASS III о безопасности и эффективности системной ТЛТ в первые 4,5 часа после появления симптомов послужили поводом к пересмотру европейских, американских и российских рекомендаций по лечению ОИИ и увеличению длительности терапевтического окна . Таким образом, данные об эффективности и безопасности применения системной ТЛТ содержатся лишь в двух исследованиях (NINDS и ECASS III).
Большинство экспертов сходится во мнении, что эффективность ТЛТ обеспечивается тщательным отбором пациентов и зависит не только от времени начала лечения, но и от наличия и размеров области головного мозга с потенциально обратимыми изменениями, особенностей системной и локальной гемодинамики, состоянии системы гемостаза, чувствительности вещества головного мозга к ишемии, степени повреждения гематоэнцефалического барьера.
Относительно возраста пациентов, которые могут являться кандидатами для применения системной ТЛТ, также в литературе консенсус отсутствует. Согласно инструкции к препарату альтеплаза, не следует проводить ТЛТ лицам моложе 18 лет, а пациентам старше 80 лет – проводить с особой осторожностью. В последней группе пациентов не отмечено существенного увеличения частоты геморрагических осложнений наряду с более высокими показателями летальности и инвалидизации, что связывают с независимым влиянием возраста на функциональный исход и риск смерти от ОИИ .
В представленных клинических наблюдениях рассмотрены результаты применения ТЛТ и ТЭ у пациентов разных возрастных групп при ОИИ.
2. Клинический случай № 1
Пациентка К., 67 лет, поступила экстренно с жалобами на нарушение речи, слабость в правых конечностях. Из анамнеза известно, что пациентка страдает сахарным диабетом, гипертонической болезнью 3 степени. На момент поступления: общее состояние пациентки тяжелое, сознание ясное, артериальное давление составило 160/100 мм. рт. ст. В неврологическом статусе отмечались дизартрия, сглаженность правой носогубной складки, девиация языка вправо, правосторонний гемипарез 3 балла и правосторонняя гемигипестезия, патологические рефлексы справа. Степень неврологического дефицита по шкале NIHSS оценена как средняя (11 баллов).
Госпитализирована в отделение реанимации и интенсивной терапии с диагнозом: цереброваскулярная болезнь, острое нарушение мозгового кровообращения в бассейне левой средней мозговой артерии (СМА) по ишемическому типу. Время от начала появления симптомов до помещения в отделение реанимации составило 3 часа.
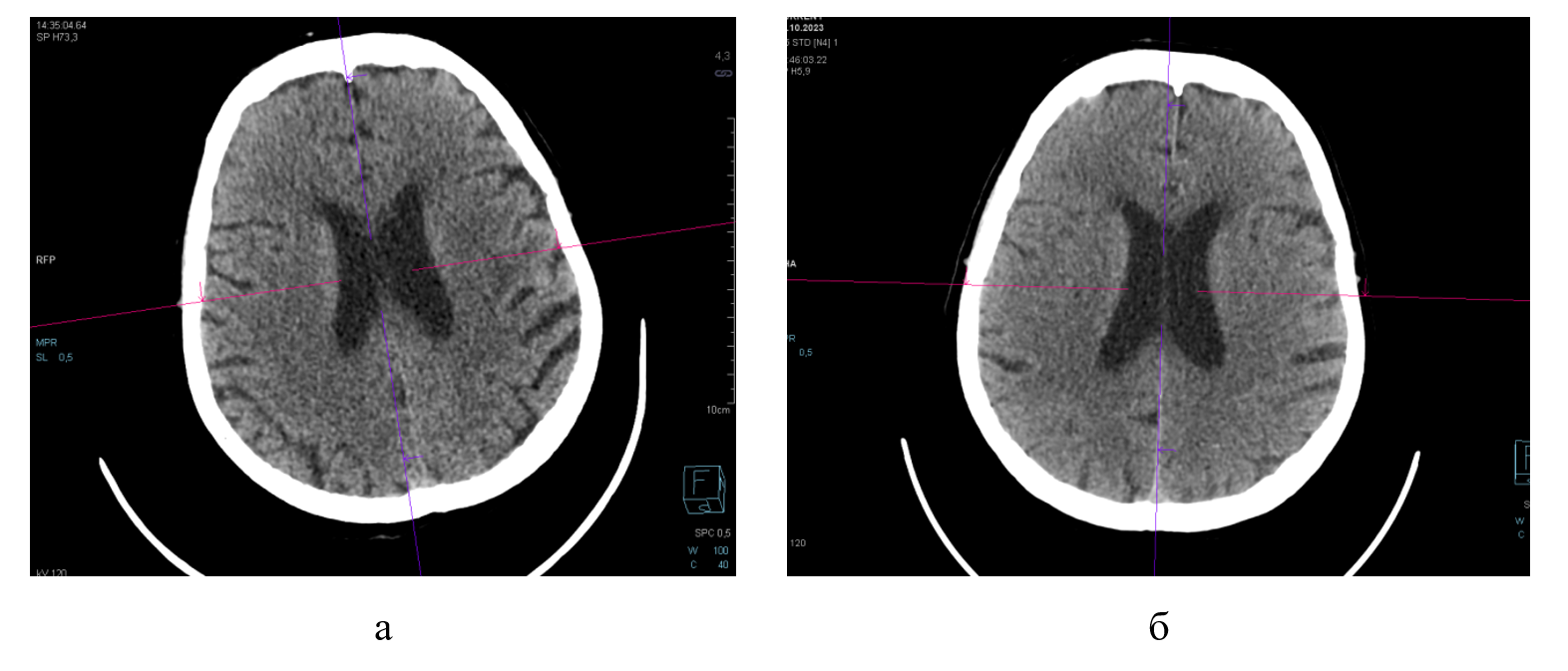
Рисунок 1 - МСКТ головного мозга без контрастного усиления в аксиальной проекции пациентки К.:
а - при поступлении в стационар; б - после проведения ТЛТ
Примечание: зон снижения денситометрической плотности головного мозга при поступлении в стационар и после проведения ТЛТ не выявлено
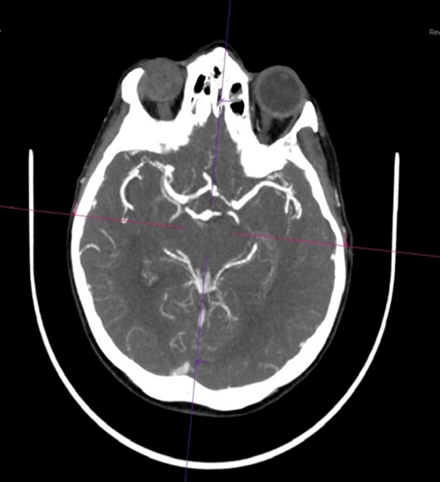
Рисунок 2 - КТА артерий головного мозга в аксиальной проекции пациентки К. при поступлении
Примечание: артериальная фаза: дефектов контрастирования M1–M3 сегментов левой СМА не выявлено
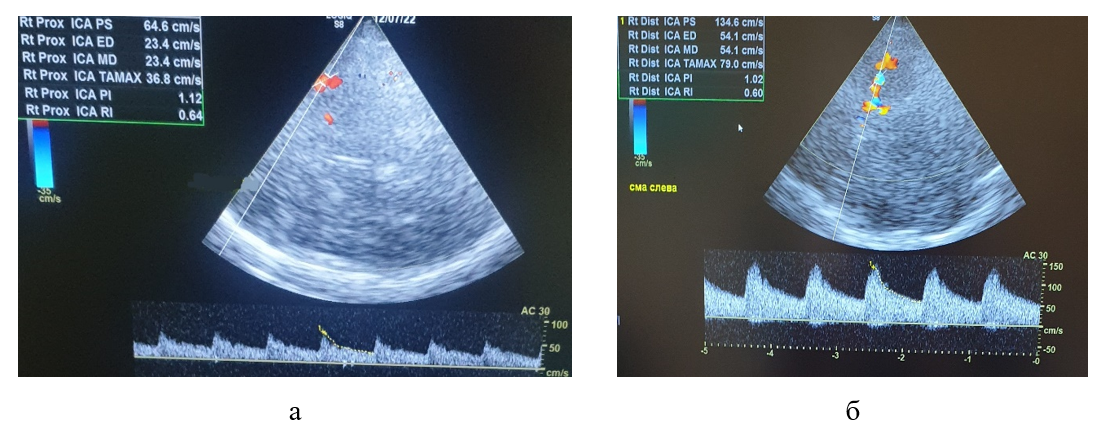
Рисунок 3 - Транскраниальное дуплексное сканирование пациентки К.:
а - при поступлении в стационар; б - на 3 сутки после ТЛТ
Примечание: гипоперфузия в левой СМА в виде снижения систолической (Vsist = 64,4 см/с) и усредненной по времени средней (TAMAX = 36,8 см/с) скоростей кровотока при поступлении в стационар; скоростные показатели в левой СМА в пределах нормативных значений (Vsist = 134,6 см/с, TAMAX = 79 см/с) на 3 сутки после ТЛТ
По данным МСКТ головного мозга, после проведенного лечения гиподенсивные изменения в обоих полушариях головного мозга не выявлены (рис. 1 б). ДС интракраниальных артерий на третьи сутки после ТЛТ определило, что скоростные показатели и индексы периферического сопротивления в левой СМА в пределах нормативных значений (рис. 3 б).
Таким образом, в результате проведенной ТЛТ у пациентки с сопутствующей патологией в виде артериальной гипертонии, дислипидемии и сахарного диабета, с неврологическим дефицитом средней тяжести (по шкале NIHSS – 11 балла) при поступлении удалось достичь клинического и функционального улучшения: реабилитационный потенциал по шкале реабилитационной маршрутизации (ШРМ) составил 3 балла (умеренное нарушение функций, структур и процессов жизнедеятельности), статус по шкале NIHSS – 4 балла, Rankin– 3 балла. Формирования зон ишемии головного мозга и нарушений церебральной гемодинамики при выписке не наблюдалось. Назначена программа реабилитации согласно основному и сопутствующему диагнозу.
3. Клинический случай № 2
Пациент Ц., 42 года, госпитализирован экстренно с жалобами на внезапную слабость в правых конечностях, нарушение речи во время нахождения за рулем автомобиля. В неврологическом статусе: моторная афазия, сглаженность правой носогубной складки, девиация языка вправо, правосторонний гемипарез 2 балла, правосторонняя гемигипестезия. Градация по шкале NIHSS составила 16 баллов. Среди сопутствующих заболеваний выявлены: артериальная гипертензия 3 степени с высоким риском сердечно-сосудистых осложнений, дислипидемия, алиментарное ожирение.
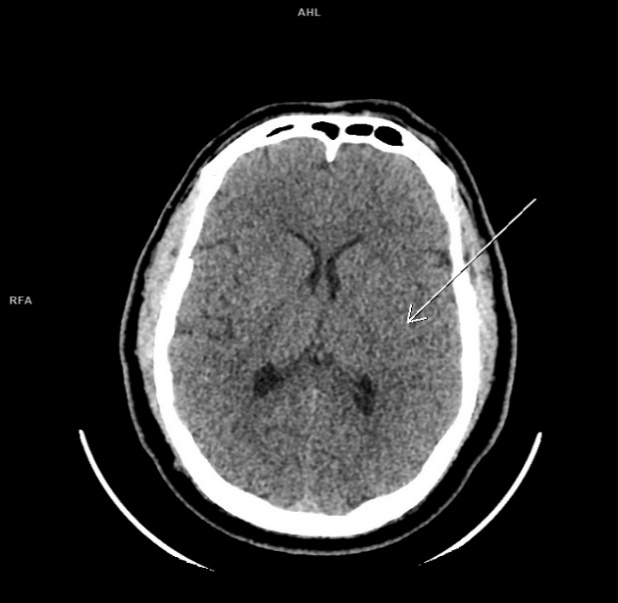
Рисунок 4 - МСКТ головного мозга без контрастного усиления в аксиальной проекции пациента Ц. при поступлении
Примечание: зон снижения денситометрической плотности головного мозга не выявлено
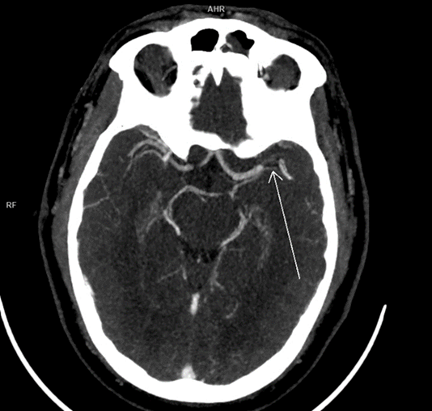
Рисунок 5 - КТА артерий головного мозга в аксиальной проекции пациента Ц. при поступлении, артериальная фаза
Примечание: окклюзия M1 сегмента левой СМА
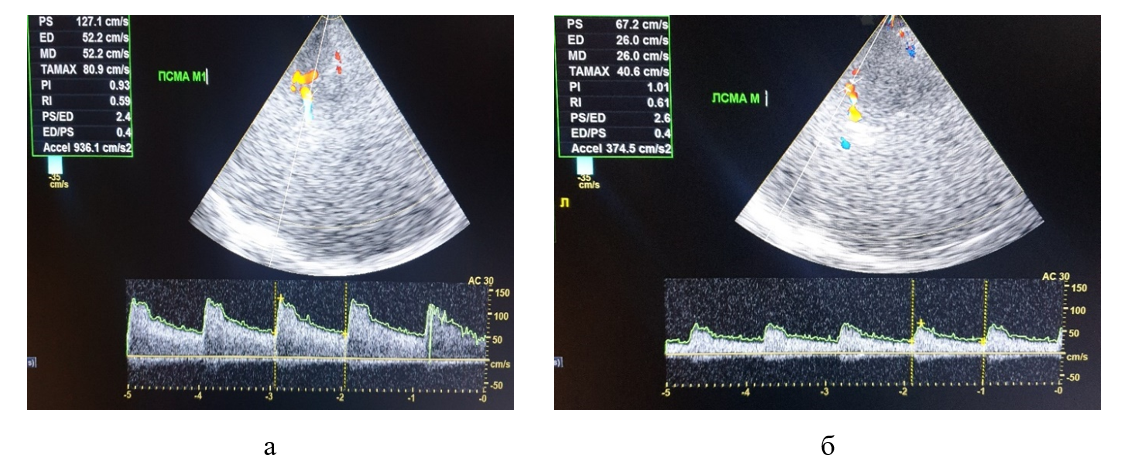
Рисунок 6 - Транскраниальное дуплексное сканирование пациента Ц. при поступлении в стационар:
а - систолическая (Vsist = 127,1 см/с) и усредненная по времени средняя (TAMAX = 80,9 см/с) скорости кровотока и индексы периферического сопротивления (PI = 0,9; RI = 0,6) в М1 сегменте правой СМА в пределах нормативных значений; б - гипоперфузия в М2 сегменте левой СМА в виде снижения систолической (Vsist 67,2 = см/с) и усредненной по времени средней (TAMAX 40,6 = см/с) скоростей кровотока
Учитывая высокую степень неврологического дефицита по NIHSS (16 баллов), продолжительность терапевтического окна не более 4,5 часов, данные МСКТ (ASPECTS 10 баллов) и КТА (окклюзия М1 сегмента левой СМА), принято решение о выполнении механической тромбэкстракции (ТЭ) из М1 сегмента левой СМА в сочетании с системной тромболитической терапией препаратом актилизе.
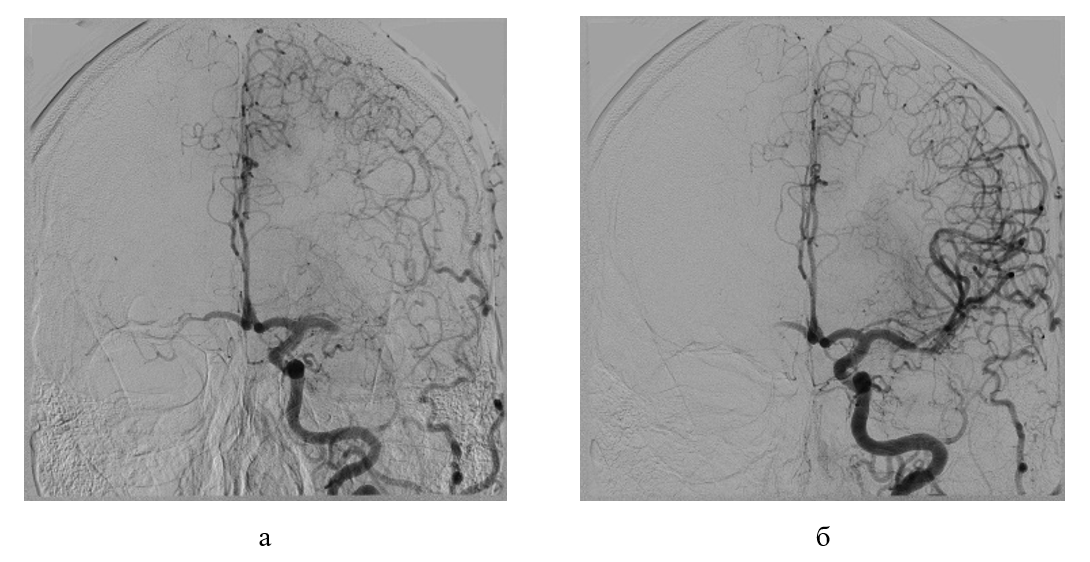
Рисунок 7 - Рентгенконтрастная церебральная ангиография пациента Ц., артериальная фаза:
а - окклюзия М1 сегмента левой СМА с контрастированием дистальных ветвей; б - антеградная реперфузия М1 сегмента левой СМА после выполнения тромбоаспирации
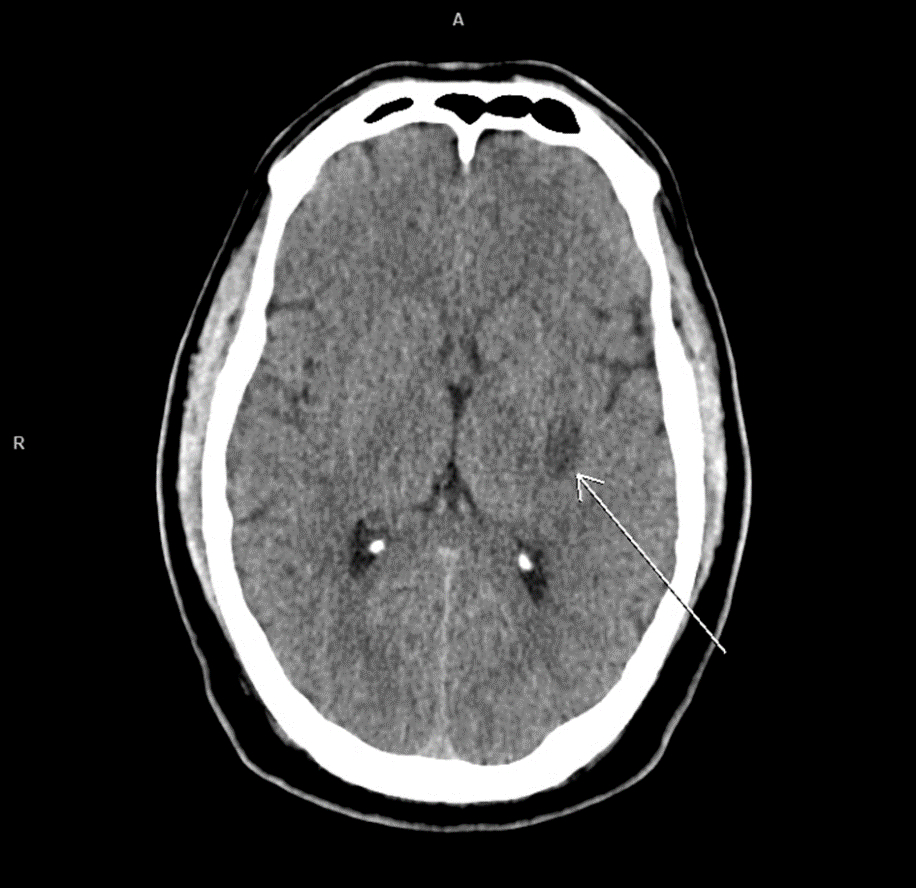
Рисунок 8 - МСКТ головного мозга без контрастного усиления в аксиальной проекции пациента Ц. на 3 сутки после лечения
Примечание: зона пониженной плотности (+21–+23HU) в бассейне левой СМА размерами 16 х 10 мм
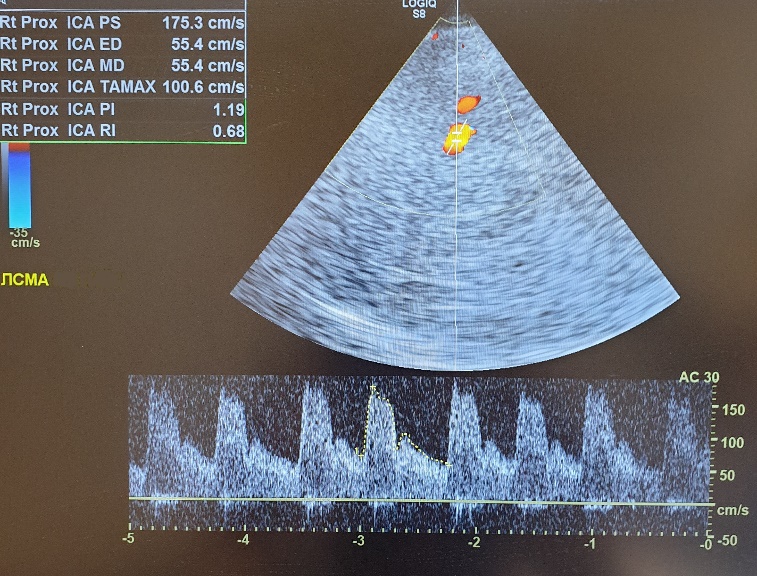
Рисунок 9 - Транскраниальное дуплексное сканирование пациента Ц. на 3 сутки после лечения
Примечание: синдром гиперперфузии в виде ускорения систолической (Vsist = 175,3 см/с) и усредненной по времени средней (TAMAX = 100,6 см/с) скоростей кровотока в левой СМА
4. Клинический случай № 3
Пациентка Н., 73 лет, поступила экстренно через 6,5ч от момента появления жалоб на слабость в левых конечностях. При поступлении пациентка в состоянии умеренного оглушения (по шкале комы Глазго 14-13 баллов), оценка по шкале Rankin – 5 баллов, NIHSS – 12 баллов. В неврологическом статусе: дизартрия, сглаженность левой носогубной складки, левосторонний гемипарез 3 балла, нарушение функции тазовых органов. Артериальное давление при поступлении – 170/100 мм. рт.ст. Среди сопутствующих заболеваний отмечены фибрилляция предсердий (пароксизм неизвестной давности), гипертоническая болезнь 3 степени, риск сердечно-сосудистых осложнений 4 степени, ишемическая болезнь сердца, хроническая сердечная недостаточность (II функциональный класс по NYHA), сахарный диабет 2 типа, компенсированный приемом пероральных сахароснижающих препаратов. По данным лабораторных исследований отмечалась дислипидемия и гипергликемия (6,8 ммоль/л).
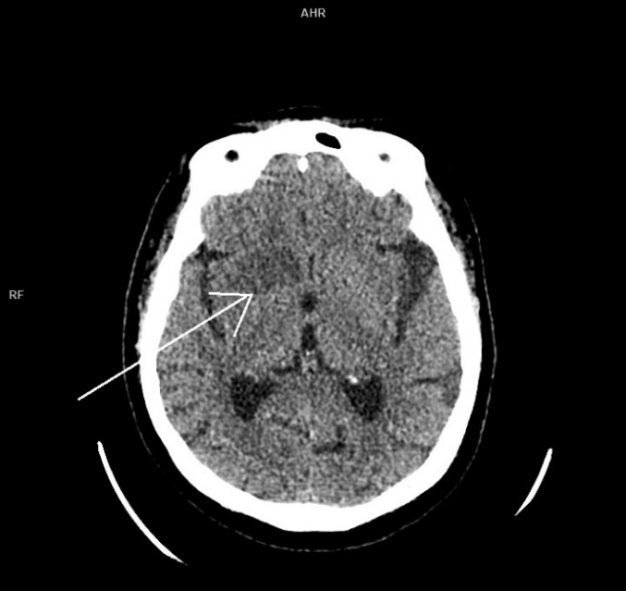
Рисунок 10 - МСКТ головного мозга без контрастного усиления в аксиальной проекции пациентки Н. при поступлении
Примечание: снижение денситометрической плотности в правой лобной доле (+22 HU), ASPECTS 8
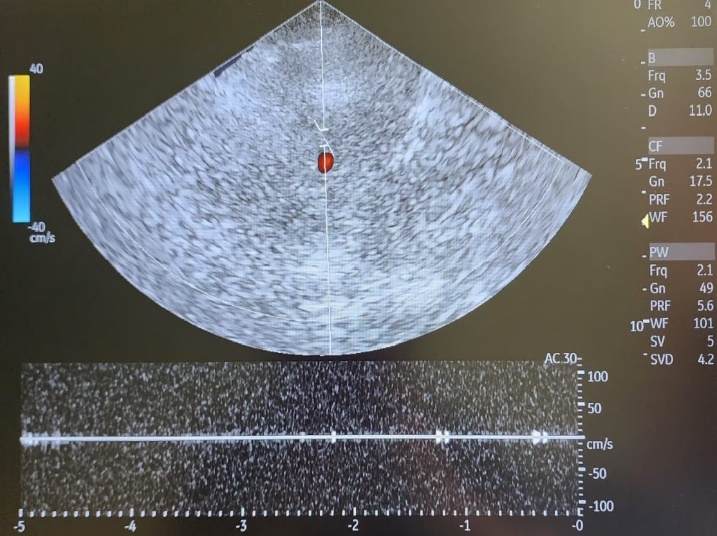
Рисунок 11 - Транскраниальное дуплексное сканирование пациентки Н. при поступлении
Примечание: отсутствие кровотока в правой СМА в режиме цветового допплеровского картирования и импульсно-волнового допплера
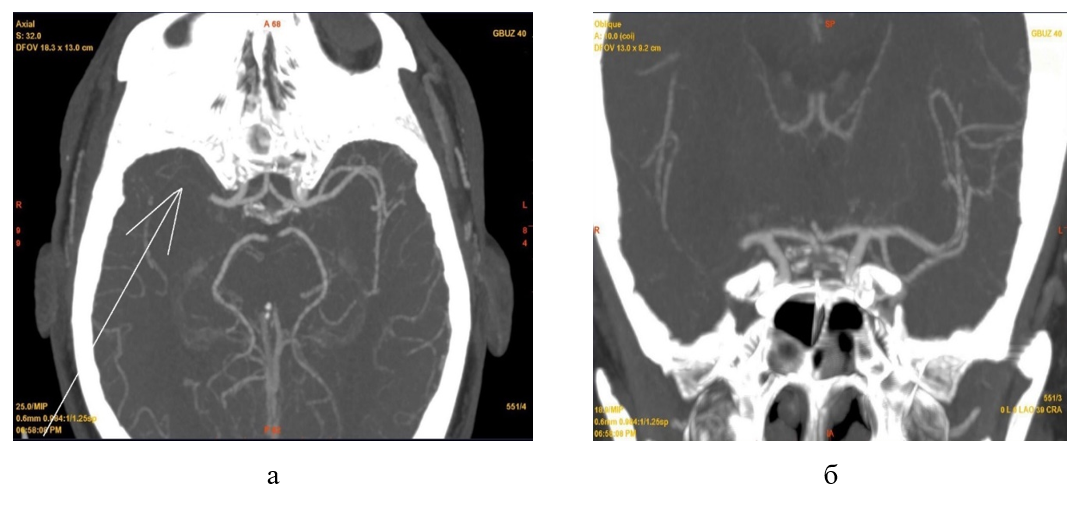
Рисунок 12 - КТА артерий головного мозга пациентки Н. при поступлении:
а - аксиальная проекция; б - фронтальная
Примечание: артериальная фаза, отсутствие контрастирования (тромбоз) М1 сегмента правой СМА
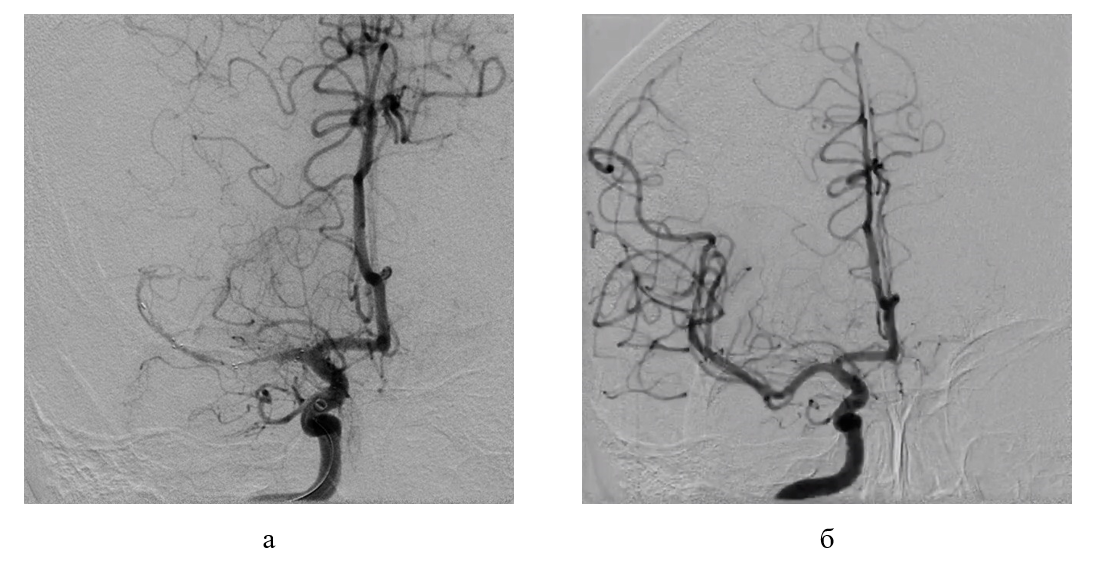
Рисунок 13 - Рентгенконтрастная церебральная ангиография пациентки Н., артериальная фаза:
а - отсутствие контрастирования правой СМА до лечения; б - антеградная реперфузия правой СМА после выполнения ТЭ с восстановлением кровотока на уровне TICI 3
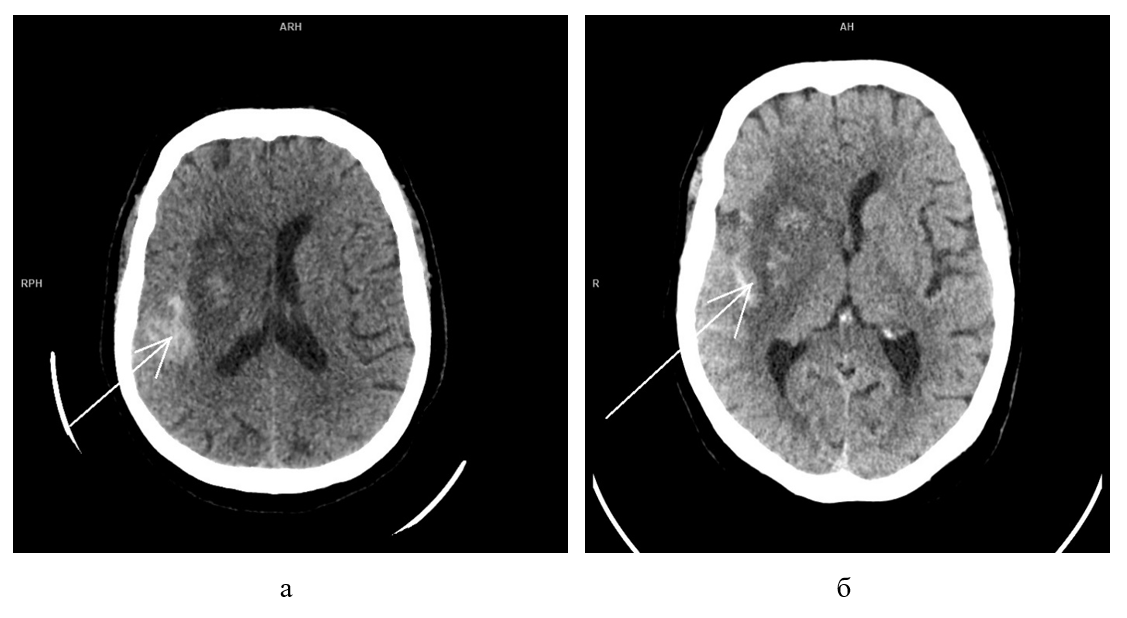
Рисунок 14 - МСКТ головного мозга без контрастного усиления в аксиальной проекции пациентки Н. после выполнения ТЭ:
а - первые сутки после лечения; б - четвертые сутки после лечения
Примечание: гиперденсный участок в области базальных ганглиев справа и гиперденсное содержимое в области борозд над правой гемисферой – геморагическое пропитывание
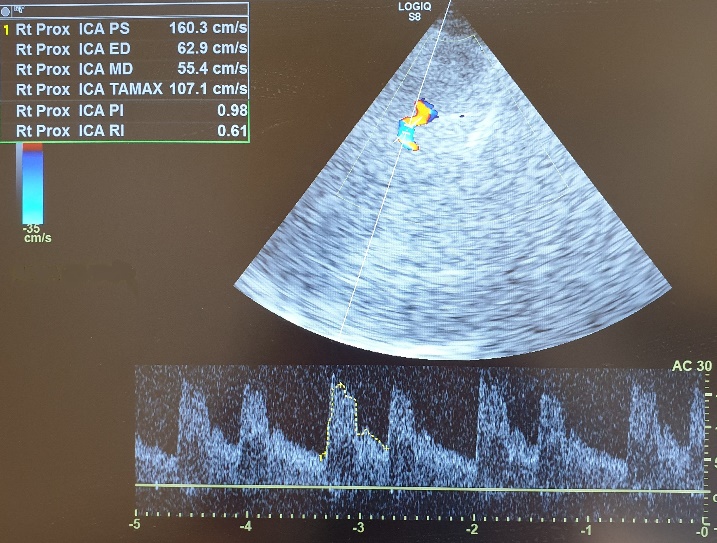
Рисунок 15 - Транскраниальное дуплексное сканирование пациентки Н. на третьи сутки после ТЭ
Примечание: синдром гиперперфузии в виде ускорения систолической (Vsist = 160,3 см/с) и усредненной по времени средней (TAMAX = 107,1 см/с) скоростей кровотока в правой СМА
5. Обсуждение случаев
По данным Американской кардиологической ассоциации, Американской ассоциации инсульта (AHA/ASA, 2019), внутривенное введение рекомбинантного тканевого активатора плазминогена (rt-PA) является основным вариантом выбора в лечении ОИИ в течение 4,5 часов с начала появления первых симптомов . В первом из представленных клинических наблюдений время от начала симптомов до проведения реперфузии составило 3,5 часа, что могло служить одним из наиболее значимых условий эффективности лечения. Показания к ТЛТ включают возраст пациентов от 18 до 80 лет, следовательно, противопоказания по критерию возраста у пациентки Ч. отсутствовали. На основании исследования ECASS-3 дополнительными критериями исключения для применения внутривенной ТЛТ ранее были: возраст более 80 лет, предшествующий ишемический инсульт и сахарный диабет, прием антикоагулянтов . Однако эти критерии больше не являются противопоказаниями к использованию внутривенной ТЛТ в соответствии с рекомендациями AHA, ASA (2019) . Внутривенная ТЛТ эффективна у пациентов с инвалидизирующим инсультом независимо от оценки по шкале NIHSS, но не рекомендуется при инсультах, не приводящих к инвалидности, когда оценка по шкале NIHSS 5 баллов и менее . В описываемом случае необходимость проведения ТЛТ представляется обоснованной ввиду промежуточного балла по шкале NIHSS. Показаний к проведению ТЭ не было в связи с отсутствием поражения магистральных церебральных артерий.
Использование рентгенхирургических эндоваскулярных вмешательств произвело революцию в сфере лечения ОИИ. До настоящего времени в литературе содержатся противоречивые данные о сравнительной эффективности ТЭ и системной ТЛТ , , . С 2015 г. эндоваскулярная реперфузия стала стандартом лечения после того, как несколько проспективных исследований продемонстрировали ее преимущества по сравнению с медикаментозным лечением у отдельных пациентов с ОИИ , . Метаанализ HERMES, который включал исследования MR CLEAN, ESCAPE, REVASCAT, SWIFT PRIME и EXTEND IA, показал, что эндоваскулярные вмешательства были эффективны у пациентов с ОИИ в результате окклюзии проксимального отдела артерии в каротидном бассейне .
В исследовании DAWN пациентов для эндоваскулярных вмешательств отбирали на основании наличия жизнеспособной ткани головного мозга по данным МСКТ и признаков клинического несоответствия тяжести неврологического дефицита и объема пораженного инфарктом мозга. Экспериментальной группе проводили ТЭ и стандартную медикаментозную терапию, в то время как контрольной группе проводили только стандартное медикаментозное лечение. Частота реканализации через 24 часа составила 77% в экспериментальной группе по сравнению с 39% в контрольной группе. При этом не было отмечено существенной разницы между экспериментальной и контрольной группами в отношении геморрагической трансформации (6% и 3% соответственно; р=0,50) или смертности (19% и 18% соответственно; р=1,00) .
Представленные клинические наблюдения подтверждают литературные данные о высокой эффективности ТЭ, в том числе в сочетании с ТЛТ (клинический случай 2), у пациентов с тромбозом крупной артерии каротидного бассейна и при наличии высокого сердечно-сосудистого риска (клинический случай 3).
6. Заключение
В рассмотренных случаях благоприятные ранние исходы ОИИ обусловлены своевременной и комплексной диагностикой патологии с помощью МСКТ, КТА и ДС интра- и экстракраниальных артерий, что позволило определить показания к проведению системного ТЛТ и ТЭ. Использование шкал NIHSS, Rankin и ШРМ показало клиническое и функциональное улучшение у всех пациентов при выписке.
