СРАВНЕНИЕ СПОСОБОВ ИММОБИЛИЗАЦИИ ПРОТЕОЛИТИЧЕСКОГО КОМПЛЕКСА BACILLUS SUBTILIS НА ХИТОЗАНЕ
Апалев П.В.1, Азаев М.Ш.2, Лебедев Л.Р.3
1Аспирант, 2доктор биологических наук, доцент, 3доктор медицинских наук,
Институт медицинской биотехнологии Федерального бюджетного учреждения науки Государственного научного центра вирусологии и биотехнологии «Вектор» Роспотребнадзора, Бердск, Новосибирская обл., Россия
СРАВНЕНИЕ СПОСОБОВ ИММОБИЛИЗАЦИИ ПРОТЕОЛИТИЧЕСКОГО КОМПЛЕКСА BACILLUS SUBTILIS НА ХИТОЗАНЕ
Аннотация
Исследованы способы активации матрицы – высокомолекулярного хитозана для последующей иммобилизации ферментов протеолитического комплекса из Bacillus subtilis. Для реакции активации использовались бензохинон, глутаровый альдегид и эпихлоргидрин. Показано, что применение для активации глутарового альдегида в технологии позволяет получать препараты иммобилизованных ферментов с более высокой удельной активностью и меньшими потерями. Выбраны технологические параметры синтеза препаратов иммобилизованных протеаз.
Ключевые слова: иммобилизация, хитозан, протеолитическая активность.
Apalev P.V.1, Azayev M.Sh.2, Lebedev L.R.3
1Postgraduate student, 2PhD in Biology, Associate professor, 3MD,
Institute of Medical Biotechnology of Federal Budgetary Institution of Science of State Research Center for Virology and Biotechnology "Vector" Rospotrebnadzor, Berdsk, Novosibirsk Region, Russia
COMPARISON OF IMMOBILIZATION METHODS OF PROTEOLITHIC BACILLUS SUBTILIS COMPLEX ON CHITOSAN
Abstract
The methods of activation of the matrix - high molecular weight chitosan for subsequent immobilization of enzymes of a proteolytic complex from Bacillus subtilis are investigated. Benzoquinone, glutaraldehyde and epichlorohydrin are used for the activation reaction. It is shown that the use of glutaraldehyde in the technology for the activation of the technology allows obtaining preparations of immobilized enzymes with a higher specific activity and lower losses. The technological parameters of synthesis of preparations of immobilized proteases were chosen.
Keywords: immobilization, chitosan, proteolytic activity.
Препараты, содержащие хитозан, применяются для лечения ран и ожогов [1], [2]. Хитозан способен стимулировать регенерацию кожи, регулируя пролиферацию фибробластов. Его бактерицидные свойства обусловлены способностью взаимодействовать с клеточной стенкой микроорганизмов [3]. Препараты на основе протеаз также используются для лечения гнойных ран в медицине и ветеринарной практике [4], [5]. Показано, что протеолитические ферменты обладают значительным противовоспалительным и противоотечным действием [6]. Представляет интерес разработка нового терапевтического средства, объединяющего два действующих начала – бактерицидный и ранозаживляющий эффекты, в одной композиции.
Наличие реакционно-способных функциональных групп в молекуле хитозана позволяет получать его конъюгаты с другими молекулами. Известны методы активации хитозана с применением глутарового альдегида, бензохинона, гидрохлорида этил (3-демитиламинопропил) карбодиимида, эпихлоргидрина для последующей иммобилизации различных ферментов [7]. При этом, получаемые по разным технологиям препараты, различаются по удельной активности иммобилизованных ферментов. При создании технологии производства комплексного препарата необходимо определить экономически наиболее эффективный метод его синтеза.
Целью исследования являлось сравнение методов иммобилизации комплекса протеаз из Bacillus subtilis на нерастворимой матрице - высокомолекулярном хитозане, для разработки технологии получения нового препарата с более высоким удельным содержанием ферментов.
Экспериментальная часть
В работе применяли: препарат «Протосубтилин Г3Х», ТУ 9291-029-13684916-2010 («Сиббиофарм»), порошок высокомолекулярного хитозана («Апифарм» или ЗАО Биопрогресс, Щёлково). Активность нейтральной протеазы определяли по методу Ансона [8], используя в качестве субстрата 2%-ый раствор казеина.
Уровень деацетилирования молекул хитозана определяли методом потенциометрического титрования [9]. В работе использовали: сорбент акрилекс Р-15 (Reanal, Венгрия), стеклянные фильтры (ПОР-16, ГОСТ 25336-82), эпихлоргидрин (Merk. Германия), отечественные реактивы (бензохинон, глутаровый альдегид, соли) квалификации «х.ч.».
Очистка ферментного комплекса для иммобилизации. Процедуру проводили аналогично как описано в работе Азаева М.Ш. [7]. По 7,5 г препарата «Протосубтилин Г3Х» растворяли в 30 мл 0,05 М натрий-фосфатного буфера, рН 7,6 (буфер А) в течение 10 - 15 мин. После удаления нерастворившихся компонентов центрифугированием (8000g, 20 мин) к надосадочной фракции добавляли 2 мл раствора хлористого кальция до конечной его концентрации 0,02 М при перемешивании. Через 15 - 20 мин сформировавшийся осадок удаляли центрифугированием. Для удаления из раствора ферментов низкомолекулярных окрашенных компонентов и солей проводили гель-хроматографию на колонке (75 мл) с акрилексом Р-15, используя буфер А. Получали по 30-32 мл комплекса протеолитических ферментов, содержащих по 185-200 мг белка с суммарной активностью нейтральной протеазы 720-780 ед.акт.
Активация хитозана. Для активации бензохиноном и глутаровым альдегидом четыре порции по 3 г порошка хитозана помещали на ночь в воду, затем на фильтрах промывали 0,2 М натрий-фосфатным буфером; рН 7,8 (буфер Б). Каждый образец суспендировали в 20 мл буфера Б.
К первым двум вносили 1 и 4 мл 25%-ого раствора глутарового альдегида (2,5 и 10 мМ) и перемешивали 5 ч при комнатной температуре. Ко вторым двум образцам добавляли по 2 мл 50%-ного раствора этанола, содержащего бензохинон, 0,25 и 1,1 г (2,5 и 10 мМ) и также перемешивали. Образцы активированного хитозана промывали буфером Б на фильтрах.
При активации с помощью эпихлоргидрина два образца хитозана (по 3 г), отмытые водой, суспендировали в 20 мл 0,5 Моль/л NaOH, содержащих по 50 мг боргидрида натрия. К первому добавляли 0,2 мл эпихлоргидрина, ко второму – 1 мл (2,5 и 10 мМ). После перемешивания в течение 5 ч при комнатной температуре образцы промывали буфером Б.
Иммобилизация ферментного комплекса. Каждую порцию активированной матрицы вносили в 10 мл раствора фермента (по 250 ед.акт. нейтральной протеазы). Инкубацию проводили 18 ч при температуре 6-80 С и слабом перемешивании на качалке. Полученные иммобилизованные комплексы последовательно промывали на стеклянных фильтрах растворами: 0,1 М Трис-HCl, рН 7,6. 0,5 М натрий-фосфат, рН 7,4 и раствором 0,01 М Трис-HCl, рН 7,4, содержащим 0,9%-ый NaCl. Количества иммобилизованного белка оценивали по разнице значений между исходным содержанием и суммарным белком в промывных жидкостях.
Изучение ранозаживляющего действия исследовали на модели термического ожога, по авторской методике Яковлевой Л.В. [10]. В эксперименте использовали крыс обоего пола линии Вистар массой 250–300 г по 6 животных в группе. Все работы с животными проводили строго в соответствии с «Правилами проведения работ с использованием экспериментальных животных», утвержденным Приказом МЗ СССР № 755 от 12.08.77 г., а также с положениями «Европейской конвенции по защите позвоночных, используемых для экспериментальных и иных научных целей» [11].
На выстриженном участке спины размером 3 х 3 см2 под барбамиловым наркозом (50 мг/кг, внутрибрюшинно) у животных вызывали термический ожог. Животных распределяли на две опытных группы. Крысам первой группы ожоговую рану лечили ежедневными аппликациями комплекса, полученного при использовании глутарового альдегида, крысам второй – аппликациями хитозана. Для аппликации использовали дозы из расчета 1 г влажного хитозана на 5 см2 раневой поверхности. Состояние раны регистрировали, проводя измерение ее площади, прикладывая к ране прозрачный трафарет. Общее состояние животных оценивали на основании поведенческих реакций, аппетита и массы тела.
Полученные цифровые данные обрабатывали статистически с использованием критерия Стьюдента [12. С.889-928] и с помощью пакета компьютерных программ «Statistica 6,0» (StatSoft Inc. 1984-2001). Результаты представляли как среднее значение ± стандартное отклонение (M±SM).
Результаты и их обсуждение
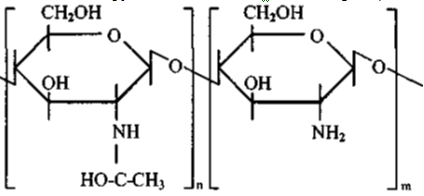
Хитозан представляет собой -(1-4)-2-амино-2дезокси-D-гликополисахарид, т.е. является аминополисахаридом, полученным при удалении части ацетильных групп из положения С2 в хитине (рис.1).
Рис. 1 – Структурная формула частично деацетилированного хитина
Степень деацетилирования используемого хитозана, определенная экспериментально, составляла 84-86%.
В эксперимент брали образцы по 3 г хитозана, что составляло по 15 мМ деацетилированных мономеров в каждом образце. Для активации хитозана использовали обработку его: 1) глутаровым альдегидом (2,5 и 10 мМ), 2) бензохиноном (2,5 и 10 мМ) и 3) эпихлоргидрином (2,5 и 10 мМ), как описано в экспериментальной части. Для иммобилизации использовали одинаковые количества раствора очищенного протеолитического комплекса. Полученные образцы иммобилизованных ферментов оценивались по массе и активности нейтральной протеазы (таблица 1).
Таблица 1 – Зависимость активности иммобилизованных протеаз от способа активации образцов хитозана
| Метод активации | Масса влажного комплекса | Активность нейтральной протеазы, ед.акт./г влажной массы | Суммарная активность иммобилизованной нейтральной протеазы, ед.акт |
| Глутаровый альдегид (2,5 мМ) (n=3) | 10,0±0,5 | 13,3±0,6 | 133±6* |
| Глутаровый альдегид (10 мМ) (n=5) | 10,0±0,5 | 16,8±0,8 | 168±8* |
| Бензохинон (2,5 мМ) (n=3) | 10,0±0,5 | 9,8±0,5 | 98±5 |
| Бензохинон (10 мМ) (n=5) | 10,0±0,5 | 10,8±0,6 | 108±6 |
| Эпихлоргидрин (2,5 мМ) (n=3) | 9,5±0,5 | 8,3±0,4 | 79±4 |
| Эпихлоргидрин (10 мМ) (n=3) | 9,4±0,5 | 9,2±0,5 | 86±5 |
Примечание: n – количество экспериментов
Символом (*) обозначены значения, статистически значимо отличающиеся от контроля (т.е. значений, полученных при активации бензхиноном и эпихлоргидрином (t test; P<0,05).
Из данных таблицы 1 видно, что при активации хитозана бензохиноном и эпихлоргидрином в условиях эксперимента удельная активность иммобилизованного протеолитического комплекса ниже, чем при активации с использованием глутарового альдегида. Это может быть связано как с неполной иммобилизацией белка, так и со снижением активности иммобилизованного фермента. Снижение массы комплекса при активации эпихлоргидрином можно объяснить частичным гидролизом молекул хитозана при его инкубации в щелочной среде. При соотношении в реакции глутарового альдегида 10 мМ на 15 мМ деацетилированных групп хитозана белок практически полностью переходил в иммобилизованное состояние и удельная активность нейтральной протеазы отмечалась до 17 ед.акт./г влажной массы. Активность иммобилизованного фермента сохранялась до 70% (170 ед.акт. от исходных 250).
После хранения в термостате при 370 С в течение 5 суток иммобилизованные ферменты сохраняли свою активность до 90%, что свидетельствует о прочности связи белка и молекул хитозана через аминогруппу последних.
Изучение ранозаживляющих свойств комплекса с активностью нейтральной протеазы 17 ед.акт./г влажной массы исследовали на модели термического ожога у крыс. В группе сравнения использовали влажный хитозан, промытый водой и 0,01 М раствором Трис-HCl, рН 7,4, содержащим 0,9%-ый NaCl. Результаты представлены в таблице 2.
Таблица 2 – Площадь раневой поверхности после термического ожога и последующего лечения, мм2
| Количество аппликаций | Комплекс (n=6) | Хитозан (n=6) | Контроль, без лечения (n=6) |
| Первый день | 134±28 | 142±28 | 120±23 |
| 5 аппликаций | 45±7 | 60±10 | 62±12 |
| 10 аппликаций | 3±3* | 3±2* | 26±5 |
| 15 день | 0 | 0 | 8±3 |
Примечание: n – количество животных в группе.
Символом (*) обозначены значения, статистически значимо отличающиеся от контроля (t test; P<0,05).
По значениям в таблице 2 видно, что поверхности ран у животных, которым проводили лечение комплексом протеаз, иммобилизованных на хитозане и хитозаном, достоверно отличается от результатов контрольной группы. Это свидетельствует о клинически более значимом эффекте данного комплекса. Наличие протеаз в комплексе предполагает ускоренное очищение и заживление ран, осложненных гнойными процессами, по сравнению с применением традиционной матрицы - хитозана.
Окончательное заживление ран у животных контрольной группы закончилось на 20±1 день эксперимента с образованием грубых рубцов, которые рассасывались достоверно медленнее (6±1 днь), чем в опытных группах (2±1 дня). И комплекс и его основа – хитозан, не вызывали изменений в двигательных реакциях крыс, не оказывали видимого токсического действия на организм животных в период наблюдения.
Выводы. Исследованы способы активации хитозана бензохиноном, глутаровым альдегидом и эпихлоргидрином. Показано, что в условиях эксперимента наиболее оптимален первый способ активации для получения комплекса с большей удельной активностью (16,8±0,8 ед.акт./г влажной массы) и выходом по иммобилизованной протеазе (до 70%).
Экспериментально выбраны параметры технологического процесса получения комплекса протеолитических ферментов из Bacillus subtilis, иммобилизованного на высокомолекулярном хитозане. Полученная субстанция может использоваться при разработке терапевтических препаратов для лечения ожогов и гнойных ран в форме мазей или гелей.
Список литературы/Refrences
- Федосов П.А. Изучение ранозаживляющего действия геля на основе хитозана с таурином и аллантоином / Федосов П.А., Сливкин А.И., Николаевский В.А. и др.// Современные проблемы науки и образования. – 2015. –№ 4. – С. 572.
- Гладкова Ю.К. Хитозан – свойства и перспективы применения // Бюллетень медицинских интернет-конференций. – 2015. – Т. 5. –№ 6. – С. 974.
- Rabea E.I. Chitosan as antimicrobial agent: applications and mode of action /Rabea E.I., Badawy M.E., Stevens C.V., et al. // Biomacromolecules. –2003. – № 4(6). – Р. 1457–1465.
- Ниязов Б.С. Современные представления о лечении гнойных ран / Б.С. Ниязов, Н.К. Абдылдаев, О.Р. Динлосан, С.Б. Ниязова // В сборнике: Материалы 3-ей междунар. заочной науч.-практ. конф. «Научный форум: медицина, биология и химия». – М., Изд. «МЦНО», 2017. – С. 38–49.
- Гуменная Е.Ю. Сравнительная терапевтическая эффективность протеолитических препаратов при гнойно-некротических заболеваниях у собак // Вестник Красноярского государственного аграрного университета. – 2003. – № 2 (2). – С. 103–105.
- Имозимаза – новый высокоэффективный препарат для лечения гнойно-воспалительных заболеваний у животных и человека [Электронный ресурс]. Режим доступа: https://goo.gl/PukSUk(дата обращения 10.12.2017).
- Азаев М.Ш. Субстанция протеолитического фермента на основе протосубтилина гзх, иммобилизованного на хитозане, и композиция для лечения гнойно-некротических ран / Азаев М.Ш., Волосникова Е. А., Лебедев Л. Р. // Патент России № 2630668. – 2017. – Бюл. № 26.
- ГОСТ 20264.2-88 Препараты ферментные. Методы определения протеолитической активности.
- Кучина Ю.А. Инструментальные методы определения степени деацетилирования хитина / Кучина Ю.А., Долгопятова Н.В., Новиков В.Ю. и др.// Вестник МГТУ. – 2012. – Т. 15. – №1. – С 107–113.
- Яковлева Л. В. Фармакологическое изучение новой ранозаживляющей мази "Пролидоксид" / Л. В. Яковлева, С. С. Кальф-Калиф, О. В. Ткачева // Провизор. – 1999. – № 1. – С. 44–45.
- Европейская конвенция о защите позвоночных животных, используемых для экспериментов или в иных научных целях (ETS N 123). – Страсбург. – 18 марта 1986 г.
- Руководство по проведению доклинических исследований лекарственных средств. Часть первая / Ред. кол.: Миронов А.Н., Бунятян Н.Д., Васильев А.Н. и др. – М.: Гриф и К, 2012. – 944 с.
Список литературы на английском языке / Refrences in English
- Fedosov P.A. Izucheniye ranozazhivlyayushchego deystviya gelya na osnove khitozana s taurinom i allantoinom [Study of Wound Healing Effect of Chitosan-based Gel with Taurine and Allantoin] / Fedosov P.A., Slivkin A.I., Nikolaevsky V.A. and others. Modern problems of science and education. - 2015. - No. 4. - P. 572. [In Russian]
- Gladkova Yu.K. Khitozan – svoystva i perspektivy primeneniya [Chitosan - Properties and Prospects of Application] // Bulletin of medical Internet conferences. - 2015. - V. 5. - No. 6. - P. 974. [In Russian]
- Rabea E.I. Chitosan as antimicrobial agent: applications and mode of action / Rabea E.I., Badawy M.E., Stevens C.V., et al. // Biomacromolecules. –2003. –No. 4(6). – Р. 1457–1465.
- Niyazov B.S. Sovremennyye predstavleniya o lechenii gnoynykh ran [Modern Ideas About Treatment of Purulent Wounds] / B.S. Niyazov, N.K. Abdyldaev, O.R. Dinlosan, S.B. Niyazova // Collection: Materials of 3rd international. extramural scientific conf. "Scientific forum: medicine, biology and chemistry". - M., Ed. "MCNO", 2017. - P. 38-49. [In Russian]
- Gumenaya E.Yu. Sravnitel'naya terapevticheskaya effektivnost' proteoliticheskikh preparatov pri gnoyno-nekroticheskikh zabolevaniyakh u sobak [Comparative Therapeutic Effectiveness of Proteolytic Drugs in Purulent-necrotic Diseases in Dogs] // Bulletin of Krasnoyarsk State Agrarian University. - 2003. - No. 2 (2). - P. 103-105. [In Russian]
- IMOZIMAZA - novyy vysokoeffektivnyy preparat dlya lecheniya gnoyno-vospalitel'nykh zabolevaniy u zhivotnykh i cheloveka [IMOZIMASE - New Highly Effective Drug for Treating Purulent-inflammatory Diseases in Animals and Humans] [Electronic resource]. Access mode: https://goo.gl/PukSUk (refference date 10.12.2017). [In Russian]
- Azayev M.Sh. Substantsiya proteoliticheskogo fermenta na osnove protosubtilina gzkh, immobilizovannogo na khitozane, i kompozitsiya dlya lecheniya gnoyno-nekroticheskikh ran [Substance of Proteolytic Enzyme Based on Protosubtilin Zinc Immobilized on Chitosan and Composition for Treatment of Purulent Necrotic Wounds] / Azaev M.Sh., Volosnikova E.A., Lebedev L.R. // Patent of Russia No. 2630668. - 2017. - Bul. No. 26. [In Russian]
- GOST 20264.2-88 Preparaty fermentnyye. Metody opredeleniya proteoliticheskoy aktivnosti. reparations Enzymatic. Methods for Determining Proteolytic Activity] [In Russian]
- Kuchina Yu.A. Instrumental'nyye metody opredeleniya stepeni deatsetilirovaniya khitina [Instrumental Methods for Determining Degree of Deacetylation of Chitin] / Kuchina Yu.A., Dolgopyatova N.V., Novikov V.Yu. and others. // Bulletin of the Moscow State Technical University. - 2012. - V. 15. - No.1. - P. 107-113.
- Yakovleva L.V. Farmakologicheskoye izucheniye novoy ranozazhivlyayushchey mazi "Prolidoksid" [Pharmacological Study of New Wound Healing Ointment "Prolidoxidum"] / L.V. Yakovleva, S.S. Kalf-Kalif, O.V. Tkacheva // Pharmacist. - 1999. - No. 1. - P. 44-45. [In Russian]
- Yevropeyskaya konventsiya o zashchite pozvonochnykh zhivotnykh, ispol'zuyemykh dlya eksperimentov ili v inykh nauchnykh tselyakh [European Convention for Protection of Vertebrates Used for Experimental or Other Scientific Purposes (ETS No. 123).] - Strasbourg. - March 18, 1986. [In Russian]
- Rukovodstvo po provedeniyu doklinicheskikh issledovaniy lekarstvennykh sredstv. Chast' pervaya [Guidelines for Preclinical Drug Research. Part One] / Ed. Kol .: Mironov A.N., Bunyatyan N.D., Vasiliev A.N. and others - M.: Grief and K, 2012. - 944 p. [In Russian]