МИНИДОСТУП В ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ПАПИЛЛЯРНОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ
Трунин Е.М.1, Татаркин В.В.2, Смирнов А.А.3, Клиценко О.А.4, Рыбаков В.А.5
1 доктор медицинских наук, профессор, 2,3 кандидат медицинских наук, 4 кандидат биологических наук, доцент, 5 Северо-Западный государственный медицинский университет им. И.И. Мечникова
МИНИДОСТУП В ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ ПАПИЛЛЯРНОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ
Аннотация
В работе, на основании топографо-анатомического эксперимента и клинического исследования рассмотрена возможность применения «плавающего» минидоступа в хирургическом лечении папиллярного рака щитовидной железы.
Ключевые слова: папиллярный рак щитовидной железы, тиреоидэктомия, минидоступ.
Trunin E.M.1, Tatarkin V.V.2, Smirnov A.A.3, Klitsenko O.A.4, Rybakov V.A.5
1 MD, professor, 2,3 MD, 4 PhD in Biology, Associate professor, 5 North-West State Medical University named after I.I. Mechnikov.
MINIMALLY INVASIVE APPROACH IN THE SURGICAL TREATMENT OF PAPILLARY THYROID CANCER
Abstract
In this work based on the topographic and anatomic experiment and clinical research the possibility of minimally invasive access used in surgical treatment of papillary thyroid cancer has been considered.
Keywords: papillary thyroid cancer, thyroidectomy, minimal access.
Актуальность:
Папиллярная карцинома щитовидной железы занимает первое место по частоте встречаемости в структуре злокачественных неоплазий эндокринных органов и имеет тенденцию к росту заболеваемости среди населения [4,5].
Диагностике и лечению этого заболевания посвящено множество рекомендаций различных тиреоидологических ассоциаций, но, тем не менее, вопросы о необходимой радикальности вмешательств остаются дискутабельными, так как, в отличии от опыта западных коллег, японские специалисты допускают выполнение органосохраняющих операций [7].
Стремительное развитие хирургии как высокотехнологичной специальности в последние десятилетия привело к высоким требованиям к косметическому результату операционного вмешательства, как к одному из основных факторов, влияющих на качество послеоперационной жизни пациентов, следовательно, минидоступ в хирургии папиллярного рака щитовидной железы применяется как адекватная замена традиционному доступу по Кохеру и альтернатива дорогостоящим, трудоёмким и доступным не всем стационарам эндовидеохирургическим операциям [2,6]..
Цели исследования:
- Доказать возможность применения минидоступа для операции в объеме тиреоидэктомии и претрахеальной лимфодиссекции.
- Оценить результаты хирургического лечения больных с папиллярным раком щитовидной железы, выполненного из минидоступа.
Материалы и методы:
Исследование состоит из двух разделов: топографо-анатомического эксперимента и клинического исследования.
Топографо-анатомический раздел исследования.
Топографо-анатомические исследования проведены на 50 нефиксированных трупах обоего пола, умерших от различных причин, не связанных с заболеваниями щитовидной железы (ЩЖ) (3 мужчин, 47 женщин) на базе патолого-анатомического отделения Городской больницы святой преподобномученницы Елизаветы (ГБ№3) Санкт-Петербург. Возраст умерших варьировал от 33 до 81 года, медиана по возрасту равна 54 годам.
В исследовании были задействованы 2 группы – основная и контрольная. Причем основная группа была разделена на две подгруппы: в 1-ой подгруппе тиреоидэктомию выполняли из ассиметричного доступа (18 трупов), во 2-ой подгруппе тиреоидэктомию проводили из срединного доступа (17 трупов). В контрольной группе, включавшей 15 трупов, тиреоидэктомию выполняли из доступа по Кохеру-Микуличу. Во всех группах провели оценку классических критериев операционного доступа по А.Ю. Созон-Ярошевичу (1954): направление оси операционного действия (НООД), угол наклона оси операционного действия (УНООД), угол операционного действия (УОД), глубина раны (ГР), площадь верхней апертуры и дна операционной раны, зона доступности, а также оценку адаптированных критериев для минимально инвазивных хирургических вмешательств по М.И. Прудкову (2007). В основной группе измерения выполняли для разрезов длиной 15, 20 и 25 мм. В контрольной группе оценка критериев была выполнена для разреза длинной 80 мм.
Клиническая часть исследования.
Клиническое исследование было основано на изучении результатов оперативного лечения 233 пациентов с предоперационным диагнозом «папиллярный рак щитовидной железы». Основная группа сформирована из 85 пациентов, оперированных из «плавающего» минидоступа. Контрольную группу составили 148 пациентов оперированных из классического хирургического доступа по Кохеру-Микуличу. Все пациенты проходили лечение на базе эндокринологического центра ГБ№ 3, в период с 1997 по 2015 гг.
Полученные в процессе выполнения работы анатомические и клинические результаты обрабатывались c использованием программной системы STATISTICA for Windows (версия 10 Лиц. BXXR310F964808FA-V).
Сопоставление частотных характеристик качественных показателей проводилось с помощью непараметрических методов c2, c2 с поправкой Йетса (для малых групп), критерия Фишера.
Сравнение количественных параметров, в т.ч. величины углов наклона оси операционного действия, соотношения площадей верхней и нижней апертур ран при различных разрезах и доступах осуществлялось с использованием критериев Манна-Уитни, медианного хи-квадрат и модуля ANOVA.
Результаты исследования:
Топографо-анатомическая часть исследования.
Направление оси операционного действия (НООД) оценивали при фиксированном положении головы оператора относительно исследуемого трупа. Этот критерий не измеряли количественно, а определяли при горизонтальном положении тела как направление спереди-назад, сверху-вниз, справа-налево (слева-направо). При этом направление оси операционного действия при классическом доступе и минидоступе были индентичными (Рис. 1). При использовании методики «плавающего доступа» ось операционного действия незначительно смещалась вслед за смещением верхней апертуры раны, что не отражалось на её направлении. Длина разреза при выполнении доступа, также не влияла на направление оси операционного действия.
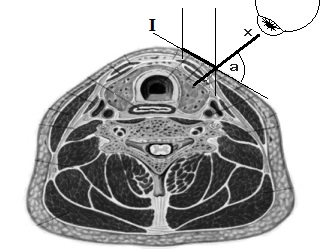 |
х – ось операционного действия (ООД) I – плоскость верхней апертуры a – угол наклона оси операционного действия (УНООД) |
| Рис. 1. Направление и угол наклона оси операционного действия. | |
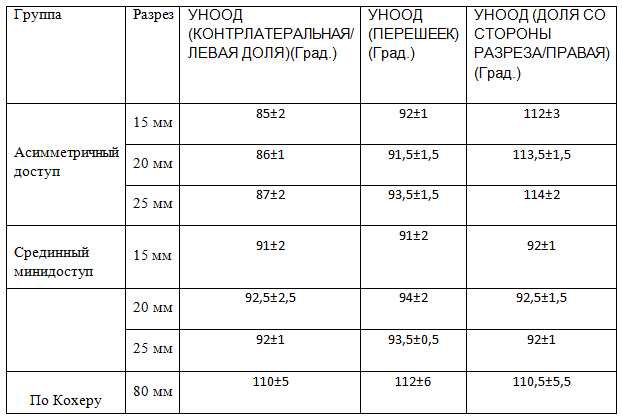
Углы наклона оси операционного действия измеренные в основной и контрольной группах представлены в таблице (Таб. 1).
Таблица 1. Величина угла наклона оси операционного действия (УНООД) в группах исследования.
Из полученных результатов следует, что величина УНООД при выполнении минидоступов приближается к величине 900, что является оптимальным углом зрения. Длина разреза на величину УНООД практически не влияла.
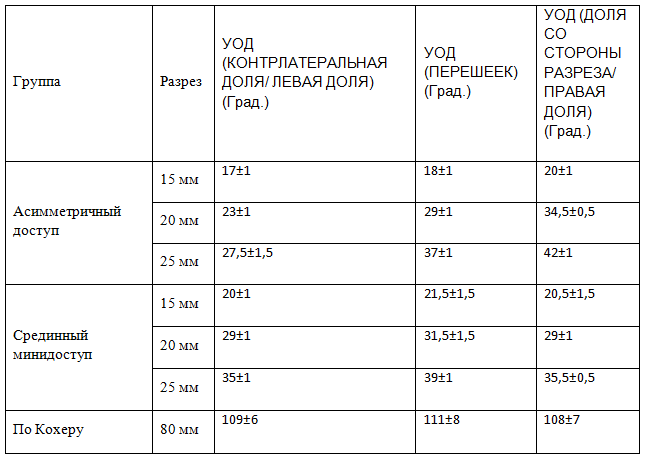
В основной группе было выполнено измерение угла операционного действия (УОД) для разрезов длиной 15 мм, 20 мм и 25 мм. В контрольной группе были выполнены измерения для разреза длиной 80 мм (Таб. 2).
Таблица 2. Величина угла операционного действия (УОД) в группах исследования.
Для разрезов длиной 20 и 25 мм получены величины УОД более 250. Это указывает на то, что при разрезе длинной от 20 до 25 мм, манипуляции в ране не вызывают затруднений. В первой подгруппе при расположении разреза над долей, содержащей узел и длине разреза 15 мм УОД над контрлатеральной долей имел величину 170. При такой величине УОД манипуляции в ране возможны, но ограничены. Следует отметить, что значении УОД в 160 и менее, когда манипуляции в ране практически невозможны в наших исследованиях получено не было. В контрольной группе величина УОД составили более 900. При такой величине УОД, оперативное вмешательство выполняется без затруднений (Рис. 2).
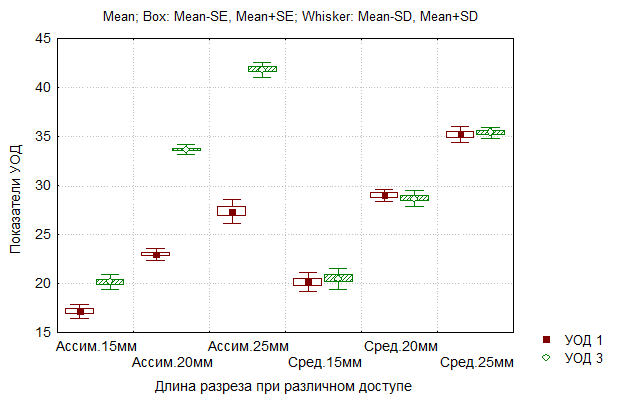
Таким образом, измерение УОД, в исследуемых группах, показало что оптимальной следует признать длину разреза не менее 15 мм, при меньшей длине разреза возможности доступа становятся ограниченными и манипуляции в ране практически невозможны.
Рис. 2. Сравнительные показатели УОД при различных длинах разрезов.
Необходимо отметить, что извлечение из раны органа или его части на одном из этапов операции меняет условия выполнения вмешательства. В этом случае угол операционного действия может превышать 1800. Чем ближе объект операции располагается (или подтягивается в процессе вмешательства) к верхней апертуре, тем больше величина УОД и соответственно тем лучше условия оперирования. Длина разреза при этом не влияет на величину УОД. Выведение доли ЩЖ возможно после мобилизации верхнего и нижнего полюсов доли, пересечения перешейка и перевязки средних щитовидных вен. В этом случае доля ЩЖ может быть извлечена из раны, а находящиеся позади доли ветви нижней щитовидной артерии могут быть пересечены без технических трудностей под визуальным контролем. Геометрию раны и УОД можно улучшить с помощью ранорасширителей. Однако надо принимать во внимание, что излишнее растяжение раны приводит к травматизации краёв кожи, что впоследствии может повлиять на процесс формирования кожного рубца и косметический результат операции.
Глубину раны (ГР) определяли по оси конуса, являющейся также и осью операционного действия (ООД). Этот показатель характеризует возможность выполнения вмешательств стандартными хирургическими инструментами. Глубина раны при доступе к щитовидной железе, также зависит от степени разгибания шеи. Глубина раны так же напрямую зависит от толщины рассекаемых слоёв. При использовании минидоступа и стандартного доступа в области шеи величина ГР одинакова. В основной группе среднее значение ГР составило 45±3 мм (M±m), в контрольной группе 47±4 мм (M±m). Полученные данные о ГР в основной группе исследования говорят о возможности работать в ране стандартными хирургическими инструментами. Следует отметить, что при моделируемых оперативных вмешательствах удобнее для манипуляций следует использовать инструменты с небольшой длиной браншей и толщиной губок, а также соответствующие ранорасширители с небольшой шириной и длиной изогнутой части. Исследования показали, что стандартные хирургические инструменты позволяют проводить необходимые манипуляции в ране в условиях минидоступа.
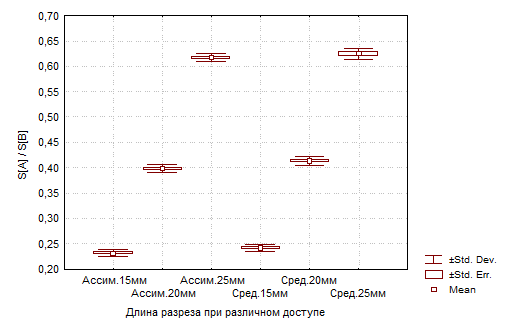
Форма раны, при моделировании вмешательства из минидоступа отличалась от цилиндрической и напоминала усечённый конус большим основанием вниз. Следовательно площадь дна раны S[ДР] превышала площадь верхней апертуры S[ВА]. В контрольной группе рана по форме, напротив, представляла собой усечённый конус широким основанием вверх.
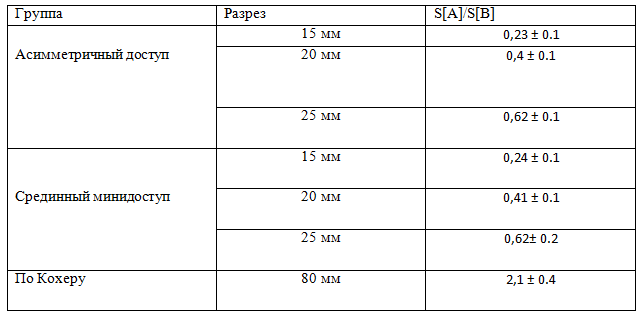
Таблица 3. Соотношения площадей верхней и нижней апертур ран.
Рис. 3 Соотношения площадей верхней и нижней апертур ран.
Полученные данные указывают на то, что в контрольной группе при традиционном доступе соотношение площади верхней апертуры и дна раны превышает потребности хирурга. При рациональном доступе это соотношение должно приближаться к единице. Необходимое соотношение выдерживается при выполнении минидоступа всех исследованных его величин (Таб.3).
Для формирования «плавающего доступа» на передней поверхности шеи, обеспечивающего доступ к большей по площади зоне доступности, используется эффект повышенной смещаемости кожи в этой анатомической области при разрезе кожи длиной 15 и 20 мм. Смещение верхней апертуры раны ЩЖ составило (M±m): вверх (Up) 16,5±0,8 мм; смещение вниз (Down) - 16,7±0,9 мм; смещение влево (Left) – 17,1±0,7 мм; смещение вправо (Right) – 18,3±0,8 мм. К верхнему полюсу левой доли (UpL) верхняя апертура раны смещалась на 15,7±0,9 мм, к верхнему полюсу правой доли (UpR) верхняя апертура раны смещалась на 18,6±0,8 мм, к нижнему полюсу левой доли (DL) на 15,9±0,8 мм и к нижнему полюсу правой доли (DR) верхняя апертура раны смещалась на 18,9±0,6 мм. (Рис. 3.)
Снижение тургора кожи на трупном материале несколько ограничивало подвижность верхней апертуры раны. Однако даже на нефиксированных трупах смещение апертуры оказывалось достаточным для полноценной визуализации верхних и нижних полюсов долей ЩЖ, а также претрахеальной клетчатки.
Адаптированные критерии оценки минидоступа.
Значительные отличия миниинвазивных доступов от классических, требуют внесения изменений в критерии оценки [3]. Особенностью многих минимально инвазивных доступов является преобладание глубины раны над длиной разреза. Средняя глубина раны в наших исследованиях составила 45 ± 3 мм. При длине разреза от 15 до 25 мм глубина значительно преобладает над длиной, а при длине разреза 80 мм длина разреза превышает глубину раны. В изученных нами доступах ось наблюдения полностью совпадает с осью операционного действия. При минимально инвазивных операциях объём и форма операционного пространства отличаются от классических цилиндрических и конических форм. В наших исследованиях доступ напоминает низкую колбу с широким основанием. Такая форма доступа признана наиболее оптимальной, так как имеющееся пространство над зоной доступности определяет достаточную свободу манипуляций. При смещении верхней апертуры раны, форма операционного пространства меняется, но объем операционного пространства остаётся прежним. Доступность не уменьшается, а даже улучшается, за счёт перемещения верхней апертуры непосредственно к зоне вмешательства. В наших исследованиях в основной группе величина УОДК (450) была меньше УОДЭ (1200) при любой длине разреза. При этом величина УОДЭ всегда была достаточно велика, так как глубина раны при моделируемом вмешательстве на ЩЖ небольшая. Относительно критерия УОДЭ доступ также является адекватным. При смещении верхней апертуры раны к краю зоны доступности, происходило изменение величины УОДЭ, при неизменной величине УОДК (500). При этом свобода манипуляций в ране определялась перемещением верхней апертуры к зоне вмешательства и величиной УОДК, а не величиной УОДЭ.
При оценке критериев операционного минидоступа к ткани ЩЖ установлено, что согласно классическим критериям оценки доступа и модифицированным критериям оценки для минидоступа, исследуемый минидоступ может быть успешно применен в клинической практике, для проведения вмешательства в объеме тиреоидэктомия и претрахеальной лимфодиссекции.
Клиническая часть исследования:
С диагнозом «папиллярный рак» нами было оперировано 233 больных. Результаты хирургического лечения этих больных рассмотрены в 2-х группах: основной – 85 пациентов оперированых из минидоступа и контрольной – 148 пациентов оперированых из классического доступа по Кохеру-Микуличу. Группы были сопоставимы по возрасту (P>>0,05). Возраст пациентов основной группы был 53,3±1,7 лет, медиана 51,0 год. Для оперированных из классического доступа по Кохеру-Микуличу - 53,6±1,1 лет, медиана 54,5. В обеих группах сопоставимо доминировали женщины. При доступе по Кохеру их было 92,6% (137), при минидоступе 91,8% (78). Мужчин соответственно 7,4% (11) и 8,2% (7).
С предоперационным цитологическим заключением «папиллярный рак» было оперировано 147 человек, из них в основной группе – 67 пациентов; в контрольной – 80 пациентов. Пациенты с рецидивной формой зоба в эти группы включены не были. В основной группе оперированы пациенты с узлами до 25 мм, у которых не был увеличен объем щитовидной железы и отсутствовали данные за экстратиреоидный рост опухоли. Лимфатические узлы шеи у этих больных увеличены не были. Длина минидоступа составила 15-25 мм, в среднем 20 мм. Среднее время оперативного вмешательства – 45 - 98 ±11,2 мин. Дренирования раны не выполняли. Края кожной раны фиксировали с помощью цианакрилатного клея или накладывали внутрикожный шов рассасывающимся атравматическим шовным материалом. Длительность послеоперационного пребывания пациентов в стационаре не превышала 2 суток. Исключение составили 14 больных с послеоперационными осложнениями. У 5 имел место односторонний парез гортани, у 1 пациента - двусторонний парез гортани. У 7 отмечен транзиторный гипопаратиреоз. Срок их наблюдения в стационаре до 4-х суток. Следует отметить, что максимальный процент оперированных больных основной группы, у которых отмечено повреждение возвратного гортанного нерва пришелся на период освоения методики (в первые 6 месяцев). Нагноений послеоперационной раны отмечено не было. Кровотечения в раннем послеоперационном периоде имело место у 1 больного. Летальных исходов отмечено не было.
В контрольной группе выполняли доступ по Кохеру-Микуличу. Длина кожного разреза составила 60 - 110 мм, в среднем 80 мм. Среднее время оперативного вмешательства - 58 - 100±8,1 мин. Длительность послеоперационного пребывания пациентов в стационаре не превышала 3 суток. Исключение составили 12 больных с послеоперационными осложнениями (5 пациентов – односторонний парез гортани, 6 пациентов – транзиторный гипопаратиреоз, 1 пациент – кровотечение в раннем послеоперационном периоде). Это послужило причиной более длительного пребывания пациента в стационаре (до 5 суток).
Повторное оперативное вмешательство по поводу папиллярного рака щитовидной железы, установленного при гистологическом исследовании препарата, в основной группе произведено у 6 пациентов (7,1%), а при доступе по Кохеру частота повторных операций составила – 12,8% - 19 человек. Однако эти различия были не достоверны (P>>0,05). В основной группе показаниями к повторному оперативному вмешательству послужили – папиллярный рак щитовидной железы при объеме первичной операции менее тиреоидэктомии (5 пациентов). Выявление во время наблюдения до 1 года после первичного вмешательства поражения региональных лимфатических узлов и наличие остаточной ткани в ложе щитовидной железы (2 случая). В поздние сроки наблюдения (более 1 года после первичного оперативного вмешательства), прогрессирование рака в виде метастазирования в регионарные лимфатические узлы шеи было выявлено в 1 случае.
В контрольной группе повторное вмешательство было произведено в 19 случаях. Показаниями к повторному вмешательству так же послужили – папиллярный рак щитовидной железы при объеме первичного оперативного вмешательства менее тиреоидэктомии (12 пациентов). Выявление во время динамического наблюдения до 1 года после первичного оперативного вмешательства метастазов в регионарные лимфатические узлы и наличие остаточной ткани в ложе щитовидной железы (4 случая). В поздние сроки наблюдения прогрессирование рака и метастазирование в регионарные лимфатические узлы было выявлено в 2 случаях.
Таким образом, миниинвазивный хирургический доступ позволяет проводить радикальное оперативное вмешательство при папиллярном раке щитовидной железы. В случае проведения адекватного предоперационного отбора больных результаты вмешательства по количеству осложнений, и наличию рецидивов заболевания в сроки наблюдения до 1 года не уступают таковым при классической форме хирургического доступа. А меньшая инвазивность доступа позволяет уменьшить койко-день до 1 суток.
Выводы.
- Согласно количественным критериям оценки операционных доступов, минидоступ на передней поверхности шеи адекватен для проведения оперативного вмешательства на щитовидной железы в объёме до тиреоидэктомии с претрахеальной лимфодиссекцией.
- Применение минидоступа в хирургическом лечении папиллярного рака снижает операционную травму, создаёт условия для ранней выписки и дает благоприятный косметический результат.
Литература
- Гутковский Ю.П. Малый асимметричный доступ в хирургии узлового зоба / Ю.П. Гутковский, С.И. Кижватов, Е.В. Рябченко // Актуальные проблемы прикладной анатомии, оперативной и клинической хирургии. Сборник трудов Российской научной конференции, посвященной 75-летию з.д.н. проф. Симбирцева С.А. – СПб.: Изд.дом СПбМАПО, 2004. – С.108-10
- Егиев В.Н., Рудакова М.Н., Воскресенский П.К. и др.; Хирургия «малых пространств» / под ред. В.Н. Егиева. - М.: Медпрактика-М, 2003. - 56 с.
- Прудков М.И. Основы минимально инвазивной хирургии / М.И. Прудков. - Екатеринбург, 2007. – 58 с.
- Minimally invasive, nonendoscopic thyroidectomy: A cosmetic alternative to robotic-assisted thyroidectomy / Cara M. Govednik, MD, Samuel K. Snyder, MD, Courtney E. Quinn, MD, Saurabh Saxena, BS, and Daniel C. Jupiter, PhD // Surgery. – 2014. - Volume 156, Number 4. - P.1030 – 1038.
- Результаты хирургического этапа лечения папиллярного рак щитовидной железы / Черников Р.А., Воробьев С.Л., Слепцов И.В., Семенов А.А., Чинчук И.К., Макарьин В.А., Куляш А.Г., Успенская А.А., Тимофеева Н.И., Новокшонов К.Ю., Карелина Ю.В., Федоров Е.А., Малюгов Ю.Н., Федотов Ю.Н., Бубнов А.Н.// Клиническая и экспериментальная тиреоидология. – 2014. – том 10, №2 – С. 38-42.
- Yoshida A. Guideliness for the management of thyroid tumors / Yoshida A. // Nihon Geka Gakkai Zasshi – 2012 - 113(6) – P.507-511.
- Abboud B. Surgical treatment of papillary thyroid carcinoma / Abboud B,Tannoury J. // J Med Liban – 2011 - Volume 59, Issue 4- 206-212.
References
- Gutkovskij Ju.P. Malyj asimmetrichnyj dostup v hirurgii uzlovogo zoba / Ju.P. Gutkovskij, S.I. Kizhvatov, E.V. Rjabchenko // Aktual'nye problemy prikladnoj anatomii, operativnoj i klinicheskoj hirurgii. Sbornik trudov Rossijskoj nauchnoj konferencii, posvjashhennoj 75-letiju z.d.n. prof. Simbirceva S.A. – SPb.: Izd.dom SPbMAPO, 2004. – S.108-10
- Egiev V.N., Rudakova M.N., Voskresenskij P.K. i dr.; Hirurgija «malyh prostranstv» / pod red. V.N. Egieva. - M.: Medpraktika-M, 2003. - 56 s.
- Prudkov M.I. Osnovy minimal'no invazivnoj hirurgii / M.I. Prudkov. - Ekaterinburg, 2007. – 58 s.
- Minimally invasive, nonendoscopic thyroidectomy: A cosmetic alternative to robotic-assisted thyroidectomy / Cara M. Govednik, MD, Samuel K. Snyder, MD, Courtney E. Quinn, MD, Saurabh Saxena, BS, and Daniel C. Jupiter, PhD // Surgery. – 2014. - Volume 156, Number 4. - P.1030 – 1038.
- Rezul'taty hirurgicheskogo jetapa lechenija papilljarnogo rak shhitovidnoj zhelezy / Chernikov R.A., Vorob'ev S.L., Slepcov I.V., Semenov A.A., Chinchuk I.K., Makar'in V.A., Kuljash A.G., Uspenskaja A.A., Timofeeva N.I., Novokshonov K.Ju., Karelina Ju.V., Fedorov E.A., Maljugov Ju.N., Fedotov Ju.N., Bubnov A.N.// Klinicheskaja i jeksperimental'naja tireoidologija. – 2014. – tom 10, №2 – S. 38-42.
- Yoshida A. Guideliness for the management of thyroid tumors / Yoshida A. // Nihon Geka Gakkai Zasshi – 2012 - 113(6) – P.507-511.
- Abboud B. Surgical treatment of papillary thyroid carcinoma / Abboud B,Tannoury J. // J Med Liban – 2011 - Volume 59, Issue 4- 206-212.