ЭФФЕКТЫ ВЫРЕЗАНИЯ ОБЪЕМА ИОНА И ПЕРЕЭКРАНИРОВАНИЯ ДИЭЛЕКТРИЧЕСКОЙ ФУНКЦИИ РАСТВОРИТЕЛЯ В НЕЛОКАЛЬНО-ЭЛЕКТРОСТАТИЧЕСКОЙ ТЕОРИИ СОЛЬВАТАЦИИ
Рубашкин А.А.1, Конев Д.В.2, Цыганов А.Б.3
1ORCID: 0000-0002-9054-0574, Кандидат химических наук, Институт цитологии РАН, Санкт-Петербург, 2Кандидат химических наук, Институт проблем химической физики РАН, Черноголовка, 3ORCID: 0000-0003-2245-3097, Кандидат физико-математических наук, ООО «Интро-Микро», Санкт-Петербург
Работа выполнена при поддержке гранта РФФИ № 14-03-00221
ЭФФЕКТЫ ВЫРЕЗАНИЯ ОБЪЕМА ИОНА И ПЕРЕЭКРАНИРОВАНИЯ ДИЭЛЕКТРИЧЕСКОЙ ФУНКЦИИ РАСТВОРИТЕЛЯ В НЕЛОКАЛЬНО-ЭЛЕКТРОСТАТИЧЕСКОЙ ТЕОРИИ СОЛЬВАТАЦИИ
Аннотация
В статье рассмотрено развитие нелокально-электростатической теории сольватации ионов, учитывающей переэкранирование диэлектрической функции растворителя, на случай, когда учитывается эффект вырезания растворителя из объема, занятого ионом. Рассчитанная энергия сольватации иона в этой модели сравнивается с расчетом по теории (J. Chem. Phys., 1996), в которой не учитывается эффект вырезания. Развитая теория объясняет различие энергий сольватации катионов щелочных металлов и анионов галоидов одинакового радиуса.
Ключевые слова: энергия сольватации, эффект переэкранирования, диэлектрическая функция растворителя, нелокальная электростатика.Rubashkin A.A.1, Konev D.V.2, Tsyganov A.B.3
1ORCID: 0000-0002-9054-0574, PhD in Chemistry, Institute of Cytology, Russian Academy of Sciences, Saint-Petersburg, Russia, 2PhD in Chemistry, Institute of Problems of Chemical Physics, Russian Academy of Sciences, Chernogolovka, Moscow region, Russia, 3ORCID: 0000-0003-2245-3097, PhD in Physics and mathematics, Intro-Micro LLC, Saint-Petersburg
EFFECTS OF CUT-OUT ION VOLUME AND OVERSCREENING OF DIELECTRIC FUNCTION OF THE SOLVENT IN THE NONLOCAL ELECTROSTATICS SOLVATION THEORY
Abstract
The article considers the development of nonlocal electrostatic theory of ion solvation in the case when taken into account the effect of cut-out the ion volume from solvent and the overscreening of dielectric function of solvent. The calculated energy of ion solvation in this model is compared with the calculation on theory (J. Chem. Phys., 1996), which does not take into account this effect. The theory developed explains the difference in solvation energies of alkali metal cations and anions of halogens of the same radius.
Keywords: solvation energy, overscreening effect, dielectric function of solvent, nonlocal electrostatics.В предыдущей работе [1] мы рассматривали роль комбинации эффектов вырезания объёма иона и размытия его заряда за пределы борновской сферы в расчёте электростатической составляющей энергии сольватации. При этом в [1] для диэлектрической функции растворителя были выбраны полюсные модели. В настоящей работе рассматривается эффект переэкранирования диэлектрической функции [2] в комбинации с двумя вышеназванными эффектами. В [3, 4] мы рассчитывали энергию сольватации иона для случая комбинации эффекта переэкранирования диэлектрической функции растворителя с эффектом размывания заряда иона за пределы его борновской сферы. При этом эффект вырезания объёма иона не учитывался, как и в работе [2].
Расчет энергии сольватации в модели с переэкранированием диэлектрической функции растворителя.
Электростатическая составляющая энергии сольватации иона W для сферически-симметричного распределения заряда иона радиуса ri согласно теории [5] рассчитывается по формуле (1)
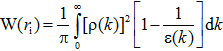 (1)
(1)
В настоящей работе используется диэлектрическая функция растворителя εOS(k), учитывающая эффект переэкранирования [2]:
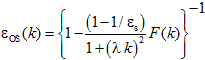 (2)
(2)
где: аббревиатура “OS” означает “overscreening” – переэкранирование; εs = 78.8; λ – подгоночный параметр модели; F(k) – вспомогательная функция:
![]() (3)
(3)
Используемые нами параметры в (2)-(4) соответствуют BKLS модели [2, с. 1526]: A = 50, B = 5, λ = 0.15, α = 0.8, κ = 3 (все размерности: Å-1), Λ = 3 Å.
Впервые рассмотрение эффекта вырезания объёма иона из растворителя в нелокальной электростатике было введено в работе [6], а в монографии содержится [7] изложение методов нелокальной электростатики.
В [1] нами был разработан метод расчета энергии сольватации иона WVR для случая, когда имеется комбинация эффект вырезания объема иона из растворителя с эффектом проникновения части заряда иона за пределы его борновской сферы. Однако в [1] не приводились результаты расчёта для ε(k) c эффектом переэкранирования. В данной работе мы представляем результаты расчёта с эффектом переэкранирования. Формулы для ρ(k), которые надо подставлять в формулу (1) были приведены в [1].
Определение параметров размытого распределения заряда, при которых рассчитанные W для катионов щелочных металлов и анионов галоидов совпадают с экспериментальными данными работы Маркуса [10]
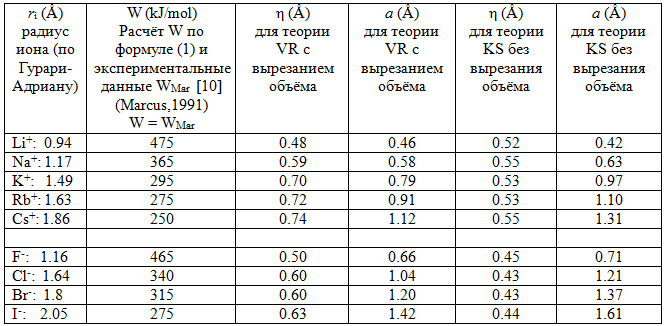
В таблице 1 приведены значения параметров SBS модели [2] (a – координата максимума плотности распределения заряда иона и η – ширина размытия заряда), для которых расчёт энергии сольватации ионов по формуле (1) даёт значения W, приведённые во второй колонке. Эти значения W совпадают с WMar – энергиями сольватации из статьи Маркуса [10]. При расчёте использовалась диэлектрическая функция, учитывающая эффект переэкранирования (формулы (2)-(4)), а её параметры была приведены после формулы (4) (BKLS модель).
Таблица 1 - Расчёт энергий сольватации W для катионов щелочных металлов и анионов галоидов. Расчёт выполнен для одномодовой модели диэлектрического отклика, учитывающей эффект переэкранирования при размытом распределении заряда иона (SBS)
На рис. 1 приведены результаты расчёта энергии сольватации для катиона натрия и для аниона фтора при варьировании модельного параметра ширины размывания заряда иона. Сплошная кривая (VR) – расчёт по нашей теории [1], учитывающей эффект вырезания объёма иона; штриховая кривая (KS) – расчёт по теории работы [2], не учитывающей вырезание объёма иона. Приведён расчёт для Na+ и F-, причём в виду близости их радиусов кривая для WNa на графике не отличается от кривой для WF. Значения параметра η в таблице 1 найдены из пересечения кривых на Рис. 1 с пунктирными линиями, соответствующими экспериментальным данным Маркуса [10]. Для нахождения параметров в таблице 1 для других ионов нами были построены аналогичные графики для каждого из них.
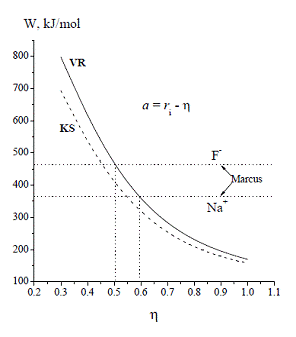
Рис. 1 - Энергия сольватации ионов W (кДж /моль) в зависимости от ширины размытия η (Å) плотности заряда иона ρ(r) в SBS модели [2]. Координата a максимума ρ(r) связана с радиусом иона как: a = ri – η. Кривые VR и KS рассчитаны для диэлектрической функции (2)-(4), учитывающей эффект переэкранирования
На Рис.2 представлены энергии сольватации W катионов щелочных металлов и анионов галоидов, рассчитанные нами как по нашей теории [1], учитывающей эффект вырезания объёма иона, так и по теории работы [2], не учитывающей вырезание объёма иона. Параметры, использованные для расчёта, приведены в таблице 1. Расчётные величины W совпадают с экспериментальными данными Маркуса [10].
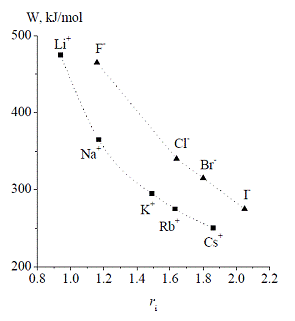
Рис. 2 - Рассчитанные энергии сольватации W (кДж /моль) для катионов щелочных металлов и анионов галоидов для параметров таблицы 1
Как видно из Рис. 2 расчёт энергии сольватации для катионов и анионов близкого радиуса (Na+ и F-, Rb+ и Cl- ) приводит к разным значениям W. При этом ширина размывания заряда иона для катионов больше, чем для анионов (см. таблицу 1). Этот результат справедлив как для расчёта по нашей теории с учётом эффекта вырезания объёма, так и для расчёта по теории, не учитывающей этого эффекта. Однако для расчётов по нашей теории надо выбрать большие значения параметра размытия. Отметим, что согласно работе [11] невозможно в рамках расчётов по нелокально-электростатической теории объяснить различие энергии сольватации для катионов щелочных металлов и анионов галоидов одинакового радиуса.
Для приложения развитой нами теории к транспорту ионов через мембраны животных клеток особое значение имеет расчёт W катионов натрия и калия. Поэтому в таблице 2 мы приводим значения параметров η для этих катионов, расчёты W для которых совпадают с экспериментальными данными работ [9-10] и [12-13]. Во всех случаях величина η, рассчитанная по теории с вырезанием объёма больше, чем для расчёта по теории, не учитывающей этого эффекта.
Таблица 2 - Расчёт параметров размытия плотности заряда иона η в SBS модели для Na+ и K+ соответствующих экспериментальным значениям энергии сольватации работ Фосета и Маркуса [9-10], а также Рэндлеса и Саломона [12-13]
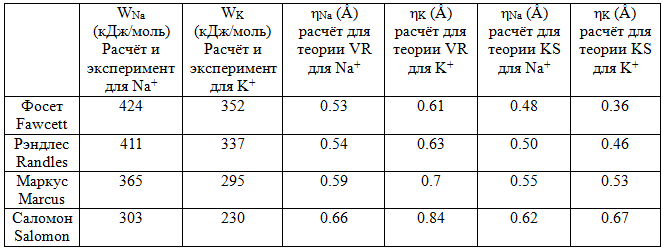
Основным выводом работы является то, что, пользуясь нелокально-электростатической теорией, можно объяснить различие энергий сольватации катионов щелочных металлов и анионов галоидов одинакового радиуса.
Список литературы / References
- Рубашкин А. А. Эффекты вырезания объёма иона и проникновения заряда иона в растворитель в нелокально-электростатической теории сольватации для полюсных моделей диэлектрической проницаемости растворителя / А. А. Рубашкин, Д. В. Конев, М. А. Воротынцев // Международный научно-исследовательский журнал. – 2016. – № 5 (47). - Часть 5. – С. 112-115. doi: 10.18454/IRJ.2016.47.106
- Kornyshev A. A. The shape of the nonlocal dielectric function of polar liquids and the implications for thermodynamic properties of electrolytes: A comparative study / A. A. Kornyshev, G. Sutmann // J. Chem. Phys. – 1996. – Vol. 104. – P. 1524-1544.
- Рубашкин А. А. Нелокально-электростатическая теория ионной сольватации: комбинация эффекта переэкранирования в диэлектрическом отклике среды с размытым распределением заряда иона / А. А. Рубашкин, М. А. Воротынцев, Е. М. Антипов и др. // ДАН. – 2015. – Т. 464. - № 1. – С. 56-60.
- Rubashkin A. A. Electrostatic contribution to the ion solvation energy: overscreening effect in the nonlocal dielectric response of the polar medium / A. A. Rubashkin, M. A. Vorotyntsev // Curr. Phys. Chem. – 2016. – V. 6(2). – P. 120-129.
- Dogonadze R. Polar-solvent structure in theory of ionic solvation / R. Dogonadze, A. A. Kornyshev // J. Chem. Soc. Faraday Trans. Pt.II. – 1974. - V. 70. – P. 1121-1132.
- Vorotyntsev M.A. Model nonlocal electrostatics. II. Spherical interface / M. A. Vorotyntsev // J. Phys. C: Solid State Physics – 1978. - V. 11. – P. 3323-3331.
- Воротынцев М. А. Электростатика сред с пространственной дисперсией / М. А. Воротынцев, А. А. Корнышев - М. : Наука, 1993 - 240 с.
- Gourary B. S. Wave function for electron-excess color centers in alkali halide crystals / B. S. Gourary, F. J. Adrian // Solid State Phys. – 1960. - V. 10. – P. 127-247.
- Fawcett W. R. Thermodynamic parameters for the solvation of monatomic ions in water / W. R. Fawcett // J. Phys. Chem. – 1999 - V. 103. – P. 11181-11185.
- Marcus Y. Thermodynamics of Solvation of Ions. Part 5 - Gibbs Free Energy of Hydration at 298.15 K / Y. Marcus // J. Chem. Soc. Faraday Trans. – 1991 - V. 87(18) – P. 2995-2999.
- Fedorov M. V. Unravelling the solvent response to neutral and charged solutes /V. Fedorov, A. A. Kornyshev // Molecular Physics – 2007 – V. 105 – P. 1-16.
- Randles J. E. B. The real hydration energies of ions / J. E. B. Randles // Trans. Faraday Soc. – 1956 – V. 52 – P. 1573-1581.
- Salomon M. Thermodynamics of ion solvation in water and propylene carbonate /Salomon // J. Phys. Chem. B – 1970 – V. 74 (12) – P. 2519-2524.
Список литературы на английском языке / References in English
- Rubashkin A.A. Effects of cut-out ion volume and of penetration of the ion charge to the solvent in the nonlocal electrostatics solvation theory for the pole models of dielectric function of the solvent / A. A. Rubashkin, D. V. Konev, M. A. Vorotyntsev // International research journal – 2016. – № 5(47). - Part 5. – P. 112-115. doi: 10.18454/IRJ.2016.47.106
- Kornyshev A. A. The shape of the nonlocal dielectric function of polar liquids and the implications for thermodynamic properties of electrolytes: A comparative study / A. A. Kornyshev, G. Sutmann // J. Chem. Phys. – 1996. – Vol. 104. – P. 1524-1544. Международный научно-исследовательский журнал ▪ № 11 (53) ▪ Часть 2 ▪ Ноябрь 171
- Rubashkin A. A. Nonlocal-electrostatics theory of ion solvation: combination of the overscreening effect in the dielectric response of the medium with a smeared distribution of the ion charge / A. A. Rubashkin, M. A. Vorotyntsev, E. M. Antipov and others // Dokl. Phys. Chem. – 2015. - V. 464(1) – P. 198-201.
- Rubashkin A. A. Electrostatic contribution to the ion solvation energy: overscreening effect in the nonlocal dielectric response of the polar medium / A. A. Rubashkin, M. A. Vorotyntsev // Curr. Phys. Chem. – 2016. – V. 6(2). – P. 120-129.
- Dogonadze R. Polar-solvent structure in theory of ionic solvation / R. Dogonadze, A. A. Kornyshev // J. Chem. Soc. Faraday Trans. Pt.II. – 1974. - V. 70. – P. 1121-1132.
- Vorotyntsev M.A. Model nonlocal electrostatics. II. Spherical interface / M. A. Vorotyntsev // J. Phys. C: Solid State Physics – 1978. - V. 11. – P. 3323-3331.
- Vorotyntsev M. A. Elektrostatika sred s prostranstvennoj dispersiej [Electrostatics of media with spatial dispertion] / M. A. Vorotyntsev, A. A. Kornyshev - M. : Nauka, 1993. - 240 p. [in Russian]
- Gourary B. S. Wave function for electron-excess color centers in alkali halide crystals / B. S. Gourary, F. J. Adrian // Solid State Phys. – 1960. - V. 10. – P. 127-247.
- Fawcett W. R. Thermodynamic parameters for the solvation of monatomic ions in water / W. R. Fawcett // J. Phys. Chem. – 1999 - V. 103. – P. 11181-11185.
- Marcus Y. Thermodynamics of Solvation of Ions. Part 5 - Gibbs Free Energy of Hydration at 298.15 K / Y. Marcus // J. Chem. Soc. Faraday Trans. – 1991 - V. 87(18) – P. 2995-2999.
- Fedorov M. V. Unravelling the solvent response to neutral and charged solutes / M. V. Fedorov, A. A. Kornyshev // Molecular Physics – 2007 – V. 105 – P. 1-16.
- Randles J. E. B. The real hydration energies of ions / J. E. B. Randles // Trans. Faraday Soc. – 1956 – V. 52 – P. 1573-1581.
- Salomon M. Thermodynamics of ion solvation in water and propylene carbonate / M. Salomon // J. Phys. Chem. B – 1970 – V. 74 (12) – P. 2519-2524.
